Материал: 105-109
Вопрос 105 Белки сыворотки крови, биологическая роль основных фракций белков, значение их определения для диагностики заболеваний
Группа |
Белки |
Концентрация в сыворотке крови, г/л |
Функция |
Альбумины |
Транстиретин |
0,25 |
Транспорт тироксина и трийодтиронина |
|
Альбумин |
40 |
Поддержание осмотического давления, транспорт жирных кислот, билирубина, жёлчных кислот, стероидных гормонов, лекарств, неорганических ионов, резерв аминокислот |
α1-Глобулины |
α1 -Антитрипсин |
2,5 |
Ингибитор протеиназ |
|
ЛПВП |
0,35 |
Транспорт холестерола |
|
Протромбин |
0,1 |
Фактор II свёртывания крови |
|
Транскортин |
0,03 |
Транспорт кортизола, кортикостерона, прогестерона |
|
Кислый α1-гликопротеин |
1 |
Транспорт прогестерона |
|
Тироксинсвязывающий глобулин |
0,02 |
Транспорт тироксина и трийодтиронина |
α2-Глобулины |
Церулоплазмин |
0,35 |
Транспорт ионов меди, оксидоредуктаза |
|
Антитромбин III |
0,3 |
Ингибитор плазменных протеаз |
|
Гаптоглобин |
1 |
Связывание гемоглобина |
|
α2-Макроглобулин |
2,6 |
Ингибитор плазменных протеиназ, транспорт цинка |
|
Ретинолсвязыва-ющий белок |
0,04 |
Транспорт ретинола |
|
Витамин D связывающий белок |
0,4 |
Транспорт кальциферола |
β-Глобулины |
ЛПНП |
3,5 |
Транспорт холестерола |
|
Трансферрин |
3 |
Транспорт ионов железа |
|
Фибриноген |
3 |
Фактор I свёртывания крови |
|
Транскобаламин |
25×10-9 |
Транспорт витамина B12 |
|
Глобулин связывающий белок |
20×10-6 |
Транспорт тестостерона и эстрадиола |
|
С-реактивный белок |
<0,01 |
Активация комплемента |
γ-Глобулины |
IgG |
12 |
Поздние антитела |
|
IgA |
3,5 |
Антитела, защищающие слизистые оболочки |
|
IgM |
1,3 |
Ранние антитела |
|
IgD |
0,03 |
Рецепторы В-лимфоцитов |
|
IgE |
<0,01 |
Реагин |
В плазме крови здорового человека при электрофорезе на бумаге можно
обнаружить 5 фракций, при электрофорезе в полиакраламидном геле – 17 фракций.
Функции белков плазмы крови:
Поддержание осмотического давления (т.к. они связывают воду и удерживают ее в кровеносном русле)
Образуют буферную систему крови, поддерживающую pH крови
в пределах 7,37-7,43
Определяют вязкость крови (играют роль в гемодинамике кровенос. системы)
Являются резервом аминокислот для организма
Осуществляют защитную функцию (белки свертывающей системы,
α1-антитрипсин, белки системы комплимента)
Транспортная функция (альбумины)
Синтез: большинство белков плазмы синтезируются в печени, но некоторые
образуются и в других органах. γ- глобулины синтезируются В-лимфоцитами, большинство пептидных гормонов секретируют эндокринные железы, а гормон эритропоэтин образуется в почках.
Строение: почти все белки плазмы (кроме альбумина), являются
гликопротеинами. Олигосахариды присоединяются к белкам, образуя гликозидные связи с ОН группой серина или треонина, или с СООН аспарагина. Концевой остаток олигосахаридов – N-ацетилнейраминовая кислота, соединённая с галактозой.
Утилизация состарившихся белков: фермент эндотелия сосудов нейраминидаза
гидролизует связь между N-ацетилнейраминовой к-той и галактозой, и последняя становится доступной для специфических рецепторов гепатоцитов. Путём эндоцитоза "состарившиеся" белки поступают в клетки печени и разрушаются.
Т1/2 белков плазмы – от нескольких часов до нескольких недель.
Диспротеинемии – изменение соотношения содержания белков в плазме крови
по сравнению с нормой. Имеет относительную диагностическую ценность, т.к. одинаковые показатели на электрофореграмме могут быть при различных заболеваниях.
Нефротический синдром –для него характерно снижение альбуминов, α1- и
γ-глобулинов и увеличение α2- и β-глобулинов.
Снижение гуморального иммунитета – уменьшение фракции γ-глобулинов,
говорит об уменьшении содержания IgG, но не отражает изменение IgA и IgM
Белки острой фазы – белки, содержание которых повышается при
воспалительных процессах, ожогах, травмах, инфаркте миокарда
Основной индуктор синтеза белков острой фазы в гепатоцитах – полипептид
интерлейкин-1, освобождающийся из мононуклеарных фагоцитов.
К белкам острой фазы относят:
С-реактивный белок, α1-антитрипсин, гаптоглобин, кислый гликопротеин, фибриноген.
1. С-реактивный белок (называется так, потому что взаимод. с С-полисахаридом
пневмококков) может стимулировать систему комплемента, и его концентрация в крови, при обострении ревматоидного артрита может возрастать в 30 раз по сравнению с нормой.
2. α1–антитрипсин – относят к α1-глобулинам. Он ингибирует ряд протеаз, кот.
обр. в острой фазе воспаления, фермент эластазу, освобождающийся из нейтрофилов и разрушающий эластин альвеол лёгких.
При недостаточности α1-антитрипсина могут возникнуть эмфизема лёгких и
гепатит, приводящий к циррозу печени.
Существует несколько полиморфных форм α1-антитрипсина, одна из которых –
патологическая. У людей, гомозиготным по 2 дефектным аллелям этого гена, в печени синтезируется α1-антитрипсин, который обр. агрегаты, разрушающие гепатоциты => нарушается его секреция гепатоцитами => снижается его содержание в крови
3. Гаптоглобин – составляет четверть всех α2-глобулинов. При внутрисосудистом
гемолизе эритроцитов образует комплекс с гемоглобином, который разрушается в макрофагах.
Если свободный Hb может фильтроваться через почечные клубочки или
агрегировать в них, то комплекс гемоглобин-гаптоглобин имеет слишком большую молекуляр. массу, чтобы пройти через гломерулы. Образование такого комплекса предотвращает потери организмом железа, содержащегося в гемоглобине.
Снижение концентрации гаптоглобина в крови наблюдают при гемолитической
анемии (Т1\2 гаптоглобина – 5 дней, а его комплекса с Hb – 90 мин; при гемолизе
эритроцитов свободный Hb связывает свободный гаптоглобин => его конц. резко↓)
Альбумин – синтезируется в печени, имеет небольшую молекуляр. массу.
Молекула альбумина содержит много дикарбоновых АК, поэтому удерживает Na+, Ca2+, Zn2+. Обеспечивает до 80% осмотического давления плазмы.
Гипоальбуминемия – пониженное содержание альбуминов в плазме крови.
Возникает вследствие снижения его синтеза при забол. Печени (цирроз), при повышении проницаемости капилляров, при потерях белка из-за обширных ожогов или катаболич. состояний (сепсис, злокач. образования), при нефротическом синдроме, сопровождающимся альбуминурий, и при голодании.
Гипоальбуминемия вызывает снижение онкотического давления крови, что
приводит к возникновению отеков.
Гиперальбуминемия наблюдается при обезвоживании организма.
Альбумин является важнейшим транспортным белком. Он транспортирует,
свободные жирные кислоты, неконъюгированный билирубин, триптофан, тироксин, трииодтиронин. Многие ЛС связывают с альбумином (аспирин, сульфаниламиды), что нужно учитывать при лечении патологий, сопровожд. гипоальбуминемией – в этих случаях повышается конц. свободного ЛС в крови.
α-глобулины – их повышение в крови наблюдается при воспалит. процессах,
стрессовых воздействиях на организм (травмы, ожоги, инфаркт миокарда и др.). Это белки острой фазы.
Уменьшение альфа-глобулинов – при угнетении их синтеза в печени, гипотиреозе.
Степень увеличения альфа-глобулинов:
Отражает интенсивность процесса
Отмечается при острых гнойных заболеваниях, вовлечении в патологический процесс соединительной ткани (ревматизм, системная красная волчанка и др.)
Возможно также при некоторых хронических заболеваниях, злокачественных новообразованиях, особенно при их метастазировании.
β-глобулины – этой фракции присутствуют липопротеиды, поэтому
количество β-глобулинов увеличивается при гиперлипопротеидемиях. Это наблюдается при атеросклерозе, сахарном диабете, гипотиреозе, нефротическом синдроме.
γ-глобулины – их повышение наблюдается при усилении иммунных процессов.
Оно обусловлено повышенной продукцией иммуноглобулинов классов G, A, M, D, Е и наблюдается при острых и хронических вирусных, бактериальных, паразитарных инфекциях, заболеваниях соединительной ткани (коллагенозах), злокач. новообразованиях
Уменьшение γ-глобулинов отмечается при заболеваниях и состояниях,
связанных с истощением, угнетением иммунной системы (хронические воспалительные процессы, аллергия, злокачественные заболевания в терминальной стадии, длительная терапия стероидными гормонами, СПИД)
Вопрос 106
Убрали из списка
Вопрос 107 Коллаген: особенности аминокислотного состава, первичной и пространственной структуры. Особенности биосинтеза и созревания коллагена. Роль аскорбиновой кислоты в созревании коллагена
Коллагены – семейство родственных фибриллярных белков, секретируемых
клетками соединительной ткани. Самые распространённые белки межклеточного матрикса и организма в целом, составляют около 1/4 всех белков организма человека.
Являются осн. белковым элементом кожи, костей, сухожилий, хрящей, сосудов, зубов
В разных тканях преобладают разные типы коллагена:
1. В пластинчатой костной ткани, из которой построены плоские и трубчатые
кости, коллагеновые волокна имеют строго ориентированное направление:
Продольное – в центральной части пластинок
Поперечное и под углом – в периферической.
Это способствует тому, что даже при расслоении пластинок, фибриллы одной
пластинки могут продолжаться в соседние, создавая таким образом единую волокнистую структуру кости. Поперечно ориентированные коллагеновые волокна могут вплетаться в промежуточные слои между костными пластинками, благодаря чему достигается прочность костной ткани.
2. В сухожилиях коллаген образует плотные параллельные волокна, которые дают
возможность этим структурам выдерживать большие механические нагрузки.
3. В хрящевом матриксе коллаген образует фибриллярную сеть, которая придаёт
хрящу прочность, а в роговице глаза коллаген участвует в образовании гексагональных решёток десцеметовых мембран, что обеспечивает прозрачность роговицы, а также участие этих структур в преломлении световых лучей.
4. В дерме фибриллы коллагена ориентированы таким образом, что формируют
сеть, особенно хорошо развитую в участках кожи, которые испытывают сильное давление (кожа подошв, локтей, ладоней), а в заживающей ране они агрегированы весьма хаотично
Молекулы коллагена образуют полимеры – фибриллы коллагена, которые
обладают огромной прочностью и практически нерастяжимы. Механические свойства с их первичной и пространственной структурами.
Молекулы коллагена состоят из 3х ППЦ, называемых α-цепями.
Первичная структура α-цепей коллагена (тропоколлаген) – трёхцепочная правозакрученная суперспиральная молекула
В коллагене отсутствуют АК: цистеин, триптофан, но содержится необычная АК –
гидроксилизин. Каждая 3-я АК – глицин.
ППЦ коллагена можно представить как последовательность:
Гли-Х-У (где Х, У – другие АК)
Спираль коллагена стабилизирована за счет стерического отталкивания
пирролидиновых колец в остатках пролина
Цепи удерживаются друг около друга за счёт водородных связей, возникающих
между амино- и карбоксильными группами пептидного остова разных ППЦ
"Жёсткие" аминокислоты – пролин и гидроксипролин – ограничивают вращение
полипептидного стержня и увеличивают тем самым стабильность тройной спирали. Глицин, имеющий вместо радикала атом водорода, всегда находится в месте
пересечения цепей; отсутствие радикала позволяет цепям плотно прилегать друг к другу
В результате такого скручивания пептидных остовов ППЦ и наличия удлинённой структуры два других радикала из триады аминокислот Гли-X-Y оказываются на наружной поверхности молекулы тропоколлагена.
Коллагеновые фибриллы формируются при объединении комплементарных
участков молекул тропоколлагена, причём эти участки расположены таким образом, что одна нить тропоколлагена сдвинута по отношению к другой примерно на ¼. Между радикалами АК возникают ионные, водородные и гидрофобные связи.
Роль модифицированных АК:
Гидроксильные группы гидроксипролина соседних цепей тропоколлагена
образуют водородные связи, укрепляющие структуру коллагеновых фибрилл.
Радикалы лизина и гидроксилизина необходимы для образования прочных
поперечных сшивок между молекулами тропоколлагена, ещё сильнее укрепляющие структуру коллагеновых фибрилл.
Синтез и созревание коллагена – сложный многоэтапный процесс,
начинающийся в клетке, а завершающийся в межклеточном матриксе.
Синтез и созревание коллагена включают в себя ряд посттрансляционных изменений:
Гидроксилирование пролина и лизина с образованием
гидроксипролина (Hyp) и гидроксилизина (Hyl)
Гликозилирование гидроксилизина
Частичный протеолиз – отщепление "сигнального" пептида,
а также N- и С-концевых пропептидов
Образование тройной спирали
Синтез полипептидных цепей коллагена: ППЦ коллагена синтезируются на
полирибосомах, связанных с мембранами ЭР, в виде более длинных, чем зрелые цепи, предшественников – препро-α-цепей, у кот. имеется гидрофобный "сигнальный" пептид на N-конце. Функция сигнального пептида – ориентация синтеза пептидных цепей в полость ЭР, после выполнения которой он сразу же отщепляется.
Синтезированная молекула проколлагена содержит дополнительные участки –
N- и С-концевые пропептиды, в состав которых входят остатки цистеина, которые образуют внутри- и межцепочечные (только в С-пептидах) S-S-связи.
Концевые пропептиды не образуют тройную спираль, а формируют глобулярные домены. Отсутствие N- и С- концевых пептидов в структуре проколлагена нарушает правильное формирование тройной спирали.
Посттрансляционные модификации коллагена:
1. Гидроксилирование пролина и лизина начинается в период трансляции
коллагеновой мРНК на рибосомах и продолжается на растущей полипептидной цепи вплоть до её отделения от рибосом. После образования тройной спирали дальнейшее гидроксилирование пролиловых и лизиловых остатков прекращается.
Реакции гидроксилирования катализируют оксигеназы.
Пролиловые и лизиловые остатки в Y-положении пептида (Гли-Х-У)n
подвергаются действию, соответственно, пролил-4-гидроксилазы и лизил-5-гидроксилазы. Пролил-3-гидроксилаза действует на некоторые остатки пролина в Х-положениях.
Необходимыми компонентами этой реакции являются альфа-кетоглутарат, О2 и
витамин С (аскорбиновая кислота). Донором атома кислорода, который присоединяется к С-4 пролина, является молекула О2, второй атом О2 включается в сукцинат, который образуется при декарбоксилировании α-кетоглутарата, а из карбоксильной группы
α-кетоглутарата образуется СО2.
Роль аскорбиновой кислоты: гидроксилазы пролина и лизина содержат в активном центре атом железа Fe2+. Для сохранения атома железа в ферроформе необходим восстанавливающий агент – это аскорбин. К-та (кофермент гидроксилаз), которая легко окисляется в дегидроаскорбиновую кислоту. Обратное превращение происходит в ферментативном процессе за счёт восстановленного глутатиона
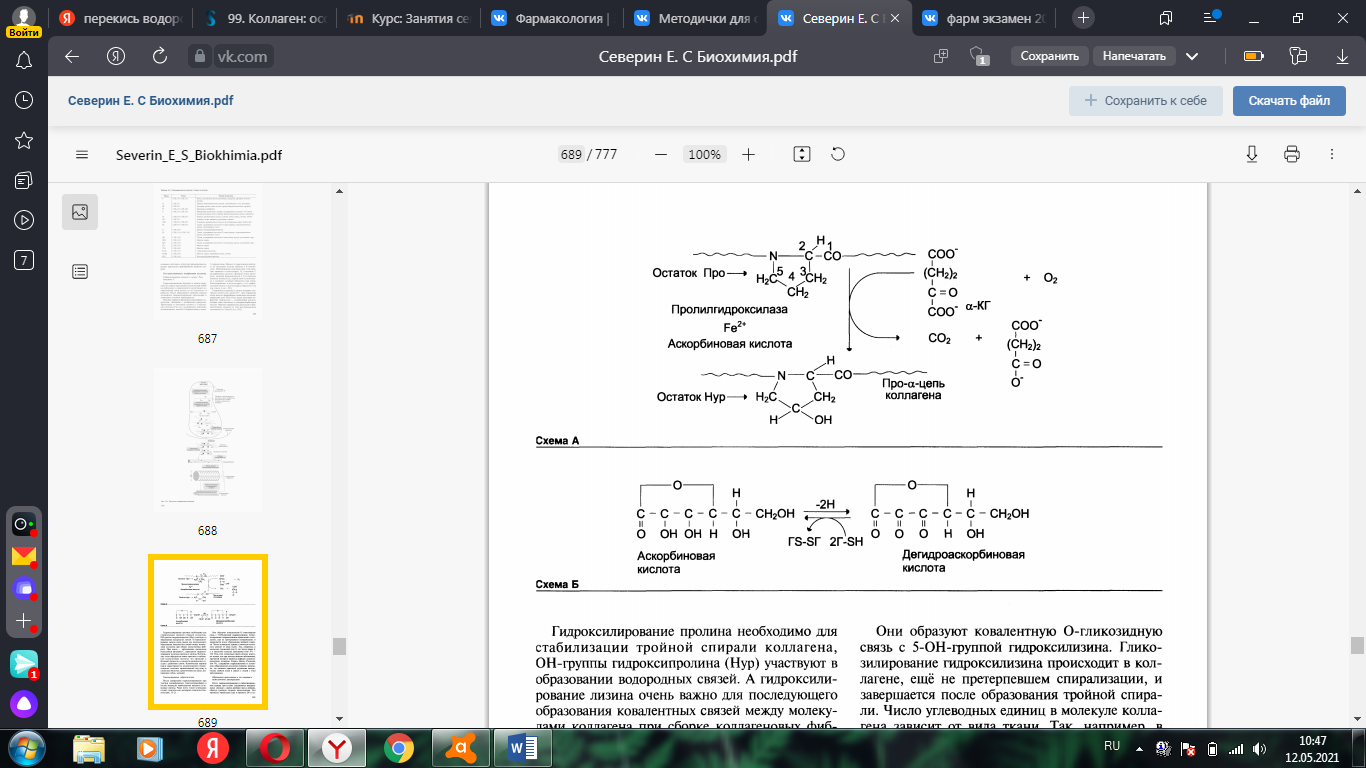
Гидроксилирование пролина необходимо для стабилизации тройной спирали
коллагена, ОН-группы гидроксипролина (Hyp) участвуют в образовании водородных связей. А гидроксилирование лизина очень важно для последующего образования ковалентных связей между молекулами коллагена при сборке коллагеновых фибрилл.
При цинге (заболевании, вызванном недостатком вит. С), нарушается
гидроксилирование остатков пролина и лизина. В результате образуются менее прочные и стабильные коллагеновые волокна, что приводит к большой хрупкости и ломкости кровеносных сосудов с развитием цинги => множествен. точечные кровоизлияния под кожу и слизистые, кровоточивость дёсен, выпадение зубов, анемия.
2. Гликозилирование гидроксилизина: по окончании гидроксилирования в
состав молекулы проколлагена вводятся углеводные группы (галактоза или дисахарид галактозилглюкоза). Они образуют ковалентную О-гликозидную связь с 5-ОН-группой гидроксилизина.