Материал: 1 Классификация и основные свойства материалов
1. Петров К.С. Радиоматериалы, радиокомпоненты и электроника: Учебное пособие для студентов Вузов-СПб.:Питер, 2003 г.
2. Пасынков В.В. Материалы электронной техники: Учебное пособие для студентов вузов – 5-е изд., - СБб.: Лань, 2003.
3. Хадыкин А.М. Радиоматериалы и радиокомпоненты. Конспект лекций ОГТУ Омск 2008 г.
4. Ястребов А.С., Волокобинский М.Ю., Сотенко А.С. Радиоматериалы и радиокомпоненты: Учебник АСАДЕМА Москва Издательский центр «Академия» 2011 г.
5. Чернышева Т.И., Кольтюков Н.А. Радиоматериалы и радиокомпоненты. Учебное пособие. ТГТУ. Тамбов 2012 г.
6. И.К. Мешковский, А.Ф. Новиков, А.В. Токарев Химия радиоматериалов. Учебное пособие. СПб.: НИУ ИТМО 2015 г
7. Постникова В.Н., Кузнецов С.Н., Каширин Ю.В. Материалы электронных средств. Учебное пособие к лабораторным работам. М.: Изд.МАИ, 2006.
Тема1. Классификация радиотехнических материалов.
По отношению к электрическому полю все радиоматериалы подразделяются на три основные группы:
электроизоляционные (диэлектрические) материалы
полупроводниковые
проводниковые
Особое место занимают магнитные материалы.
В основе подразделения материалов на три группы лежит зонная теория твердого тела. Расположение энергетических зон показано на рис.1.
1

1. Зона проводимости
![]()
 2
2
 2. запрещенная
зона
2. запрещенная
зона
3. валентная зона
При заполнении электронами энергетических зон могут быть три случая:
1. Валентная зона заполнена целиком, при Т = Табс.нуля. зона проводимости пуста, ширина запрещенной зоны велика ∆Е>3 эв. Соответствующая этому случаю группа материалов носит название диэлектрики. ρ v=106÷1018 Ом*м. при Т↑, ρ v ↓.
Эта группа занимает ведущее положение по количеству, разнообразию материалов и ассортименту. Диэлектрики используются в газообразном, жидком и твердом состоянии.
Твердые диэлектрики представляют наиболее многочисленную группу, которая по составу и структуре подразделяются на:
органические
неорганические
элементарные
По применению:
Низкочастотные
Высокочастотные
2. Валентная зона заполнена целиком, при Т = Табс. нуля зона проводимости пуста, а ∆Е<3 Эв. Эта группа материалов – полупроводники. ρ v=10-5÷106 Ом*м . При Т↑, ρ v ↓.
Между диэлектриками и полупроводниками нет качественной разницы, только по ширине запрещенной зоны. Эта группа материалов в настоящее время занимает ведущее положение по применению и значимости материалов электронной техники.
Полупроводники могут быть в твердом и жидком состоянии (Bi2S3 Sb2S3 Cu2S). Практическое применение находят в основном твердые полупроводники.
Полупроводники подразделяются на:
Элементарные полупроводники Ge, Si.
Неорганические полупроводниковые соединения GaAs, GaP, SiC
Органические полупроводниковые соединения.
3. Запрещенная зона практически равна нулю и валентная зона перекрывается с зоной проводимости. Эта группа материалов - проводники. Качественное отличие от двух предыдущих групп заключается в том, что при Т= Табс. нуля в зоне проводимости имеются свободные носители заряда.
ρ v=10-8÷10-5 Ом*м, при Т↑, ρ v ↑.
Проводники подразделяются на:
Проводниковые материалы с высокой удельной проводимостью или с малым удельным сопротивлением (алюминий, серебро, медь, золото, платина, палладий)
Проводниковые материалы с высоким удельным сопротивлением (манганин, константан, нихром).
Магнитные материалы по величине удельного сопротивления могут относиться к одной из трех выше перечисленных групп, но обладают особыми свойствами.
По отношению к магнитному полю все радиоматериалы подразделяются на следующие группы:
диамагнетики
парамагнетики
ферромагнетики
антиферромагнетики
ферримагнетики (ферриты).
По свойствам и применению подразделяются на:
магнитомягкие материалы МММ
магнитотвердые МТМ
магнитные материалы специального назначения.
По агрегатному состоянию все радиоматериалы подразделяются на три группы:
Твердые
Жидкие
Газообразные
Твердые материалы могут быть: кристаллические или аморфные.
Кристаллические твердые материалы разделяют на поликристаллы и монокристаллы.
Кристалл - это структура, состоящая из частиц, обладающих упорядоченным расположением, которое сохраняется по всему объему каждого кристаллического зерна.
Кристаллическое зерно - область кристалла, внутри которой сохраняются неизменными направления кристаллических осей.
В аморфных веществах (в диэлектриках и в жидкостях) такого порядка не наблюдается.
Для описания правильной внутренней структуры кристаллов пользуются понятием Кристаллической решетки.
Кристаллическая решетка - это пространственная сетка в узлах которой располагаются частицы (атомы, ионы или молекулы), образующие кристалл.
В основе кристаллической решетки лежит элементарная кристаллическая ячейка.
Монокристалл- единичный кристалл. Для этой структуры характерно:
анизотропия
однородность
несовершенство
Монокристаллы представляют наибольший интерес т.к. на них базируется вся полупроводниковая технология.
Поликристалл –это структура хаотически ориентированных зерен. 1зерно≈10мкм, в 1 см3≈109 шт. зерен.
Анизотропия кристаллов.
Изотропностью называют независимость физических свойств тела от направления внутри него. В противном случае тело обладает анизотропией, т.е. неодинаковостью свойств по разным направлениям (например для механических модулей, температурный коэффициент расширения, удельное сопротивление, показатель преломления и т.д.).
Анизотропия - характерная особенность кристаллов, а проявляется она только у монокристаллов.
Пример анизотропии механической прочности кристалла - способность кристаллов слюды легко расщепляться на тонкие листочки по определенному направлению и обладать достаточной прочностью в перпендикулярном направлении (тоже у полупроводников).
Классификация кристаллов по типам внутренних связей.
Кристаллическое состояние является нормальным состоянием твердого вещества, аморфное - нарушенным, временным состоянием. Поэтому в кристаллическом состоянии вещество обнаруживает свои физические свойства в самом чистом виде и в самых богатых сочетаниях, а в аморфном веществе свойства как бы затушеваны.
При сближении атомов на расстоянии порядка нескольких ангстрем (1А = 10-10 м), между ними проявляются силы взаимодействия и между частицами, из которых состоит вещество возникают различные виды химических связей. Различие в свойствах материалов определяется видом химической связи. Рассмотрим некоторые из них.
Если эти силы являются силами притяжения, то атомы могут соединяться с выделением энергии, образуя химические соединения. При этом электроны внутренних и внешних оболочек атомов ведут себя по разному. Электроны внутренних, полностью заполненных оболочек прочно связаны с ядром и не участвуют в образовании химических связей. Строение внешней, не полностью заполненной электронами оболочки определяет химические свойства атомов в образовавшемся соединении.
Электроны, находящиеся на внешних оболочках, являются валентными. Валентность атома определяется числом этих электронов.
Все многообразие существующих в природе материалов характеризуется несколькими видами химической связи.
Ковалентная (гомеополярная) связь. При наличии такой связи объединение атомов в молекулу достигается за счет электронов, которые становятся общими для пар атомов (рис. 1.). Плотность отрицательно заряженного электронного облака между положительно заряженными ионами получается наибольшей. Появление состояния с повышенной плотностью электронного заряда в межионном пространстве приводит к возникновению сил притяжения между атомами.
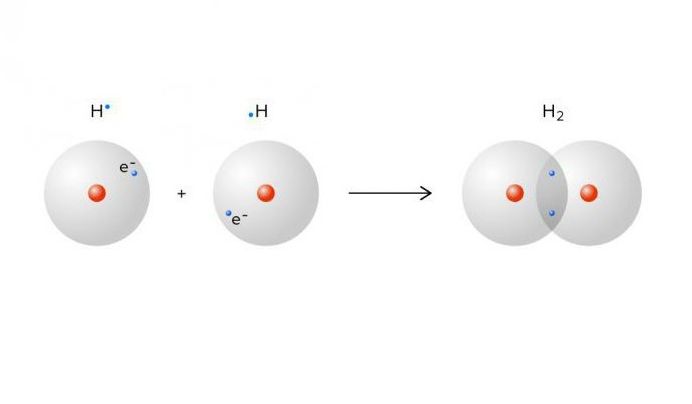
Рис. 1 Ковалентная связь, формирующая молекулу водорода H2 (справа), где два атома водорода перекрывают два электрона
Ковалентная связь характерна как для органических, так и для неорганических соединений. К неорганическим веществам с ковалентной связью относятся алмаз, кремний, германий, арсенид галлия (GaAs), карбид кремния (SiС) и другие, являющиеся полупроводниками. Многие полупроводники кристаллизируются в структуре алмаза, в которой каждый атом образует четыре связи со своими ближайшими соседями. Ковалентная связь в неорганических материалах характеризуется высокой прочностью. Подтверждением этому является высокая твердость и температура плавления алмаза, кремния и др. В зависимости от симметрии строения эти молекулы могут быть симметричными и ассиметричными.
В симметричных молекулах центры положительного и отрицательного зарядов совпадают, такие молекулы называют неполярными.
В ассиметричных молекулах центры положительного и отрицательного зарядов не совпадают, такие молекулы называют полярными (диполями).
Особенности:
резкое изменение свойств материала при переходе от монокристалла к поликристаллу (отсутствие однородности, анизотропии)
более прочные чем монокристаллы
менее требовательны к чистоте обработки
более дешевые чем монокристаллы
Эпитаксиальная структура – ориентированно наращенный кристалл при температуре меньшей температуры плавления.
Эпитаксия- ориентированный рост пленки или слоя данного материала на монокристаллической подложке.
Р=0 + -
Н H
│ │
H─ C ─H H─ C─H p=q*l
│ │

H Cl
Ионная (гетерополярная) связь. Наблюдается в химических соединениях атомов металла с металлоидными атомами (типа NaCl). Ионная связь возникает вследствие перехода валентных электронов от металла к металлоиду и возникновения электростатического притяжения разноименно заряженных ионов друг другу. Способность атома захватывать электрон при образовании ионной химической связи называется электроотрицательностью. Чем больше разность электроотрицательностей атомов, участвующих в образовании химической связи, тем прочнее ионное соединение. В узлах кристаллической решетки находятся разноименно заряженные ионы, связанные силой Кулоновского взаимодействия. Такая связь характерна для неорганических диэлектриков. Самым типичным примером ионных кристаллов являются галоидные соли щелочных металлов.
Металлическая связь. Имеет место в металлах. В узлах кристаллической решетки находятся положительные ионы находящиеся в среде свободных коллективизированных электронов. Общее у металлической и ковалентной связи – наличие обобществленных электронов. Отличие - в обобществлении электронов участвуют все атомы. Обобщенные электроны не локализируются вблизи своих атомов, а свободно перемещаются внутри решетки, образуя «электронный газ». Притяжение между положительными ионами и «электронным газом» определяет целостность металлов. Наличие свободных электронов придает металлам высокую электро- и теплопроводность.
Молекулярная связь (связь Ван-дер-Вальса). Наблюдается у ряда веществ с ковалентными внутримолекулярными связями. Это наиболее слабая связь, энергия ее примерно на два порядка меньше энергии ионной и ковалентной связей. Вещества с молекулярной связью (парафин, жидкие кристаллы) характеризуются сравнительно низкой температурой плавления и невысокой механической прочностью. Наиболее характерна органическим диэлектрикам.
Расположение частиц в кристаллической решетке. (плотное или неплотное, тип плотной упаковки) определяет свойства материала.
Странная история произошла однажды зимой. В конце прошлого века в Петербурге на одном из складов военного обмундирования простудились и заболели солдатские пуговицы. Пуговицы в те времена делали из олова. На холодном не отапливаемом складе лежали большие запасы белых начищенных пуговиц. Не обратили внимания, что верхние пуговицы стали темнеть. Продолжали темнеть, теряли блеск и рассыпались в порошок. При этом они как бы заражали соседние, с которыми происходило тоже самое. Разрушение распространилось как чума. Все имущество погибло от «оловянной чумы».
Что же происходит с оловом. Эта «болезнь» - результат перестройки атомов в кристаллическом слое.
Есть две модификации олова: обычное серебристо-белое олово, ковкий металл, в виде больших монокристаллов. Белое олово получается при температурах более 13,2о С. Если же температура ниже, атомы могут перестроиться и образовать другую разновидность хрупкого неметаллического серого олова.
Свойства этих двух модификаций совершенно различны. Плотность белого олова 7,3 г/см3, серого – 5,8 г/см3, а температурный коэффициент объемного расширения у серого в четыре раза больше, поэтому при переходе из белой разновидности в серую, олово резко меняет свой объем и рассыпается.
При температуре ниже 13,2оС решетка белого олова становится неустойчивой, атомы олова немного расступаются, строй их меняется - образуется серое олово.