Материал: Загрязнение и очистка воздуха от тепловых электростанций
![]() (14)
(14)
где Сф = 0, т.к. нет дополнительных источников загрязнения. Полученное
значение ![]() подставляем в уравнения 2; 3; 4
(стр. 16 -17) для расчета значений ƒ1
подставляем в уравнения 2; 3; 4
(стр. 16 -17) для расчета значений ƒ1![]() m1
m1![]() и для определения n1.
и для определения n1.
Расчет минимальной высоты трубы во втором и последующих приближениях, Н2
и Нn:
![]() (15)
(15)
![]()
Рассчитываем значения Сm с
минимальной высотой трубы, т.е. с подобранной величиной ![]() , причем все остальные величины
рассчитаны ранее по уравнениям 2; 3; 4
, причем все остальные величины
рассчитаны ранее по уравнениям 2; 3; 4
![]() = 0,163 (16)
= 0,163 (16)
способ снижения величины выброса - за счет увеличения СЗЗ. Сравним
рассчитанное значения ![]() (с учетом
(с учетом ![]()
![]()
![]() . Если
. Если![]() , то рассчитаем расстояния СЗЗ с учетом розы ветров для горячего
источника.
, то рассчитаем расстояния СЗЗ с учетом розы ветров для горячего
источника.
ПДК>![]()
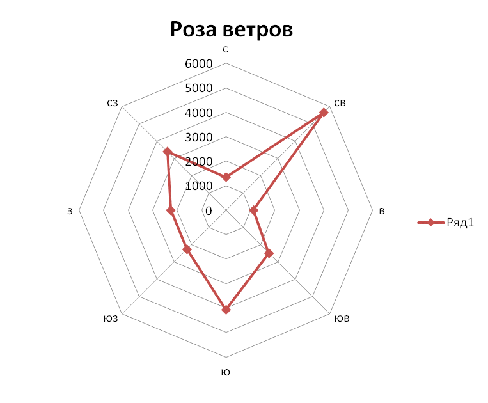
Построение розы ветров
Расчет расстояния от источника до внешней границы СЗЗ без учета розы
ветров (L0). Причем, используем величины: ![]() рассчитанная по уравнению (1);
рассчитанная по уравнению (1); ![]() рассчитанная по уравнению (6):
рассчитанная по уравнению (6):
![]() = 1803,4 (17)
= 1803,4 (17)
где ![]() = 0,638 (18)
= 0,638 (18)
где ![]() (19)
(19)
Расчет расстояния СЗЗ до ее внешней границы по восьми румбам с учетом вытянутости среднегодовой розы ветров.
Lс = L0 ![]() (Pn / P0) = 1352,5 м
(Pn / P0) = 1352,5 м
Lю = 5635,6 м
Lз= 1127,1 м
Lв= 3381,3 м
Lюз = 2479,6 м
Lюв = 4057,6 м
Lсз= 2254,2 м
Lсв=
2254,2 м
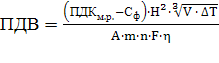 = 1772
= 1772![]()
Данное значение превышает ПДК выброса в окружающую среду, поэтому
необходимо установить очистное оборудование.
|
|
|
|
|
|
|
|
|
|
ПДВ |
|
|
0,783 |
1364,41 |
0,239 |
64,12 |
2373 |
855 |
3512,04 |
4959 |
633 |
1772 |
0,5 |
Методы очистки газов
В настоящее время разработано и опробовано в промышленности большое количество различных методов очистки газов от технических загрязнений: NOx, SO2, H2S, NH3, оксида углерода, различных органических и неорганических веществ.
Опишем эти основные методы и укажем их преимущества и недостатки.
Абсорбционный метод.
Абсорбция представляет собой процесс растворения газообразного компонента в жидком растворителе. Абсорбционные системы разделяют на водные и неводные. Во втором случае применяют обычно малолетучие органические жидкости. Жидкость используют для абсорбции только один раз или же проводят ее регенерацию, выделяя загрязнитель в чистом виде. Схемы с однократным использованием поглотителя применяют в тех случаях, когда абсорбция приводит непосредственно к получению готового продукта или полупродукта. В качестве примеров можно назвать:
· получение минеральных кислот (абсорбция SO3 в производстве серной кислоты, абсорбция оксидов азота в производстве азотной кислоты);
· получение солей (абсорбция оксидов азота щелочными растворами с получением нитрит-нитратных щелоков, абсорбция водными растворами извести или известняка с получением сульфата кальция);
· других веществ (абсорбция NH3 водой для получения аммиачной воды и др.).
Схемы с многократным использованием поглотителя (циклические процессы) распространены шире. Их применяют для улавливания углеводородов, очистки от SO2 дымовых газов ТЭС, очистки вентгазов от сероводорода железно-содовым методом с получением элементарной серы , моноэтаноламиновой очистки газов от CO2 в азотной промышленности.
В зависимости от способа создания поверхности соприкосновения фаз различают поверхностные, барботажные и распыливающие абсорбционные аппараты.
В первой группе аппаратов поверхностью контакта между фазами является зеркало жидкости или поверхность текучей пленки жидкости. Сюда же относят насадочные абсорбенты, в которых жидкость стекает по поверхности загруженной в них насадки из тел различной формы.
Во второй группе абсорбентов поверхность контакта увеличивается благодаря распределению потоков газа в жидкость в виде пузырьков и струй. Барботаж осуществляют путем пропускания газа через заполненный жидкостью аппарат либо в аппаратах колонного типа с тарелками различной формы.
В третьей группе поверхность контакта создается путем распыления жидкости в массе газа. Поверхность контакта и эффективность процесса в целом определяется дисперсностью распыленной жидкости.
Общими недостатками абсорбционных методов является образование жидких
стоков и громоздкость аппаратурного оформления.
Метод очистки газов от диоксида серы с использованием твердых хемосорбентов <#"817744.files/image069.gif">
Рисунок 1 - Схема установки оксидно-марганцевой очистки дымовых газов от
диоксида серы:1 - адсорбер; 2 - циклон; 3 - электрофильтр; 4 - дымовая труба; 5
- аммонийный скруббер; 6 - реактор; 7 - сепаратор; 8 фильтр; 9 - кипятильник;
10 - кристаллизатор; 11-центрифуга; 12 - циклон
Недостатки:
значительные затраты на регенерацию;
необходимость выполнения реакционной аппаратуры из дорогостоящих материалов, так как процессы идут в условиях коррозионных и повышенных температурах.
отходящих газов в производствах серной кислоты и целлюлозы, на нефтеперерабатывающих предприятиях и др.
Сорбционная способность силикагелей по диоксиду серы составляет существенную величину даже при высоких температурах (150-200 °С) и низких концентрациях целевого компонента в газах [<1% (об.)], что объясняют происходящим окислением адсорбированного SO2 в SOS кислородом, содержащимся в обрабатываемых потоках. Регенерацию насыщенного поглотителя ввиду его негорючести можно проводить нагретым воздухом. Если в очищаемых газах содержатся пары воды, величина поглощения силикагелями диоксида серы резко уменьшается.
В качестве поглотителей диоксида серы из газов исследованы ионообменные смолы - аниониты; кислотостойкие цеолиты, в том числе природные.
Большинство сухих методов очистки газов от диоксида серы требует
значительных затрат тепла на регенерацию. Их реализация связана также с
повышенными капитальными затратами ввиду необходимости выполнения адсорбционной
аппаратуры из дорогостоящих специальных материалов. Это препятствует внедрению
адсорбционных процессов для очистки газов.
Расчет М (массы выброса после очистки)
Э=95%
![]()
![]()
![]()
Выводы по расчетам
В ходе работы была проведена экологическая экспертиза загрязнения атмосферного воздуха тепловой электростанцией.
Рассмотрено три варианта снижения выброса загрязняющего вещества:
· Снижение выброса за счет увеличения высоты трубы;
· Снижение выброса за счет увеличения санитарно защитной зоны;
· Снижение выброса установкой очистного оборудования.
Более выгодным вариантом, с точки зрения производительности и экологичности, является установка очистного оборудования, так как:
существенно снижаются выбросы загрязняющего вещества;
исключается необходимость в увеличении высоты трубы и санитарно защитной
зоны.
Химическая, физическая и токсикологическая характеристика диоксида серы
Диоксид серы - SO2. В нормальных условиях представляет собой бесцветный газ с характерным резким запахом (запах загорающейся спички), ядовит. Под давлением сжижается при комнатной температуре. Растворяется в воде с образованием нестойкой сернистой кислоты; растворимость 11,5 г/100 г воды при 20 °C, снижается с ростом температуры.
Раздражает дыхательные пути, вызывая спазм бронхов и увеличение сопротивления дыхательных путей. При воздействии SO2 в виде аэрозоля, образующегося при туманах и повышенной влажности воздуха, раздражающий эффект сильнее. При неблагоприятных метеорологических условиях может вызвать массовое отравление населения. Влажная поверхность слизистых поглощает SO2, затем последовательно образуются H2SO3 и H2SO4. Общее действие заключается в нарушении углеводного и белкового обмена; угнетении окислительных процессов в головном мозге, печени, селезенке, мышцах. Раздражает кроветворные органы.
Спектр поглощения SO2 в ультрафиолетовом диапазоне
Относится к кислотным оксидам. Растворяется в воде с образованием сернистой кислоты (при обычных условиях реакция обратима):
+ H2O ↔ H2SO3
Химическая активность SO2 весьма велика. Наиболее ярко выражены восстановительные свойства SO2, степень окисления серы в таких реакциях повышается.
Последняя реакция является качественной реакцией на сульфит-ион SO32− и на SO2 (обесцвечивание фиолетового раствора). В присутствии сильных восстановителей SO2 способен проявлять окислительные свойства.
диоксид
ветер газ труба
Список использованной литературы
. Рыжкин В. Я. Тепловые электрические станции. Под ред. В. Я. Гиршфельда. Учебник для вузов. 3-е изд., перераб. и доп. - М.: Энергоатомиздат, 1987. - 328 с.
. Елизаров Д.П. Теплоэнергетические установки электростанций: Учебник для вузов / Д.П. Елизаров. - М.: Энергоиздат, 1982. - 264 с.
. Баскаков А.П., Берг Б.В., Витт О.К. и др. Теплотехника: Учебник для вузов / Под ред. А.П. Баскакова. - М.: Энергоатомиздат, 1991. - 224с.