Материал: Задачи по биохимии
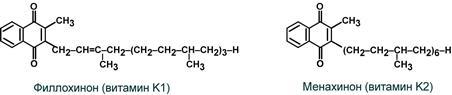
витамин обеспечивает:
1. Синтез факторов свертывания крови в печени – Кристмаса (ф.IX), Стюарта (ф.X), проконвертина (ф.VII), протромбина (ф.II);
2. Синтез белков костной ткани, например, остеокальцина.
3. Синтез протеина C и протеина S, участвующих в работе антисвертывающей системы крови.
Гиповитаминоз K
Причина
Возникает при подавлении микрофлоры лекарствами, особенно антибиотиками, при заболеваниях печени и желчного пузыря. У взрослых здоровая кишечная микрофлора полностью удовлетворяет потребность организма в витамине.
Клиническая картина
Наблюдается кровоточивость, снижение свертываемости крови, легкое возникновение подкожных гематом,
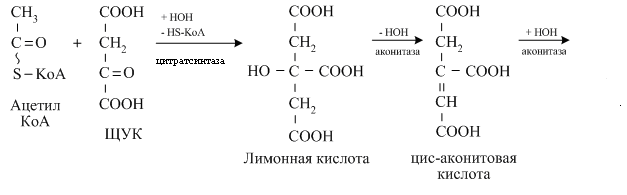
толерантность к глюкозе Изменение толерантности к глюкозе при сахарном диабете
|
|
У больных с СД после приёма пищи концентрация глюкозы в крови может достигать 300-500 мг/дл и сохраняется на высоком уровне в постабсорбтивном периоде, т.е. снижается толерантность к глюкозе. На стадии латентного СД концентрация глюкозы в крови натощак соответствует норме, а нагрузочные пробы уже выявляют снижение толерантности к глюкозе. Определение толерантности к глюкозе Обследуемый принимает раствор глюкозы из расчёта 1 г на 1 кг массы тела (сахарная нагрузка). Концентрацию глюкозы в крови измеряют в течение 2-3 ч с интервалами в 30 мин. 1 — у здорового человека; 2 — у больного сахарным диабетом. |
Серповидно-клеточная анемия
HbS – гемоглобин серповидно-клеточной анемии. При этом нарушении в ДНК в результате точковой мутации триплет ЦТТ заменен на триплет ЦАТ, что влечет за собой включение в 6-м положении β-цепи вместо глутамата аминокислоты валина. Изменение свойств β-цепи влечет изменение свойств всей молекулы и формирование на поверхности гемоглобина "липкого" участка. При дезоксигенации гемоглобина участок "раскрывается" и связывает одну молекулу дезоксигемоглобина S с другими подобными. Результатом является полимеризация гемоглобиновых молекул и образование крупных белковых тяжей, вызывающих деформацию эритроцитов и, при прохождении ими капилляров, гемолиз.
Изоферменты. Часть ферментов состоят не из одной белковой цепочки, а из нескольких субъединиц. Изоферменты – это семейство ферментов, которые катализируют одну и ту же реакцию, но отличаются по строению и физико-химическим свойствам.
Например: лактатдегидрогеназа (ЛДГ) состоит их 4 субъединиц 2хтипов: субъединица Н, выделенная из сер дечной мышцы (heart – сердце), субъединица М, выделенная из скелетных мышц (musculus – мышца). Эти субъединицы кодируются разными генами
ФОЛИЕВАЯ
КИСЛОТА (витамин В9 или Вс) фактор роста
(антианемический)
Гиперпродукция глюкокортикоидов (гиперкортицизм) может быть следствием повышения уровня АКТГ при опухолях гипофиза (болезнь Иценко-Кушинга) и опухолях других клеток (бронхов, тимуса, поджелудочной железы), вырабатывающих кортикотропинподобные вещества, или избыточного синтеза кортизола при гормонально-активных опухолях коры надпочечников (синдром Иценко-Кушинга).
При гиперкортицизме наблюдаются гипергликемия и снижение толерантности к глюкозе, обусловленные стимуляцией глюконеогенеза ("стероидный диабет"), усиление катаболизма белков, уменьшение мышечной массы, истончение кожи, остеопороз, инволюция лимфоидной ткани. Характерно своеобразное перераспределение отложений жира ("лунообразное лицо", выступающий живот).
ВИТАМИН
В12 - кобаламин – антианемический

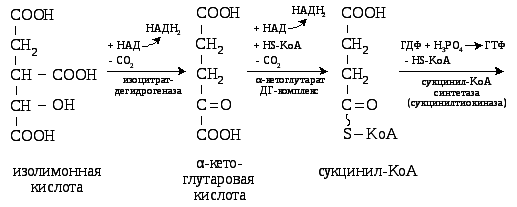
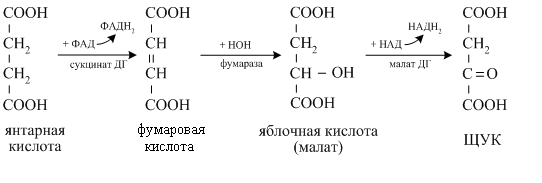
Энергетическая функция. Образовавшиеся в ЦТК 3 молекулы НАДН2в последующем окисляются в длинной ЦПЭ с образованием 9 молекул АТФ
Образовавшийся в ЦТК ФАДН2 окисляется в короткой ЦПЭ, давая энергию для синтеза 2 молекул АТФ.
В сукцинилтиокиокиназной реакции ЦТК непосредственно образуется 1 макроэрг – ГТФ (1 ГТФ = 1 АТФ).
Анаболическая функциязаключается в том, что некоторые метаболиты цикла Кребса не окисляются в нём, а используются для синтеза новых веществ.
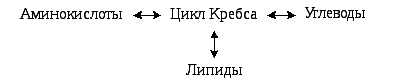
1. Ферменты
а) Химическая природа ферментов:
Ферменты(энзимы) — биологические катализаторы белковой природы, которые обеспечивают необходимые скорость и координацию биохимических реакций, составляющих обмен веществ(метаболизм).
б) Ферменты могут быть:
-
простыми
-
сложными (холоферменты) — имеют небелковую часть (белковая — апофермент, небелковая — простетическая группа (кофермент или кофактор)
Кофакторы — низкомолекулярные небелковые вещества, необходимые для реализации каталитической активности ферментов (биоорганические соединения разной химической природы или ионы металлов).
Ионы металлов либо связаны с апоферментом, либо входят в состав небелковой простетической группы — чаще всего порфиринового кольца геминовых ферментов (цитохромов, пероксидаз, каталазы).
Коферменты (коэнзимы) — биоорганические соединения небелковой природы, которые необходимы для действия фермента, а именно превращения субстрата в каталитическом акте.
Они могут соединяться с апоферментом нековалентными или ковалентными связями (в последнем случае они являются простетическими группами ферментного белка — флавиновые коферменты, перидоксальфосфат, липоевая кислота). Иногда коферменты образуют комплексы с апоферментом только в ходе каталитического процесса (НАД, НАДФ).
Классификация
-
по химической природе:
- производные витаминов (В1 — тиаминдифосфат, В2 — флавинмононуклеотид (ФМН), В6 — перидоксальфосфат (ПАЛФ), перидоксаминфосфат (ПАМФ), В3 — КоА, В12 — метилкобаламин (метил-В12), дезоксиаденозилкобаламин (DA-B12), Н (биотина) — карбоксибиотитн, В9 — тетрагидрофолиевая кислота(ТГФК)
- динуклеотиды (производные В2 — ФАД, В5 — НАД+, НАДФ+)
-нуклеотиды (производные пуринов и пиримидинов — АТФ, АДФ, ЦТФ, ЦДФ, УТФ, УДФ)
-комплексы порфиринов с ионами металлов
-
по типу катализируемой реакции:
-переносчики атомов водорода и электронов
-переносчики разных химических групп
-коферменты синтеза, изомеризации, расщепления углеродных связей
Самые распространенные:
НАД+, НАДФ+ входят в состав дегидрогеназ
ФАД, ФМН входят в состав дегидрогеназ и оксидаз
ПАЛФ, ПАМФ входят в состав аминотрансфераз и декарбоксилаз
КоА входит в состав ферментов ацилирования
Металлопрорфирины — компоненты цитохромов (Fe в цитохромах b, Cu в цитохромах а)
ТГФК участвует в переносе и оксидоредукции одноуглеводных радикалов
Липоевая кислота — окислительное декарбоксилирование
Карбоксибиотин — карбоксилирование
Тиаминдифосфат - окислительное декарбоксилирование, транскеталазные реакции
метил-В12 — метилирование
DA-В12 — изомеризация
в) Проферменты — функционально неактивные предшественники ферментов, подвергающиеся тем или иным преобразованиям (обычно расщеплению специфическими эндо- или экзопептидазами или гидролизу), в результате чего образуется каталитически активный продукт — фермент. Относятся к группе протеиназ. К ним относятся пепсиноген, активной формой которого является пепсин, трипсиноген — трипсин, химотрипсиноген — химотрипсин, прокарбоксилепептидазы — карбоксипептидазы (ферменты поджелудочной железы) и др. К зимогенам относятся ферменты свёртывания крови(факторы свёртывания крови), компоненты и факторы системы комплемента.
г) Изоферменты — множественные молекулярные формы одного и того же фермента. Катализируют одну и ту же реакцию, но отличаются по их физико-химическим (молекулярной массой, подвижностью при электрофорезе и тд) и каталитическим (разным сродством фермента с субстратом) свойствам. Разные изоферменты могут располагаться в разных органах и тканях.
Одним из самых ярких представителей является лактатдегидрогеназа (ЛДГ), катализирующая превращение пирувата в лактат. Есть 5 изоферментов ЛДГ. Их колличество в крови имеет диагностическое значение. Так ЛДГ1 может указывать на инфаркт миокарда, а ЛДГ5 на гепатит.
д) Мультиферментные комплексы катализируют последовательности спряженных биохимических реакций. Эти комплексы состоят из нескольких физически ассоциированных ферментов, каждый из которых катализирует определенную реакцию. Например, пируватдегидрогеназный комплекс.
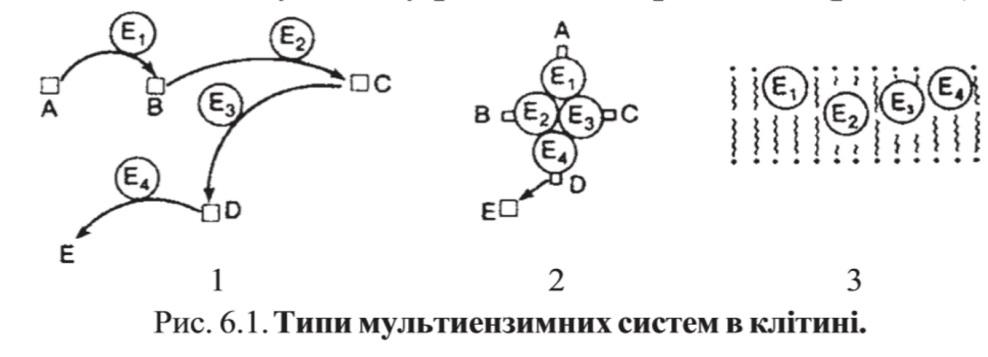
Различают:
-
Растворимые мультиферментные системы, в которых отсутствует постоянная ассоциация между ферментами
-
Системы в которых отдельные ферменты соединены между собой, образуя комплексы, которые облегчают передачу субстратов между отдельными ферментами
-
Мембранно-связанные системы, в которых отдельные ферменты ассоциированы с липидным бислоем субклеточных органелл.
2. Классификация ( номенклатура) ферментов
А) принцип классификации
В) краткая характеристика основных классов ферментов, примеры
Классификация ферментов. В настоящее время известно более 2000 ферментов. Все ферменты разделены на шесть классов, каждый из которых имеет строго определенный номер.
-
Оксидоредуктазы катализируют окислительно-восстановительные процессы.
-
Трансферазы катализируют реакции переноса функциональных групп и молекулярных остатков с одной молекулы на другую.
-
Гидролазы катализируют реакции гидролиза.
-
Лиазы катализируют реакции отщепления (кроме атомов водорода) с образованием двойной связи либо присоединения по двойной связи, а также негидролитический распад органических соединений либо синтез без участия макроэргических веществ.
-
Изомеразы катализируют процессы изменения геометрической или пространственной конфигурации молекул.
-
Лигазы катализируют реакции синтеза, сопровождающиеся гидролизом богатой энергией связи (как правило, АТФ).
Классы ферментов делятся на подклассы, а подклассы, в свою очередь, на подподклассы. Подкласс уточняет действие фермента, так как указывает в общих чертах на природу химической группы субстрата. Подподкласс еще более конкретизирует действие фермента, уточняя природу атакуемой связи субстрата или природу акцептора, который участвует в реакции.
Система классификации предусматривает для каждого фермента специальный шифр, состоящий из четырех кодовых чисел, разделенных точками. Первая цифра в шифре обозначает номер класса, вторая - номер подкласса, третья - подподкласса и четвертая - порядковый номер в данном подподклассе. Так, лактатдегидрогеназа имеет шифр КФ 1.1.1.27, т.е. относится к первому классу, первому подклассу, первому подподклассу и занимает 27-е место в перечне ферментов упомянутого подподкласса.
Приведем конкретные примеры биохимических процессов, катализируемых ферментами, относящимися к определенному классу и подклассу.
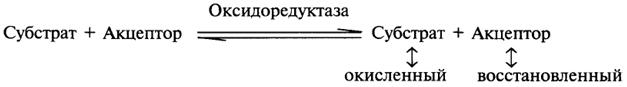
1. Оксидоредуктазы. Общая схема процессов, катализируемых оксидоредуктазами, может быть выражена следующим образом:
55
Наиболее часто мы будем встречать оксидоредуктазы подкласса оксидаз и дегидрогеназ, поэтому рассмотрим их подробнее.
Оксидазы - это оксидоредуктазы, которые переносят атомы водорода или электроны непосредственно на атомы кислорода либо внедряют в молекулу субстрата атом кислорода:
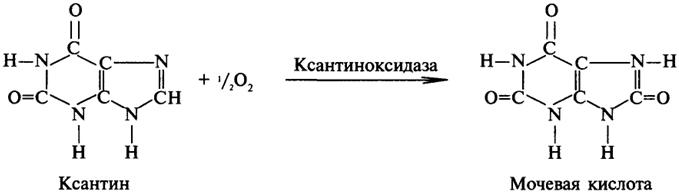
Дегидрогеназы - это оксидоредуктазы, катализирующие процесс отщепления атомов водорода.
Все дегидрогеназы являются холоферментами, коферментами которых служат следующие соединения: никотинамидаденинди-нуклеотид (НАД), никотинамидадениндинуклеотид (НАДФ), флавинмононуклеотид (ФМН), флавинадениндинуклеотид (ФАД), хиноны.
Наиболее распространены в природе дегидрогеназы, содержащие в качестве кофермента НАД:
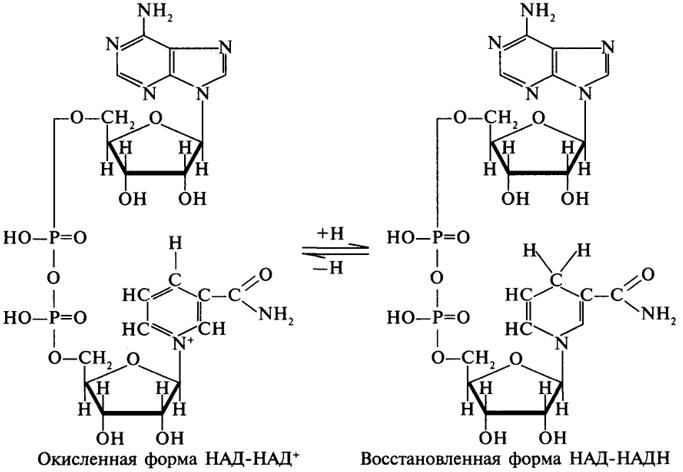
Как видно из схемы, присоединение снятого с субстрата атома водорода происходит по ядру никотинамида. Механизм действия НАДФ такой же, как и НАД. НАД- и НАДФ-зависимые дегидрогеназы способны отщеплять атомы водорода от субстратов (спиртов, альдегидов,гидроксикислот, аминов и др.) в виде гидрид-ионов (Н-) и протонов (Н+), окисляя таким образом указанные соединения.
Примером процесса, катализируемого НАД-зависимой дегидрогеназой, может служить окисление молочной кислоты (лактата) до пировиноградной кислоты (пирувата):
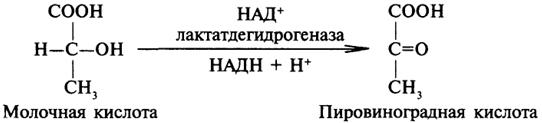
Коферменты ФМН и ФАД содержат в своем составе фосфорилированный витамин В2 (рибофлавинфосфат), который способен отщеплять от субстрата два атома водорода:
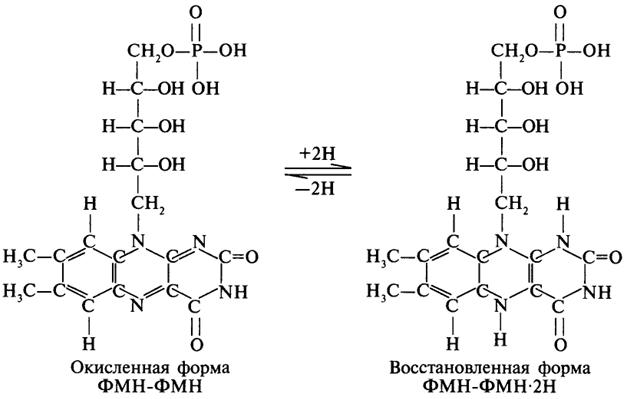
Пример реакции, катализируемой ФАД-зависимой дегидрогеназой:
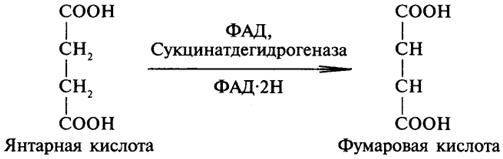
2. Трансферазы. Это один из самых многочисленных классов ферментов. В зависимости от характера переносимых групп выделяют фосфотрансферазы, аминотрансферазы, гликозилтрансферазы, ацилтрансферазы и др.
Фосфотрансферазы - это ферменты, катализирующие перенос остатка фосфорной кислоты. В результате действия фосфотрансфераз образуются фосфорные эфиры различных органических соединений, многие из которых обладают повышенной реакционной способностью и более легко вступают в последующие реакции. Следовательно, фосфорилирование органических соединений можно считать процессом их активации. Чаще всего донором фосфатных групп является молекула аденозинтрифосфорной кислоты (АТФ). Фосфотрансферазы, использующие в качестве донора фосфатной группы молекулу АТФ, называются киназами. К киназам относится, например, глицеролкиназа, ускоряющая перенос остатка фосфорной кислоты от молекулы АТФ к молекуле глицерина:
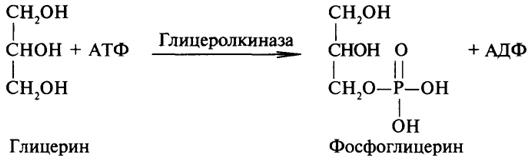
Аминотрансферазы ускоряют перенос аминогруппы. Аминотрансферазы - двухкомпонентные ферменты, коферментом которых служит пиридоксальфосфат (фосфорилированный витамин В6).
Гликозилтрансферазы ускоряют реакции переноса гликозильных остатков, обеспечивая, главным образом, реакции синтеза и распада олиго- и полисахаридов. Если гликозильный остаток переносится на молекулу фосфорной кислоты, то процесс называетсяфосфоролизом, а ферменты, обеспечивающие этот процесс, называются фосфорилазами. В качестве примера приведем схему фосфоролиза мальтозы:
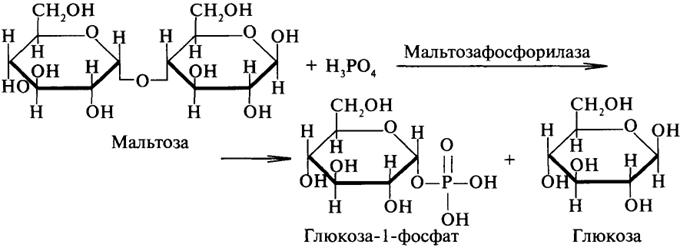
Донором гликозильных остатков в процессах синтеза олиго- и полисахаридов служат нуклеозиддифосфатсахара (НДФ-сахара), одним из представителей которых является уридиндифосфатглюкоза (УДФ-глюкоза):
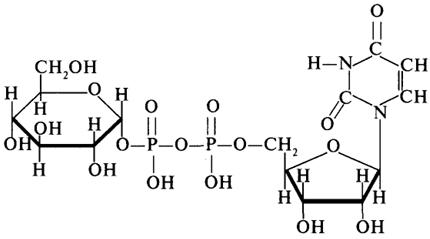 УДФ-глюкоза
УДФ-глюкоза
Ацилтрансферазы катализируют процессы переноса ацилов (радикалов карбоновых кислот) на спирты, амины, аминокислоты и другие соединения. Источником ацилов является ацил-КоА, который можно рассматривать в качестве кофактора в реакциях переноса ацильных групп. Примером реакции трансацилирования может служить реакция синтеза фосфатидной кислоты, в которой участвует фосфоглицерин и две молекулы ацил-КоА: