Материал: Взаимодействие лекарственных средств с мембранами клеток
Поддержание градиента концентраций ионов натрия и калия обеспечивается работой натрий-калиевого насоса. Он представляет собой мембранные белки, которые работают как ферменты аденозинтрифосфатазы (АТФазы). Задачей этих ферментов является расщепление АТФ на АДФ и неорганический фосфат. Процесс распада сопровождается выделением энергии, которая расходуется на транспорт ионов в сторону увеличения электрохимического потенциала. Расщепление АТФ стимулируется ионами натрия и калия и зависит от наличия магния. Активный транспорт возможен только за счет сопряжения транспорта какого-либо вещества с реакцией гидролиза АТФ.
Механизм сопряжения окончательно не выяснен. Вероятнее всего, энергия АТФ расходуется на изменение конформации транспортного белка, что изменяет его сродство (константу связывания) к тем или иным ионам. Транспорт всегда осуществляется в ту сторону, где сродство ниже. В клетке константа связывания переносчика с Na+ значительно выше, чем с K+. Поэтому ионы натрия в клетке связываются с белком и транспортируются во внеклеточную среду. По другую сторону мембраны конформация белка меняется таким образом, что константа связывания с Na+уменьшается, а с K+ - увеличивается. Структура ионсвязывающего участка белка в этом случае такова, что к нему могут присоединяться уже не три, а два иона калия, которые и переносятся в клетку.
Согласно современным представлениям, процесс активного транспорта Na+ и K+ происходит в следующие семь этапов.
. В присутствии Mg2+ на внутренней стороне мембраны образуется комплекс фермента АТФазы с АТФ.
. Присоединение АТФ изменяет конформацию фермента таким образом, что к образовавшемуся комплексу присоединяются три иона натрия.
. Происходит фосфорилирование Na+,K+ - АТФазы и отщепление АДФ.
. Ионсвязывающий центр фермента перемещается относительно толщины мембраны, в результате чего ион натрия оказывается на внешней стороне клетки.
. Снаружи клетки вследствие уменьшения сродства фермента к ионам натрия и повышения сродства к калию происходит обмен этими ионами.
. После отщепления фосфата фермент с присоединенными ионами калия снова изменяет положение относительно мембраны.
. Ионы калия и неорганический фосфат высвобождаются в цитоплазму, и фермент возвращается в исходное состояние.
Таким образом, энергии, выделяющейся при гидролизе одной молекулы АТФ достаточно, чтобы вынести из клетки три иона натрия и внести два иона калия. Na+,K+ - насос способствует не только повышению градиентов концентраций ионов, но и возрастанию градиента электрического потенциала, то есть является электрогенным, так как сумма вносимых зарядов неравна сумме выносимых. Межклеточная среда приобретает "более положительный" заряд по сравнению с клеткой за счет выноса одного "лишнего" положительного иона.
В мембранах саркоплазматического ретикулума мышечных клеток и цитоплазматических мембранах кардиомиоцитов существует Ca2+ - насос, работа которого во многом сходна с механизмом переноса ионов Na+,K+ - насосом. За один цикл, в процессе которого расходуется одна молекула АТФ, переносится два иона кальция.
Активный транспорт протонов может осуществляться как с помощью подвижных переносчиков, так и через мембранные каналы. Протонные каналы представляют собой интегральные белки, образующие внутреннюю пору, где содержатся участки, к которым могут присоединяться протоны. Энергия АТФ расходуется на изменение конформации белковых молекул, вследствие чего сродство одних участков связывания к протонам понижается, а других - увеличивается, что заставляет протон перескочить на другой участок канала, сродство которого к протону на данный момент выше. Путем таких перескоков с одного участка связывания на другой ион водорода пересекает мембрану.
Перенос Н+ против градиентов их концентраций осуществляется не только за счет энергии, выделяющейся при гидролизе АТФ, но и за счет энергии фотонов. Этот способ используется галофильными бактериями, которые на свету выкачивают протоны из клетки, а энергию создавшегося градиента концентраций используют для синтеза АТФ.
Вторично-активный транспорт
Транспорт, источником энергии которого служит не непосредственно АТФ или энергия окислительно-восстановительных реакций, а градиент концентраций других веществ, называется вторично-активным, или сопряженным транспортом. Существует три вида вторично-активного транспорта ионов (представлена на рис.3): унипорт, симпорт и антипорт.
. В случае унипорта за счет существования на мембране градиента электрического потенциала осуществляется однонаправленный транспорт заряженных частиц в сторону меньшего значения потенциала. Например, митохондрии в процессе своего функционирования активно выкачивают протоны из матрикса в цитоплазму, в результате чего их внутренняя область оказывается заряженной более отрицательно, чем внешняя. В нормальных условиях созданный градиент электрохимического потенциала используется для синтеза АТФ.
. По механизму симпорта осуществляется транспорт
противоположно заряженных ионов в одну сторону. При этом транспорт одного из
ионов осуществляется по градиенту концентраций, а транспорт второго - по
градиенту электрического потенциала, создаваемого транспортом первого иона.
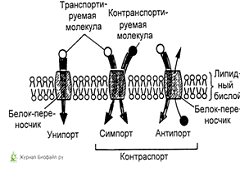
Рис. 3. Схема вторично-активного транспорта
веществ.
Одним из наиболее изученных случаев
вторично-активного транспорта незаряженных молекул является всасывание глюкозы
в стенках кишечника. Концентрация глюкозы в энтероцитах выше, чем в просвете
кишечника, поэтому пассивное её всасывание невозможно. Клетки кишечника активно
выкачивают натрий из энтероцитов в серозную область кишечника, в результате
чего концентрация Na+ в клетке снижается по сравнению с его концентрацией
снаружи. Благодаря этому становится возможным пассивный транспорт натрия из
просвета кишечника в энтероцит. Однако простая диффузия ионов через бислой мало
вероятна и натрий может пересечь мембрану только с помощью переносчика. При
этом переносчик связывается не только с натрием, но и с молекулой глюкозы.
Образовавшийся комплекс пассивно по градиенту концентраций ионов натрия и
электрического потенциала переносится внутрь клетки. Таким образом, транспорт
глюкозы осуществляется против градиента концентрации, но не за счет энергии
АТФ, а за счет существования градиента концентрации другого вещества, в данном
случае - ионов натрия. Подобные системы транспорта существуют и для многих
других веществ, например, углеводов и аминокислот, что очень важно, так как для
них отсутствуют специфические насосы.
. Механизм действия (фармакодинамика)
лекарственных средств
Механизм действия лекарств связан с их воздействием на физиологические, патофизиологические и биохимические процессы, происходящие в организме человека.
Фармакодинамика подавляющего большинства лекарственных средств является следствием их влияния на функцию биологически активных веществ (БАВ), участвующих либо в передаче нервного импульса, либо являющихся гормонами, витаминами, аминокислотами, метаболитами и пр.
Многие лекарственные вещества могут изменять активность рецепторов (компонентов цитоплазматической мембраны, внутриклеточных структур, в том Числе ферментов, структурных белков и пр.), существующих в организме для взаимодействия с БАВ. Для каждого эндогенного БАВ существуют специфические рецепторы. Лекарства же могут быть в разной степени похожими (по структуре, пространственному расположению частей молекулы) на эти эндогенные вещества. Их структурные аналоги или вещества очень похожего строения могут взаимодействовать с соответствующим рецептором, вызывать его возбуждение и имитировать эффект эндогенного вещества. Лекарственные средства, менее похожие по структуре на БАВ, тоже могут взаимодействовать с рецептором, слегка его возбуждать, но блокировать реакцию на эндогенное БАВ и его агонисты (неполный антагонист, антагонист с внутренней миметической активностью). Наконец, лекарственное вещество может взаимодействовать с рецептором и полностью блокировать его реакцию и на соответствующее БАВ, и на его агонисты.
Лекарства могут вступать в связь не с самим рецептором, находящимся, например, на поверхности клеточной мембраны, а с другими ее компонентами, окружающими рецептор. При этом могут произойти изменения в пространственном расположении компонентов мембраны так, что рецептор станет более или менее доступным для БАВ. В результате может возникнуть либо сенсибилизация (повышение чувствительности), либо десенситизация (снижение чувствительности) рецептора по отношению к БАВ. Поскольку в этом случае лекарство влияло не на рецепторы, а на другие участки мембраны, то этот эффект называют аллостерическим (от греч. alios - другой).
Взаимодействие лекарственных средств - аналогов БАВ - с рецепторами, расположенными на поверхности клеточных мембран или внутри клетки, приводит (как и при контакте с БАВ) к возникновению сигнала для начала активности клетки. Как уже сказано, для каждого БАВ существуют свои рецепторы, нередко разные (по 2-5 и более). Но реакции клеток на возникший сигнал обычно развиваются с помощью внутриклеточных посредников (мес-сенджеров) и могут оказаться одинаковыми независимо от качества БАВ или похожего на него вещества.
Рецептор, локализованный на поверхности клеточной мембраны, может быть компонентом (доменом) системы, в которую помимо самого рецептора входит каталитическая (ферментная, энзиматическая) субъединица (домен), находящаяся внутри клетки. Оба компонента (домены) связаны друг с другом короткой цепью из гидрофобных остатков аминокислот внутри самой клеточной мембраны.
Такими рецепторами являются, например, рецепторы для полипептидных гормонов, регулирующих рост, дифференцировку, развитие и иногда быстрые метаболические реакции. Эти рецепторы представляют собой протеинкиназы, катализирующие фосфорилирование протеинов-мишеней. Мишенями могут быть энзимы (в том числе другие киназы), регуляторные или структурные протеины. Фосфорилирование изменяет активность этих протеинов. В них чаще фосфорилируются остатки тирозина с помощью тирозинкиназ, например, в рецепторах для инсулина, эпидермального ростового фактора, некоторых лимфокинов. Фосфорилироваться могут остатки серина или треонина в протеинах, например при взаимодействии рецептора с трансформирующим ростовым Р-фактором.
Рецепторы могут быть связаны не с протеинкиназами, а с внутриклеточной гуанилатциклазой, образующей вторичный мессенджер - гуанозинмонофосфат (ГМФ), например, рецептор, взаимодействующий с предсердным натриуретическим пептидом.
Рецепторы для различных нейромедиаторов могут быть у медиаторозависимых (лигандозависимых) ионных каналов в плазматических мембранах клеток, по которым происходит передвижение ионов как внутрь, так и из клетки. Например, рецепторы для ацетилхолина (Н), гамма-аминомасляной кислоты: ГАМК-А, рецепторы для глутамата, аспартата, глицина, серотонина. Эти каналы являются частью сложной структуры, состоящей из нескольких компонентов, способных реагировать на различные агонисты и антагонисты названных БАВ.
Ионы кальция - внутриклеточные посредники 3-го порядка в активности многих БАВ и их аналогов, стимулирующих образование цАМФ или гидролиз ФИФ2 и либо увеличивающих поступление его в клетку, либо освобождающих его из внутриклеточных депо (эндо - или саркоплазматического ретикулума, митохондрий). Повышение внутриклеточной концентрации кальция активирует процессы освобождения нейромедиаторов, сокращения миокарда, скелетных и гладких мышц, секрецию эндо - и экзокринных желез, агрегацию тромбоцитов; Са++ повышает активность многих ферментов, участвующих в белковом, жировом и углеводном обмене, способствующих освобождению арахидоновой кислоты из фосфолипидов и пр. Посредником в активности Са++ является кальмодулин - белок, состоящий из 148 остатков аминокислот. Комплекс кальмодулина с Са++ стимулирует функцию многих ферментов: фосфодиэстераз циклических нуклеотидов (цАМФ и цГМФ), протеинканаз, зависящих от этих нуклеотидов, Са++-, М-Фазы цитоплазматической мембраны, фосфорилазы, киназы гликогенсинтетазы, фосфолипазы А2, сукциндегидрогеназы, N-метилтрансферазы и многих других. Под влиянием этого комплекса (кальмодулина с Са +) могут одновременно увеличиваться процессы образования цАМФ и распада цГМФ. Кальмодулин участвует в регуляции деления клеток (стимулируя синтез ДНК, вступление клетки в фазу митоза), в сократительной функции миокарда, склелетных мышц, миометрия.
Кроме кальциевых каналов, открывающихся под влиянием различных медиаторов и гормонов (стимулирующих образование цАМФ), существует по крайней мере три типа "медленных" кальциевых каналов, открывающихся под влиянием деполяризации клеточной мембраны (потенциал - или вольтажзависимые каналы). В настоящее время существует большая группа лекарственных веществ (блокаторы кальциевых каналов), блокирующих эти потенциалзависимые каналы, препятствующих поступлению Са++ внутрь клетки и этим ограничивающих его чрезмерную активнодть. Некоторые лекарства могут тормозить кальмодулин.
В фармакодинамике ряда лекарственных средств
имеет значение их способность взаимодействовать (вместо БАВ) с ферментами
(холинэстеразами, моно-аминоксидазами, редуктазой фолиевой кислоты, кининазами,
ангиотензин-конвертирующим ферментом, плазмином, калликреином, синтетазой
оксида азота и др.), тормозить их активность и этим изменять зависимые от них
биохимические процессы.
Заключение
Активным средством в руках врача, с помощью которого он может влиять на течение того или иного заболевания, является лекарственный препарат.
Лекарственное средство в руках знающего врача приносит огромную пользу людям. Незнание лекарственных средств, неумение пользоваться ими, низкие морально-этические требования к себе могут привести к непоправимым последствиям для больного человека.
Нередко перед врачом стоит сложная задача -
выбрать из большого арсенала лекарственных средств не только самое эффективное,
но и наименее токсичное, а также уменьшить риск появления побочного действия.
Это в значительной мере обусловлено тем, что при различных условиях одно и то
же вещество может оказаться лекарством или ядом. Так, стрихнин, морфин,
фосфакол и другие ядовитые и сильнодействующие лекарственные вещества в
сравнительно небольших, так называемых терапевтических дозах оказывают лечебный
эффект. С увеличением доз этих ЛС выше допустимых они могут проявлять
токсическое действие, нередко приводящее к тяжелым последствиям. Иногда обычные
дозы ЛС вместо желаемого действия могут оказать отрицательное влияние на
организм, что связывают с индивидуальной чувствительностью больных к этому ЛС.
Отсюда вытекает необходимость знания особенностей фармакодинамики и
фармакокинетики лекарственных средств в повседневной деятельности провизора.
Список использованных источников
1. http://internet-apteka.su/dt8/doc/mehanizm-deystviya-farmakodinamika-sredstv
. Журнал Биофайл.ру.
. Биологические мембраны, под ред. Д.С. Парсонса, пер. с англ., М., 1978
. Болдырев А.А. Введение в биохимию мембран, М., 1986, библиогр.
. Конев С.В. и Мажуль В.М. Межклеточные контакты. Минск, 1977
. Кульберг А.Я. Рецепторы клеточных мембран, М., 1987, библиогр.
. Маленков А.Г. и Чуич Г.А. Межклеточные контакты и реакции ткани, М., 1979
. Сим Э. Биохимия мембран, пер. с англ., М., 1985, библиогр.
.
Финеан Дж., Колмэн Р. и Митчелл Р. Мембраны и их функции в клетке, пер. с
англ., М., 1977, библиогр.