Материал: высокополярные нефти
СПБГУАП группа 4736
Образование кристаллических неорганических агрегатов (солей) как процесс состоит из ряда этапов:
1)пересыщение раствора солями;
2)зародышеобразование;
3)рост кристаллов;
4)перекристаллизация.
Причем эти этапы могут протекать либо поочередно один за другим, либо одновременно.
Пересыщение раствора солями относительно какого-либо комплекта связано с увеличением концентрации последнего выше равновесной (растворимости).
Условием возникновения этого процесса на месторождениях является наличие минерализованной попутно добываемой воды и причин,
вызывающих ее пересыщение. В водах многих нефтяных месторождений растворено большое количество неорганических солей.
Главным условием возникновения солеотложений является несовместимость закачиваемых и пластовых вод. Например, на упомянутых местоорждений Узень и Жетыбай закачиваемая морская вода и пластовые воды химически не совместимы. При их смешивании образуются пересыщенные растворы. Не совместимы в химическом отношении и пресные воды с пластовыми в условиях месторождений Западной Сибири:
при внедрении впервые законтурного заводнения на Треозерном месторождении с использованием воды из р. Конды с началом отложениями солей в оборудовании скважин (см. выше). Те же проблемы возникли и по месторождениям Широтного Приобья. Именно несовместимость закачиваемых с пластовыми водами - одна из главных причин солеотложений на большинстве нефтяных месторождений.
Однако в практике образование осадков солей часто наблюдается до начала заводнения пластов. Отсюда помимо названной причины образования пересыщенных растворов существуют и другие. Исследователи выявили эти причины.
16
СПБГУАП группа 4736
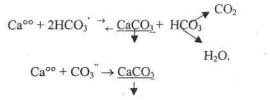
/. Изменение термодинамических условий Образование карбонатов при
этом протекает по схеме:
(6.9)
Впластовых водах |НС03| »|С03| и образование СаС02 происходит в основном по схеме (6.9).
Вотличие от большинства неорганических солей кальций лучше растворяется в воде с уменьшением температуры. Если при 1000С его рав-
новесная концентрация составляет 14 мГ/л, то при 00С - 85 мГ/л. Однако с уменьшением давления и температуры из раствора выпадает осадок Са-СОз,
ибо на направление реакции по схеме (6.9) в значительно большей степени,
чем температура, влияет парциальное давление углекислого газа. Влияние
парциального давления С02 |
на растворимость СаС03 в воде отображается |
|||
соотношениями: |
|
|
|
|
Парциальное давление |
0,0001 |
0,01 |
0,1 |
1,0 |
С02, МПа |
|
|
|
|
Растворимость N, мг/л |
60 |
400 |
920 |
2125 |
Изменение Р и Т способно привести к пересыщению раствора отно-
сительно сульфата кальция и бария (табл. 6.4).
Таблица 6.4. Влияние температуры на растворимость сульфатов кальция и бария в воде
Сульфат- |
|
|
Растворимость N (в мг/л) при tв0 С |
|
|
|||||
ные соли |
0 |
20 |
25 |
40 |
50 |
80 |
92 |
|
95 |
100 |
Ангидрит |
- |
3000 |
- |
2200 |
- |
1080 |
- |
|
- |
660 |
|
|
|
|
|
|
|
|
|
|
|
Гипс |
1759 |
2036 |
2080 |
2097 |
- |
l966 |
- |
|
- |
1619 |
Барит |
- |
- |
2,8 |
- |
3,2 |
3,2 |
3,9 |
|
3,6 |
– |
Максимальная растворимость гипса наблюдается при температуре
40°С. При дальнейшем повышении температуры он менее растворим, а
уменьшение растворимости ангидрита при этом более интенсивное. Поэтому в скважинах и пластах с температурой выше 400С в отложениях должно
17
СПБГУАП группа 4736
наблюдаться преобладание ангидрита. На растворимость барита температура влияет незначительно.
При падении давления от 50 МПа до 10 МПа при t = 1000С раство-
римость сульфата кальция уменьшается на 0,04% по массе и составляет
0,09%. Влияние давления на растворимость сульфата кальция в насыщенном
растворе при 200С приведено ниже: |
|
|
|
|
Растворимость N, мг/л |
2,08 |
2,12 |
2,33 |
2,46 |
Давление, МПа |
0,1 |
4,1 |
10,1 |
16,1 |
Из чего следует, что оно невелико. Однако анализ лабораторных и
промысловых данных показал, что уменьшение давления может привести к выпадению сульфатов бария и кальция из растворов.
Понижение давления вызывает испарение части воды в газовую фазу,
что также способствует пересыщению водно-солевых систем.
2. Изменение химического состава пластовых вод в процессе
разработки месторождений
Смешение закачиваемой и пластовой вод даже при условии их хи-
мической совместимости приводит зачастую к формированию попутно до-
бываемой воды совершенно нового состава по сравнению с пластовой. А это,
в свою очередь, способствует изменению растворимости отдельных компонентов. Например, в табл. 6.5 показано влияние содержания NaCl на
растворимость CaCО3, CaSО4 и BaSО4 в дистиллированной воде. Из чего следует, что при высокой концентрации NaCl в растворе заметно повышается
растворимость СаСО3 и CaSО4 . Отмечаются максимумы растворимости СаСОз при содержании NaCl в количестве (20 г/л, а гипса –150 г/л).
Таблица 6.5. Влияние содержания NaCl на растворимость других солей в воде
|
|
|
|
Содержание NaCl, г/л |
|
|
|
|||||
|
0 |
40 |
50 |
100 | 120 |
| 150 | 200 |
250 |
300 |
350 |
||||
Соли |
|
|
Растворимость солей N, мг/л |
|
|
|||||||
СаСОз |
- |
- |
1632 |
1736 |
1750 |
1720 |
1576 |
1416 |
1256 |
1056 |
||
(t=20°C) |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||
BaS04 |
2,8 |
18,4 |
- |
26,8 |
28,4 |
|
- |
- |
- |
- |
– |
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
18
СПБГУАП группа 4736
(t=25°C) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CaS04 |
3200 |
- |
6000 |
7000 |
- |
7280 |
7200 |
- |
- |
– |
|
(t=20°C) |
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
В большей степени (в 10 раз) повышается при этом растворимость |
|||||||||||
BaSО4. |
|
|
|
|
|
|
|
|
|
|
|
Пластовые воды месторождений, разработка которых осложнена солеотложениями, являются водами хлоркальциевого типа. В таких водах растворимость гипса невелика. Если при отсутствии в воде СаС12 равно-
весная концентрация гипса 2080 мг/л, то при содержании в растворе 367, 85
г/л СаС12 |
она уменьшается до 32 мг/л. |
|
|
|
||||
Влияние содержания G СаС12 |
на растворимость N сульфата кальция |
|||||||
приведено ниже: |
|
|
|
|
|
|
||
G, г/л |
367,85 280,3 |
192,9 97,02 51,53 32,05 25,07 |
11,97 |
7,49 |
0 |
|||
N, мг/л |
32 |
203 |
465 |
841 |
1016 1080 1096 |
1181 |
1244 |
2080 |
Таким |
образом |
в |
двухкомпонетных системах |
различные |
соли |
|||
по-разному влияют на равновесную концентрацию основных компонентов неорганических осадков. Реальные пластовые, закачиваемые и попутно добываемые воды - многокомпонентные водно-солевые системы.
Зависимость растворимости ангидрита и гипса от суммарной минерализации и от массовой доли отдельных компонентов носит сложный характер и изменяется в широких пределах. При увеличении доли Сl до 4% для большинства значений температур растворимость сульфата кальция возрастает. При дальнейшем повышении содержания ионов Сl в системе уменьшается равновесная концентрация сульфата кальция. То есть изменение минерализации попутно добываемой воды может привести к ее перенасыщению.
3.Поступление на забой скважины вод различных горизонтов
Примером проявления данной причины в образовании солевых отложений может служить Майкопское газоконденсатное месторождение. При эксплуатации скважин за счет некачественного разобщения горизонтов
(цементажа) и значительной разницы в давлениях в I ,II и III горизонтах воды
19
СПБГУАП группа 4736
перетекали из одного горизонта в другой. Смешение щелочных вод I и II
горизонтов, содержащих большое количество СаС12 к MgCl2, с водами III
горизонта приводило к образованию солевых осадков из карбонатов кальция
имагния.
4.Тепловые методы разработки
Исследованиями ВНИИ было установлено, что при закачке воды в глубоко залегающие пласты возможно частичное (или полное) растворение воды в нефти. В качестве аналога нефти использовался н – гексадекан (табл.
6.6).
Н – гексадекан имеет высокую температуру кипения (286,80С) и
большой молекулярный вес (226,4), поэтому он принят за аналог нефти.
Существуют и другие факторы, способствующие возникновению процесса солеотложений: выщелачивание солей, содержащихся в пласте,
процессы обогащения закачиваемых вод солями при их контактировании с погребенными водами, повышение растворимости воды в нефти с увеличением температуры (то есть углеводороды будут играть роль высаливателей).
20