Материал: Водородная энергетика: задачи, проблемы и сферы применения
3.2 Способы получения водорода
Получение водорода весьма трудоемкий процесс. На данный момент известно несколько способов получения водорода. Среди них:
1. химический;
2. электролиз;
3. термохимический.
Данные способы относятся к традиционным методам. Но каждый способ сегодня является экономически и экологически нецелесообразным, по причине необходимости затраты природных ископаемых.
Рассмотрим один из наиболее распространенных способов получения водорода - из воды путем электролиза.
Под электролизом понимается некоторый электронный проводник, погруженный в ионный проводник (раствор электролита, расплав) или соприкасающийся с ним. На межфазной границе раздела электрод - раствор протекают электродные процессы, в результате которых между электродом и раствором устанавливается разность потенциалов - электродный потенциал, значение которого зависит от природы, протекающей на поверхности электрода электрохимической реакции. В данном случае можно измерить лишь разность электродных потенциалов нескольких электродов.
Таким образом, в обратимой реакции при электролизе воды наряду с затратами электроэнергии принципиально возможно непосредственное преобразование теплоты, подводимой к ячейке, в химическую энергию топливно-окислительной композиции (водорода и кислорода).
Многочисленные прогнозируемые оценки показывают, что в соответствии с ростом цен на природное жидкое и газообразное топливо в перспективе, а также совершенствование существующих и развитие новых типов электролизеров в будущем может оказаться дешевле, чем получение его из природного топлива.
3.3 Расчет водородной энергетики
Молекула водорода состоит из двух атомов водорода. При образовании молекулы два электрона, которые до этого времени принадлежали к двум различным атомам водорода, начинают вращаться в плоскости, перпендикулярной к оси, соединяющей ядра.
При образовании ковалентной химической связи за счет перехода электронов от одного атома к внешней оболочке другого происходит выделение энергии. Данное выделение энергии можно объяснить сродством атомов водорода по отношению к электрону. Это соответствует формуле 0,72 эВ ·2, где 0,72 эВ есть энергия сродства одного атома водорода по отношению к одному электрону.
Одновременно при образовании новой связи и электроны, и ядра приближаются друг к другу, что приводит к потере энергии. Согласно опытным данным, межъядерное расстояние в молекуле водорода составляет 0.74А. Соответственно, потеря энергии, происходящая за счет взаимного отталкивания ядер, составляет около 9 эВ.
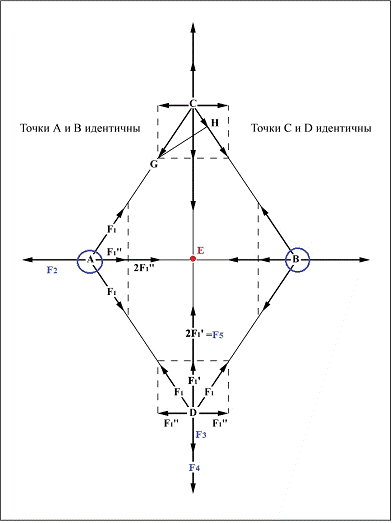
Рис. 3.1 Силы притяжения и отталкивания в молекуле АВ
Рассчитаем энергию молекулы водорода так, как мы это делали для атома: энергия молекулы также приравнивается к сумме ее электронных энергий. Согласно этой модели (рис. 3.1), электроны вращаются вокруг точки Е в плоскости, перпендикулярной к оси, соединяющей ядра А и В. Силы притяжения электронов к ядрам направлены перпендикулярно к плоскости круга, в котором электроны вращаются и где они взаимно уравновешивают друг друга. Их взаимное действие, таким образом, равно нулю. Задача о вычислении энергии молекулы водорода сводится к вопросу об определении энергии гелиеподобного атома (атома с двумя электронами).
Для этого расчета необходимо знать ядерный заряд, так как энергия гелиеподобного атома определяется по формуле:
He =
13,6· (Z-0.25) 2·2 (3.0)
Следует отметить, что в точке E не существует реального положительного заряда. Электроны притягиваются к этой точке за счет сил F11, которые являются проекциями сил F1 на оси DC.
Данные силы идентичны тем силам, которые удерживают электроны на
орбите гелиеподобного атома с зарядом Z. Эти силы предотвращают разрыв
электронов из-за взаимного отталкивания силы F3 и центробежных сил,
то есть
F11 = F3+F4,
где F3 - силы межэлектронного отталкивания; F4 - центробежные силы.
В данном случае используется система, предложенная Бором для расчета атомарных систем. Энергия системы и линейные параметры в этих расчетах определяются посредством сравнения зарядов и расстояний (радиусов) с энергией электрона и радиусом орбиты в атоме водорода. Заряд электрона принят за единицу заряда, а радиус атома водорода (0,529 А) выступает в качестве единицы длины. Единичная сила в данном случае есть сила взаимодействия протона с электроном в атоме водорода, расстояние между которыми составляет 0,529 А.
Таким образом, ядерный заряд может иметь сходство с зарядом Ze, поскольку заряд протона равен заряду электрона. С учетом всех принятых обозначений, определим эффективный заряд Z в точке E молекулы водорода (рис. 3.1).
Здесь электроны расположены в точках C и D, а ядра (протоны) - в точках А и В. Точка Е находится в центре, вокруг которого вращаются электроны в плоскости, перпендикулярной по отношению к нему, как это изображено на рис. 3.1 Силы притяжения электронов к ядрам обозначены на рисунке как F1, силы отталкивания между ядрами - как F2, силы отталкивания между электронами - как F3.
Проекции F1 на оси CD обозначены как F11, проекции F1 на оси AB - F111.
Свойства молекул водорода не изменяются с течением времени, поэтому расстояния между электронами и ядрами являются постоянными. То есть, силы F1, притягивающие ядро F111, есть равные силы межъядерного отталкивания. Силы F111, действующие на электроны, также равны по той же причине. Эти силы действуют на электроны C и D в противоположных направлениях и являются равными по величине, т.е. их результирующая сила равна нулю. То же самое относится к силам 2F11 и F3+F4. Теперь обозначим радиус орбиты электрона как а (EC = а), расстояние между ядрами как 2b (AB = 2, b), расстояние между электроном и ядром как с (AC = с), а половину силы, притягивающей электрон к точке Е, как F5. Таким образом, мы получаем:
5 =
F11+F11 = 2F11
С другой стороны, поскольку силы, действующие на каждый электрон, равны силам в водородоподобных атомах с радиусом а и зарядом Ze, получаем:
5 =
Ze2/a2 (3.1)
Если подставить значение F5 в (3.1), мы получаем:
e2/a2
= 2F11
Здесь для того, чтобы определить Z и энергию молекулы водорода, надо решить данное уравнение. F11, как уже отмечалось, является проекцией F1 на ось CD. Согласно тригонометрии:
11 = F1xcos∠ECB (3.2)
Тогда cos∠ECB =
EC/CB, или, в соответствии с принятыми обозначениями, EC = a и BC = c,
следовательно, cos∠ECB =
a/c. Согласно теореме Пифагора и принятым обозначениям, EB = b:
cos∠ECB = a/ (a2+b2) 0,5
= a (a2+b2) - 0,5
Подставляя значение cos∠ECB в уравнение 3.2, получаем:
11 = F1xa
(a2+b2) - 0,5
В соответствии с принятыми обозначениями, BC = c
1 =
e2/c2
В нашем случае положительный заряд в точке B равен 1. Подставляя
значение F1 из этого уравнения, получаем:
F11 = e2/c2xa
(a2+b2) - 0,5; c2 = a2+b2
Таким образом, мы получаем теорему Пифагора:
F11 = e2a
(a2+b2) - 0,5/ (a2+b2) =
e2a (a2+b2) - 1,5
Подставляя значение F11, получаем:
Ze2/a2 = 2e2a (a2+b2) - 1,5
Умножая обе части этого уравнения на a2 и деля их на e2, получаем:
= 2a3 (a2+b2) - 1,5
Теперь делим и умножаем значение в скобках на а:
= 2a3a-3 (1+b2/a2) - 1,5
= 2 [1+ (b/a) 2] - 1,5 (3.3)
То есть, для того, чтобы определить значение b, мы должны определить значение b/a, для которого мы будем использовать следующее уравнение.
В соответствии с рис.3.1, 2F111 = F2 или, согласно тригонометрии F111 = F1cos∠CBE, поскольку в соответствии с законами тригонометрии и теоремой Пифагора, cos∠CBE = b/ (a2+b2) 1,5
Тогда, используя закон Кулона, получим:
F111 = [e2/
(a2+b2)] ·b/ (a2+b2) 0.5
= e2b/ (a2+b2) 1,5
С другой стороны, согласно модели и законом Кулона:
F111= e2/4b2, то есть,
2e2b/ (a2+b2) 1,5 = e2/4b2
Теперь умножим обе части уравнения на 4 (a2+b2)
(a2+b2) 0,5/be2 и мы получаем:
e24 (a2+b2)
(a2+b2) 0,5/4b2be2 = 2e2b4
(a2+b2) (a2+b2) / (a2+b2)
0,5 (a2+b2) 0,5be2
Квадрат обеих частей уравнения дает нам:
2 (a2+b2) (a2+b2)
/b6 = 64 или (a2+b2) 3/b6
= 64
По извлечении кубического корня в обеих частях уравнения, имеем:
(a2+b2) /b2 =
4 или a2/b2+1 = 4; a2/b2
= 3; a/b = 30,5
Подставляя значения b/a = 1/30,5 в уравнение 3.3, получаем:
= 2· (1+1/30,5) - 1,5 = 2· (1,333) - 1,5 =
1,299
Подставляя значение Z в уравнении 3.0, определяем значение энергии молекулы водорода (EH2), которое составляет:
H2=1,317
103 2 (1,299-0,25) 2 = 5,526 кДж/моль
В ходе расчетов установлено, что энергия молекулы водорода составляет 5,526 кДж/моль.
Таким образом, мы имеем достаточно высокий энергетический
потенциал водородной среды для производства электроэнергии.
Выводы
В процессе работы рассмотрены основные виды классических
источников энергии и их влияние на окружающую среду. Приведено определение
альтернативных источников энергии, а также их виды, преимущества и задачи. В
курсовом проекте особое внимание уделено водородной энергетике. Указано
описание водорода, как химического элемента и носителя энергии. Рассмотрены
способы получения водорода из различных сред. Проведены энергетические расчеты
молекул водорода.
Литература
1. http://nuclphys. sinp. msu.ru/ecology/ecol/ecol05. htm.
2. Шпильрайн Э.Э. Введение в водородную энергетику. Под ред. Легасова В.А. - М.: Энергоатомиздат, 1984. - 264 с., ил.
. Доклад Введение в водородную энергетику и топливные элементы. Филиал "ЦНИИ СЭТ" ФГУП "Крыловский государственный научный центр”.
. http://itchem.ru/energiya_molekuly_vodoroda.