Материал: Виробництво хлору, каустичної соди та водню
Виробництво хлору, каустичної соди та водню
МІНІСТЕРСТВО ОСВІТИ І НАУКИ УКРАЇНИ
НАЦІОНАЛЬНИЙ УНІВЕРСИТЕТ “ЛЬВІВСЬКА ПОЛІТЕХНІКА”
Кафедра хімії і технології неорганічних речовин
Курсовий проект на тему:
«Виробництво
хлору, каустичної соди та водню»
Виконала студентка:
Панасюк А.М
групи ТНРс-11
Керівник:
доц. Слюзар
А.В
Львів-2014
Зміст
Вступ
. Загальна характеристика виробництва хлору, каустичної соди та водню
.1 Виробництво хлору, каустичної соди та водню в Україні та країнах СНД
.2 Характеристика та вимоги до якості продукції
.3 Характеристика сировини, матеріалів та напівпродуктів
.4 Фізико-хімічні основи технологічного процесу виробництва каустичної соди
. Технологія виробництва хлору, каустичної соди та водню
.1. Основи електролізу водних розчинів хлориду натрію діафрагмовим методом
.2. Технологічна схема виробництва
.2.1. Діафрагмові електролізери
.2.2 Електроліз водних розчинів хлориду натрію бездіафрагмовий з ртутним катодом
.2.3 Електроліз водних розчинів хлориду натрію мембранним методом з твердим катодом
.3. Проблемні стадії виробництва
.4.Порівняльна характеристика технологічних схем виробництва
Висновки
Список використаної літератури
Вступ
Перед нами стоїть завдання - електролізом водного розчину хлориду натрію одержати три цільових продукти: хлор, гідроксид натрію і водень.
Сировиною для електролітичного виробництва лугу і хлору є водні розчини NаСl. Вапняне молоко, використовуване содових заводах, на хлорних заводах замінюють розчином каустичної соди ( католіт ), тому метод очищення носить назву содово - каустичний.
Електроліз - розклад речовин
(наприклад, води <#"821086.files/image001.gif"> і починає
проходити процес виділення хлору c низькою перенапругою (крива 2). Проводимо
еквіпотенціальну лінію при робочому потенціалі анода (Еа=1,42
В) до перетинання з поляризаційними кривими і знаходимо силу струму (![]() , що
витрачається на кожен процес. У даному прикладі
, що
витрачається на кожен процес. У даному прикладі ![]() = 45...60 А×м-2, а
= 45...60 А×м-2, а ![]() =1450 А×м-2.
Звідси
=1450 А×м-2.
Звідси ![]() і, отже,
вихід за струмом хлору складає 96…97 %.
і, отже,
вихід за струмом хлору складає 96…97 %.
Таким чином, завдяки застосуванню анодного матеріалу з високою перенапругою виділення кисню і низькою перенапругою хлору, основним процесом на аноді є утворення хлору.
Аналізуючи хід парціальних
поляризаційних кривих (рис. 1.1), можна зробити висновок про те, що чим вище
робоча густина струму, тим більшого виходу за струмом хлору слід очікувати.
Тому електроліз рекомендується вести за густиною струму: діафрагмовим методом -
1500...2500 А×м-2,
мембранним - 2000...4000 А×м-2, із ртутним катодом -
6000...15000 А×м-2.
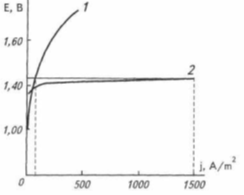
Рис.1.1. Парціальні поляризаційні
криві виділення кисню (1) і хлору (2) на ОРТА
. Для зниження напруги на електролізері і питомої витрати електроенергії електроліз доцільно проводити при підвищених температурах - 358...369 К. Такі технологічні параметри диктуються кінетикою електродних процесів і витратою електроенергії і можуть уточнюватися при конкретному методі електролізу.
. Надійний розділ анодних і катодних
продуктів. При електролізі водних розчинів хлоридів лужних металів в зоні
потенціалів негативніше лінії а рівноваги води з воднем, на твердому
металевому катоді буде проходити реакція:
Н2О + 2е = 2ОН- + Н2
з накопиченням лугу в католіті і виділенням водню.
Якщо анодні продукти (Cl2, рН < 4) не відокремити від катодних (NaOH ~ 100...140 г×дм-3), почнуть проходити побічні процеси 2, 4, 5, 12 і 18 з утворенням гіпохлориту, хлориту і хлорату натрію, і цільових продуктів не одержимо.
Для відділення анодного простору з кислим розчином від катодного, заповненого розчином лугу, застосовують катіонообмінні мембрани і пористі діафрагми. В залежності від виду роздільного елемента в промисловості застосовують три методи електролізу водних розчинів хлориду натрію:
· діафрагмовий з твердим катодом;
· мембранний з твердим катодом;
· бездіафрагмовий з ртутним катодом.
Розглянемо більш докладно кожний з них.
Кожен їх зазначених способів відрізняється реакціями, що протікають. У діафрагмовому способі на твердому катоді відбувається розряд іонів водню, що містить залишкові кількості NаСl. На аноді подається гарячий очищений розсіл і утворюється газоподібний хлор. Рух розсолу з анодного в катодний відбувається за рахунок різниць рівнів аноліта і католіта.
Катодний процес . При електролізі
водного розчину хлориду натрію на твердому, наприклад, залізному катоді,
виділяється водень і в католіті утворюється луг.
Н2О +2 е → Н2 +2 ОН
Різні іони розряджаються при різних значеннях потенціалу. Це властивість іонів і дозволяє використовувати електроліз для розділення сумішей речовин. Мінімальний потенціал електорода, необхідний для розряду даного іона при концентрації його в розчині, що дорівнює 1екв / л, називають нормальним електродним потенціалом і позначають через Е0. Для багатьох іонів значення Е0 відомі і наводяться у довідковій літературі.
У практичних умовах розряд іонів на електродах відбувається при більш високих значеннях потенціалу, ніж теоретичне. Різниця між значеннями дійсного та оборотного електродного потенціалу називається поляризацією, яка зростає із збільшенням щільності струму.
Лімітуючою стадією процесу електролізу може бути стадія розряду іонів - гальмування процесу за рахунок електрохімічної стадії ( виникає при протіканні струму), що призводить до появи перенапруги - поляризації. На поляризацію в цьому випадку впливає зміна умов ведення електролізу. Так, наприклад, для зменшення поляризації виділення водню залізний катод покривають нікелем або кобальтом ( каталізатором ), що знижує потенціал виділення водню.
Розряд іонів натрію на сталевому катоді не відбувається внаслідок високого від'ємного значення стандартного потенціалу реакції.
а + е → Nа, рівного - 2.714В
Крім основного процесу, що протікає
на аноді 2Сl → Сl2, в анодному просторі електролізера протікає ряд
побічних реакцій, що зменшують вихід по струму, наприклад:
ОН - - 4е → О2 + Н2О
Хлор, що виділяється на аноді,
частково розчиняється в електроліті, взаємодіючи з водою відповідно до
реакціями
Сl2 + Н2О ↔
НСlО + НСl, Сl2 + ОН- ↔ НСlО + Сl -
На окислення іонів СlО - на аноді до
СlО3 - витрачається значна частка струму, отже, зазначені процеси є
небажаними. Таким чином, вихід за струмом продукту, що позначається зазвичай А,
залежатиме від ретельності поділу катодних і анодних продуктів. Крім того,
вихід за струмом залежить від концентрації їдкого натру в католіті, від
розчинності хлору в аноліті, а остання пов'язана з концентрацією NаСl: чим вище
концентрація NаСl в аноліті, тим нижче розчинність хлору. Розчинність хлору у
водних розчинах концентрацією NаСl знижується також з підвищенням температури.
Цим і пояснюється прагнення направити на електроліз практично насичений водний
розчин концентрацією NаСl і вести процес при температурі 85- 900С . Вихід хлору
і луги по струму в цих умовах складає 92-96 %.
2. Технологія виробництва хлору, каустичної соди та водню
2.1
Основи ектролізу водних розчинів хлориду натрію діафрагмовим методом
Вперше діафрагмовий електроліз з твердим катодом був здійснений з непроточним електролітом. У діафрагмовий електролізер заливають визначений об’єм розчину хлориду натрію з концентрацією 310 г×дм-3. Аноліт і католіт знаходяться на одному рівні. При проходженні струму, на катоді розряджається вода (b) з накопиченням у католіті NaOH. На аноді виділяється хлор за реакцією:
-
- 2e = Cl2 (2.1.)
Іони ОН- під дією електричного поля рухаються до анода. Поки концентрація їх у католіті невелика, то участь ОН- іонів у переносі струму теж невелика, і тому на початку електролізу струм переноситься іонами Na+ і Cl-. По мірі накопичення в розчині NaOH усе більша частина струму переноситься іонами ОН-, що призводить до зменшення виходу за струмом Cl2 і NaOH. Практично в електролізерах з нерухомим електролітом (наприклад, системи Грисгейм - Електрон) працювали до концентрації 40...50 г*дм-3. Проте при цьому вихід за струмом падав до 50...65 %.
Цей факт підтверджується таким
теоретичним висновком. Припустимо, що через електролізер пройшов 1F електрики.
При цьому в католіті утвориться 1 моль NaOH , що буде брати участь у переносі
струму поряд з іонами Na+ і Cl-. Якщо х долей F
переноситься NaOH, тоді (1 - х) долей F переноситься NaCl. Відношення
кількості струму, що переносять NaOH і NaCl пропорційно питомій електричній
провідності
![]()
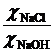
![]() (2.2)
(2.2)
Звідси
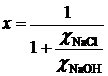 (2.3)
(2.3)
Якщо n - число
переносу іонів ОН-, то nх - кількість ОН-,
що беруть участь у переносі струму, потрапляють в анодний простір і беруть
участь у побічних процесах. Оскільки при проходженні 1 F електрики утвориться 1
моль NaOH, то вихід за струмом NaOH
ВСNaOH = 1-nx (2.4)
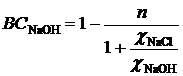 (2.5)
(2.5)
Відомо, що ![]() , тому
, тому
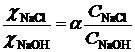 , (2.6)
, (2.6)
де a1 і
a2 -
ступінь дисоціації відповідно NaCl і NaОН; ![]() - молярна електрична провідність
відповідно хлориду і гідроксиду натрію при нескінченному розведенні.
- молярна електрична провідність
відповідно хлориду і гідроксиду натрію при нескінченному розведенні.
З урахуванням наведеного
співвідношення одержимо рівняння Ферстера:
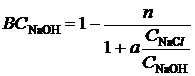 (2.7)
(2.7)![]()
з якого очевидно, що з підвищенням концентрації NaОН вихід за струмом падає.
Для підвищення виходів за
струмом хлору і гідроксиду натрію застосовують діафрагмовий електроліз водного
розчину хлориду натрію з протитечією. Підвищення виходів за струмом при
одночасному збільшенні концентрації лугу досягається створенням потоку
електроліту в порах діафрагми назустріч руху іонів OH-. Прохідність
електроліту від анода до катода створюється за рахунок різниці рівнів
електроліту h. Для цього в анодний простір безперервно подається розчин
NaCl c концентрацією 310±5г×дм-3, а католіт, що
містить NaOH 120...140 г×дм-3 і NaCl 180...200 г×дм-3,
безперервно виводиться з електролізера.
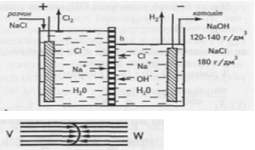
Рис.2.1.
Схема роботи діафрагмового електролізера з протитоком електроліту
На аноді проходить процес виділення хлору, а на катоді - процес з виділенням водню і гідрокcиду натрію.
У порах діафрагми (рис. 2.1.) іони
ОН- під дією електричного поля починають рухатися в напрямку до
анода зі швидкістю W. Проте рідина в порі рухається у бік катода зі
швидкістю V і зносить іони ОН- у катодний простір. Якщо V ³
W, то теоретично міграція іонів ОН- в
анодний простір буде дорівнювати нулю, а вихід за струмом лугу повинен бути
близький до 100% за умови, що усунута конвекція і дифузія. Якщо V < W,
то вихід за струмом менший 100%.
2.2
Технологічна схема виробництва
Технологічна схема виробництва гідроксидів натрію або калію, хлору і водню діафрагмовим методом включає стадії приготування і підготовки вихідних розчинів (I), електролізу (II), обробки продуктів електролізу і доведення їх до товарного вигляду відповідно до вимог споживача (III). Сюди відносяться стадія охолодження і сушіння хлору, а також стадія випарювання католіту (IV) і скраплення хлору. Принципова технологічна схема цього виробництва подана на рис. 2.2.
Вихідною сировиною для електролізу є концентрований розчин хлориду натрію. Розчин солі готують або розчиненням солі під землею, подаючи гарячу воду в спеціально пробурені свердловини, або розчиненням твердого хлориду натрію в наземних умовах на складах-солерозчинниках. На окремих підприємствах як сировину використовують природні розсоли. Сирий розсіл надходить у збірник 1. Він містить значну кількість зважених часток, а також шкідливих для електролізу домішок - солей кальцію, магнію, заліза і тому він надходить на очистку.
Сирий розсіл , що містить 310...315 кг×м-3 хлориду натрію через підігрівач 2 подається в освітлювач 10. Для очищення розсолу від домішок на хлорних заводах в основному застосовують содово-каустичний метод очистки, відповідно з яким для очистки від іонів Са2+ використовують содовий розчин, від іонів Mg2+ і заліза - гідроксид натрію, що надходить зі зворотним розсолом. Вміст NaOH в зворотному розсолі, отриманому розчиненням зворотної солі на стадії випарювання електрощолоків, складає 2...3 кг×м-3 і перевищує кількість гідроксиду натрію, що необхідна для осадження іонів Mg2+ і Fe3+. Тому одна частина зворотного розсолу направляється в зону змішування освітлювача 10, а інша частина - у карбонізатор 5, куди подаються топкові гази, що містять не менше 6% (об’ємних) СО2. Гідроксид натрію, що утримується в зворотному розчині, карбонізується за реакцією:
NaOH + СО2 = Nа2СО3
+ Н2О.
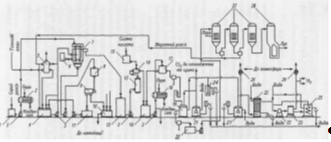
Рис.2.2. Технологічна схема
виробництва хлору і каустичної соди діафрагмовим методом: 1
-збирач сирого розсолу; 2- підігрівник сирого розсолу; 3- відцентрові насоси;
4-збирач зворотного розсолу; 5- колона карбонізація; 6- напірний бак для
гідролізованого поліакриламіду; 7- освітлювач; 8- напірний бак шламової
суспензії; 9- центрифуга; 10- приймач шламу; 11-приймач фільтрату; 12- збирач
чистого розсолу; 13- фільтр для розсолу; 14- бак-нейтралізатор; 15- напірний бак
для соляної кислоти; 16- збирач освітленого розсолу; 17- напірний бак для
освітленого розсолу; 18- підігрівник; 19- електролізери; 20- приймач щолоку;
21- гідразатвор; 22-холодильник змішування; 23-водневий компресор;
24-бризковідділювач; 25- холодильник; 26-вогнеперешкоджувачі; 27- випарні
апарати першого ступеня; 28- випарний апарат другого ступеня
Карбонізацію зворотного розчина ведуть з таким розрахунком, щоб утворилася достатня кількість соди для осадження іонів Са2+ і створення необхідного їх надлишку в очищеному розсолі - 0,3...0,4 кг×м-3. При цьому в зворотному розсолі повинен залишатися гідроксид натрію в кількості достатній для осадження магнію і створення надлишку NaOH не менше 0,05 кг×м-3. У випадку нестачі лугу в зворотному розсолі для виконання вищевказаних вимог добавляють розчини соди. Для цього в схему включають розчинник соди, ємності і насоси для содового розчину. Содовий розчин готують на зворотному розсолі з концентрацією соди 60...80 кг×м-3. Карбонізований і зворотний розсоли зі збірника 4 подають у зону змішування освітлювача 7. Для прискорення коагуляції осаду туди надходить гідролізований розчин поліакриламіду (ППА) з напірного баку 6. При інтенсивному перемішуванні сирого й зворотного карбонізованого розсолів в освітлювачі протікають реакції осадження іонів: