Материал: Використання напівпроникних мембран природного походження для виготовлення осмометрів
Використання напівпроникних мембран природного походження для виготовлення осмометрів
Міністерство освіти та науки України
Сумський державний педагогічний університет ім.А. C. Макаренка
кафедра хімії та методики викладання
хімії
Курсова робота
на тему:
"Використання напівпроникних
мембран природнього походження для виготовлення осмометрів"
Виконала:
студентка 631 групи
природничо-географічного факультету
Русанівська Неля
Науковий керівник: Бугаєнко В.В
Суми - 2011
Зміст
Вступ
Розділ I. Осмотичний тиск розчинів
1.1 Зворотній осмос
Розділ II. Методи дослідження осмотичного тиску
2.1 Комірка зі скляного фільтра
2.2 Комірка з мембраною із колодія
2.3 Комірка з мембраною із целофану
2.4 Комірка з мембраною зі свинячого міхура
Розділ III. Експериментальна частина
Висновки
Використана література
Вступ
Осмос (від грец. σμος "поштовх, тиск") - процес однобічної дифузії через напівпроникну мембрану молекул розчинника в бік більшої концентрації.
Вперше осмос спостерігав А. Нолле в 1748, однак дослідження цього явища було розпочато через століття. Явище осмосу спостерігається в тих середовищах, де рухливість розчинника більше рухливості розчинених речовин. Важливим окремим випадком осмосу є осмос через напівпроникну мембрану. Напівпроникні називають мембрани, які мають досить високу проникність не для всіх, а лише для деяких речовин, зокрема, для розчинника. Якщо така мембрана розділяє розчин і чистий розчинник, то концентрація розчинника в розчині виявляється менш високою, оскільки там частина його молекул заміщена на молекули розчиненої речовини [7,cт. 105]. Внаслідок цього, переходи частинок розчинника з відділу, що містить чистий розчинник, в розчин відбуватимуться частіше, ніж у протилежному напрямку. Відповідно, обсяг розчину буде збільшуватись (а концентрація зменшуватися), тоді як об'єм розчинника буде відповідно зменшуватися.
Наприклад, до яєчної шкаралупи з внутрішньої сторони прилягає напівпроникна мембрана: вона пропускає молекули води і затримує молекули цукру. Якщо такою мембраною розділити розчини цукру з концентрацією 5 і 10% відповідно, то через неї в обох напрямках будуть проходити тільки молекули води. У результаті в більш розбавленому розчині концентрація цукру підвищиться, а в більш концентрованому, навпаки, знизиться. Коли концентрація цукру в обох розчинах стане однаковою, настане рівновага. Розчини, які досягли рівноваги, називаються ізотонічними.
Осмос, спрямований усередину обмеженого обсягу рідини, називається ендосмос, назовні - екзосмос. Перенесення розчинника через мембрану обумовлений осмотичним тиском. Воно дорівнює надлишковому зовнішньому тискові, яке слід докласти з боку розчину, щоб припинити процес, тобто створити умови осмотичного рівноваги. Перевищення надлишкового тиску над осмотичним може призвести до звернення осмосу - зворотної дифузії розчинника.
Осмос грає важливу роль в багатьох біологічних процесах, в екології водойм, бере участь в перенесенні поживних речовин у стовбурах високих дерев, де капілярне перенесення не здатне виконати цю функцію. Завдяки цьому явищу здійснюється більшість процесів внутрішньоклітинного обміну. І триває життя [7, ст. 107].
Саме ці якості та проблеми і визначають актуальність теми курсової роботи.
Об`єктом дослідження мембрана тваринного походження.
Мета дослідження: визначити молярну масу сахарози за допомогою експериментального метода зі свинячим міхуром та порівняти з табличними даними.
Завдання роботи полягають в тому:
. опрацювати наукову літературу та періодичні видання з даної теми;
2. визначити який метод доцільний для проведення осмосу;
. опрацювати експериментально отримані результати;
. охарактеризувати необхідність
застосування осмосу у природі.
Розділ I. Осмотичний тиск розчинів
Водні розчини відіграють виключно важливу роль у всіх процесах, що протікають у ґрунтах, а також у живих і рослинних організмах. Всі природні води представляють собою розчини різних солей. Водні розчини - системи, найбільш поширені у природі, і тому вчення про розчини є важливим розділом фізичної хімії. Тому природа розчиненої речовини практично не робить впливу на властивості розведеного розчину.
В кінці XIX ст. Рауль, Вант-Гофф, Арреніус установили дуже важливі закономірності, що зв'язують концентрацію розчину з осмотичним тиском, тиском насиченої пари, температурою кипіння і замерзання. Застосувавши для узагальнення результатів вимірювань осмотичного тиску закони термодинаміки і молекулярно-кінетичну теорію газів, Вант-Гофф вперше встановив, що між станом речовини в дуже розбавленому розчині і газоподібним положенням є повне якісна і кількісна схожість. Іншими словами, осмотичний тиск сильно розбавлених розчинів підпорядковується законам ідеальних газі.
Про осмос, як про спосіб обміну речовин ми знаємо ще зі шкільних підручників. Завдяки осмосу, клітини організму забезпечуються живильними речовинами, і з них же виводяться токсини і шлаки, таким чином, здійснюється процес життєдіяльності.
В основі осмосу лежить принцип вибіркового пропускання молекул та іонів певних розмірів через напівпроникну мембрану за умови розділення цією мембраною двох сольових розчинів різних концентрацій. Наприклад, через мембрану проникають молекули води, а молекули розчинених у ній солей - ні. Завдяки різниці концентрацій сольових розчинів по обидва боки мембрани, молекули води будуть переміщатися з розчину з низькою концентрацією розчинених речовин у більш концентрований. Тому в більш концентрованому розчині рівень рідини підвищиться. Різниця у висоті рівнів двох розчинів різної концентрації пропорційна прикладеній силі, що діє на воду. Явище проникнення розчинника через напівпроникну мембрану в розчин одержало назву осмосу, а сила, в результаті дії якої вода проникає через пори мембрани, називається осмотичним тиском. Осмотичний тиск також можна тлумачити як додатковий гідростатичний тиск, який припиняє перехід розчинника через напівпроникну перетинку, що розділяє розчин і розчинник, або два розчини різної концентрації [1, ст.122].
Величина осмотичного тиску, створювана розчином, залежить від кількості, а не від хімічної природи розчинених у ньому речовин (або іонів, якщо молекули речовини дисоціюють). Чим більше концентрація розчину, тим більший буде утворюватися осмотичний тиск.
Експериментальні дані Пфеффера і лягли в основу
відкритого Вант-Гоффом (1887) закону осмотичного тиску. Вант-Гофф
показав, що осмотичний тиск в розведених розчинах неелектролітів
підпорядковується рівнянню:
р=cRT,
р - осмотичний тиск; с - молярність розчину.
Рівняння Вант-Гоффа показує, що осмотичний тиск дорівнює тому тиску,що мала б розчинена речовина, якби вона у вигляді ідеального газу займала б один і той же об`єм, що і в розчині, при тій же температурі [1, ст. 106].
Осмотичний тиск біологічних рідин в різних організмах неоднаковий, і значною мірою змінюється залежно від тиску зовнішнього середовища.
.1 Зворотній осмос
Даний метод фільтрації води прийшов до нас з історії мореплавства, де він був вперше застосований для опріснення морської води. Це один з найбільш ефективних методів, що дозволяє щодня очищати в світі сотні тисяч тонн води для питних і господарсько-побутових потреб не тільки промисловості способом, але і в домашніх умовах. Ступінь фільтрації води в таких установках унікальна. Очищена вода набуває властивостей талої води льодовиків.
Зворотний осмос - це процес, коли на воду з більшою концентрацією солей додатково впливає зовнішній тиск, за величиною більше, ніж осмотичний. У такому випадку молекули води будуть рухатися в зворотному напрямку - з більш концентрованого розчину в розчин з меншою концентрацією. У процесі зворотного осмосу вода і розчинені в ній речовини розділяються на молекулярному рівні і по один бік мембрани накопичується чиста вода, а все, чим вона була забруднена, залишається з іншого боку. Основними показниками, від яких залежить ефективність роботи систем і установок зворотного осмосу є температура, водневий показник рН і хімічний склад очищуваної води. Чим вищий створюється тиск перед мембранним елементом, тим вища продуктивність установки зворотного осмосу, і краще якість отриманої очищеної води [8]. Метод зворотного осмосу гарний тим, що видаляються органічні речовини, надлишок мінеральних сполук, але у воді залишаються кисень та інші гази. Які відповідають за смак води. Українські лікарі визнають, що вітчизняна система водопостачання не готова забезпечити населення безпечною питною водою. Більше 80% захворювань Жителів України пов'язане саме з якістю питної води. Для забезпечення повної відповідності водопровідної води потребам людського організму, відповідності нормам, буде потрібно серйозна реконструкція існуючих муніципальних водоочисних споруд, заміна великої частини водопровідних і каналізаційних трубопроводів, зменшення викидів промислових підприємств, утилізація і переробка побутових відходів. Таке завдання вимагає значних капіталовкладень, і не може бути виконана в короткі терміни. Багато споживачів намагаються вирішити для себе проблему очистки води різними, часом не завжди ефективними способами. Відстоювання, кип'ятіння, застосування рідких флокулянтів, механічна фільтрація, сорбція - кожен з цих методів очищення води здатний лише частково вирішити питання підготовки питної води. У багатьох населених пунктах водопровідна вода не відповідає нормам за такими показниками, як вміст заліза, жорсткість, загальний солевміст. Кип'ятіння усуває жорсткість води лише на половину. При нагріванні води, утворюється нерозчинний з'єднання - карбонат кальцію, який випадає в осад у вигляді накипу, яку ми бачимо в чайнику, а залишкова жорсткість - усувається тільки за допомогою спеціального обладнання - пом'якшувач води. Практично всі види забруднень питної води можна усунути при допомозі фільтра на основі зворотного осмосу.
На даний момент зворотний осмос - практично єдина технологія, що дозволяє за розумну ціну отримати достатню кількість питної води.
Чи потрібно говорити, що більшість видів бутильованої питної води, або води, яку розвозять різні служби доставки, виробляють саме за допомогою системи зворотного осмосу. так, щоб пити чисту воду ми повинні купувати фільтровану воду в магазині, або встановити у себе вдома фільтр очищення питної води на основі зворотного осмосу. Що стосується смаку води, що пройшла очищення за допомогою фільтру зворотного осмосу, то він не йде ні в яке порівняння з кип'яченою водою. Плюс до цього, нагрівальні елементи чайника й кавоварки будуть мати первозданний вигляд протягом багатьох років. Чиста вода - запорука здоров'я, а воно - основне джерело задоволення життям. Сьогодні, піклування про своє здоров'я, здоров'я своєї родини - справа кожного. Постійне вживання чистої, фільтрованої води дозволить вам відчути різницю в смаку напоїв і страв, які ви готуєте. Ви забудете про плівку в чашці чаю. Воду можна пити прямо з під крана, в будь-який час. Заморозивши її в крижані кубики, ви ніколи не зіпсуєте ними смак коктейлю, а гарна кава віддасть вам свій справжній "бразильський" аромат.
мембрана осмотичний тиск колодій
Розділ II. Методи дослідження осмотичного тиску
2.1 Комірка зі скляного фільтра
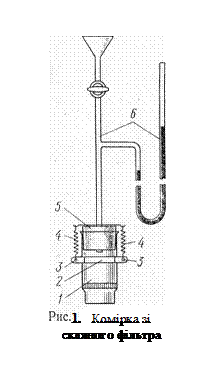
На рис.1. схематично зображено осмотичну комірку, за допомогою якої з успіхом демонструють досить високі осмотичні тиски розчинів. Ця комірка виготовляється наступним чином. Шотовський скляний фільтр 1 марки 1G2 добре прогрівають на полум'ї газового пальника і вливають в нього нагрітий 15% -ний розчин желатину, так щоб на дні фільтра утворився шар завтовшки в 1 мм. Після того як желатин застигне, вливають у фільтр 3% -ний розчин гексаціано (II) ферат калію і занурюють його в розчин сульфату міді такої ж концентрації майже на добу. З латунної стрічки виготовляють кільце 2, яке як обруч має щільно охоплювати злегка конічні стінки скляного фільтра, причому по обидва боки кільця повинні бути "вушка" 3 з отворами, у які будуть входити кінці пружинок 4, що кріплять гумову пробку 5. Досліджуваний розчин наливають у підготовлену таким способом осмотичну комірку і, стежачи за тим, щоб усередині не залишалось бульбашок повітря, щільно закривають її корком зі вставленою в неї манометричною трубкою 6. Слід зазначити, що після кожного досліду комірку знову доводиться виготовляти заново. Для цієї мети комірку розбирають, ретельно промивають у хромовій суміші, а потім все повторять в такій же послідовності, як було описано вище.
Проведення досліду А. Розчиняють близько 150 г тростинного цукру в 75 мл окропу, охолоджують отриманий розчин до кімнатної температури і підфарбовують, вводять в нього один-два мл розчину еозину. Таким чином, розчин тростинного цукру отримують майже насиченим (65%). Далі цей розчин вливають в осмотичну комірку, який занурюють у велику склянку з дистильованою водою (можна використовувати і водопровідну воду).
Результат досліду. Забарвлений розчин піднімається в манометричній трубці зі швидкістю приблизно декількох міліметрів на хвилину. Через деякий час розчин буде випливати з манометричної трубки і його можна збирати в мірний циліндр. Якщо осмотична комірка працює добре, то в зовнішній розчин барвник надходити не буде.
Проведення досліду Б. Заповнюють осмотичну комірку розчином, що містить 0,25% тростинного цукру і 0,3% жовтої кров'яної солі, і занурюють їх у посудину 0,12% -ного розчину сульфату міді.
Результат досвіду. Після закінчення певного часу рідина в трубці манометра піднімається приблизно на 1,7 м. Досить зручно для вимірювання осмотичного тиску використовувати ртутний манометр. Необхідно тільки стежити за тим, щоб в просторі між осередком і ртуттю не було бульбашок повітря. Виміряний з допомогою ртутного манометра тиск буде дорівнює приблизно 130 мм. рт. ст.
Проведення досліду В. Виготовляють осмотичну комірку,
схема якої показана на рис. 2. Бічне відгалуження крана через гумову
трубку з'єднане з капілярною трубкою, по всій довжині якої наклеєна полоса
міліметрового паперу. Перед постановкою досвіду капіляр повинен бути ретельно
промитий гарячою хромовою сумішшю. Осмотичну комірку разом з трубкою і
капіляром заповнюють дистильованою водою і занурюють у кристалізатор з
досліджуваним розчином. При цьому потрібно постаратися, щоб у трубці і капілярі
не було бульбашок повітря.
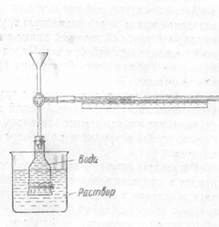
Рис. 2
Результат досліду. Як тільки осмотичний осередок прийде в зіткнення з випробуваним розчином, меніск рідини в капілярній трубці починає рухатися в бік осередку. Проектуючи капілярну трубку на екран проекційним ліхтарем, фіксують положення меніска на початку досліду і, включивши секундомір, виміряють час, за який меніск пройде шлях довжиною в 30 см.
У якості піддослідних розчинів можна взяти по 100 мл розчинів тростинного цукру наступних мольних концентрацій: 0,5, 1,0, 1,5 і 2,0. При зміні розчинів необхідно кожен раз споліскувати зовнішню сторону мембрани невеликою кількістю випробуваного розчину; а також знову заповнювати через лійку і кран капілярну трубку дистильованою водою, як це вже було описано вище.
Якщо у демонстрації потрібно показати, що розчини електролітів в силу своєї дисоціації володіють у порівнянні з розчинами неелектролітів при однакових молярних концентраціях більш високим осмотичним тиском, слід в досвіді використовувати мембрану з великим терміном висушування. Цілком зрозуміло, що при роботі з такою мембраною швидкість переміщення меніска рідини в капілярній трубці буде значно менше в порівнянні з попереднім досвідом.
Проведення досліду Г. Змішують приблизно по 10 мл фенолу і води. Після ретельного збовтування і відстоювання, суміш чітко поділяється на два шари: нижній шар - фенол, насичений водою, і верхній - вода, насичена фенолом. За допомогою невеличкої дільникової воронки відокремлюють шар води, насичений фенолом, і ділять його на дві частини. В одній частині розчиняють майже до насичення нітрат кальцію Са (NO3) 2, другу частину залишають без зміни. Після зливання всіх розчинів в пробірку спостерігають утворення трьох шарів рідини (знизу вгору): вода + фенол + нітрат кальцію, фенол + вода, вода + фенол. Шари добре помітні, оскільки середній шар фенолу, насичений водою, має в порівнянні з іншими двома шарами більш темне забарвлення. Пробірку залишають у спокої на 24 год, після чого спостерігають зміну положення шарів.