Материал: Виготовлення та дослідження органічного фотоелементу
Виготовлення та дослідження органічного фотоелементу
Міністерство освіти і науки України
Департамент освіти і науки Харківської облдержадміністрації
Харківське територіальне відділення МАН України
Відділення: хімія та біологія
Секція: хімія
Виготовлення та дослідження
органічного фотоелементу
Роботу виконав:
Лебединець Олександр,
Учитель хімії:
Самошко Любов Миколаївна
Науковий керівник:
Марков
Вадим Вікторович, молодший науковий співробітник, викладач кафедри хімічної
метрології хімічного факультету Харківського національного університету ім.
В.Н. Каразіна
Харків - 2014
ЗМІСТ
ЗМІСТ
ВСТУП
РОЗДІЛ 1. ЛІТЕРАТУРНИЙ ОГЛЯД ЯВИЩ, ЩО ВИКОРИСТОВУЮТЬСЯ В ХОДІ РОБОТИ
РОЗДІЛ 2. ВИГОТОВЛЕННЯ ОРГАНІЧНОГО ФОТОЕЛЕМЕНТА
РОЗДІЛ 3. ВИМІРЮВАННЯ ПАРАМЕТРІВ ТА ПОРІВНЯННЯ З КРЕМНІЄВИМ ФОТОЕЛЕМЕНТОМ
РОЗДІЛ 4. ТЕХНІКА БЕЗПЕКИ
ВИСНОВКИ
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
ВСТУП
Чисельність населення планети Земля з кожним століттям зростає. Якщо на початку нашої ери проживало близько 200-300 млн. осіб, за часів відкриття Колумбом Америки 500 млн., на початку ХХ століття 1,6 млрд., а приблизна кількість на кінець ХХІ століття становить 10-12 млрд. осіб. Але ми зможемо и не прожити до кінця ХХІ століття, бо у наш час постає проблема екології, швидкого вичерпання корисних копалин, наприклад, природного газу та нафти вистачить не більше ніж на сторіччя, а вугілля вистачить ще на 300 років, але не потрібно думати, що воно зможе замістити всі паливні ресурси. Хоча в наш час вчені вже знайшли спосіб синтезувати и нафту и газ, але потім постає проблема парникового ефекту, через збільшення концентрації СО2 в нашій атмосфері. Вуглекислий газ виділяється при всіх реакціях горіння нафти, природного газу, вугілля. На допомогу вирішенню цієї проблеми приходять альтернативні джерела енергії - вітер, сонячна енергія та інше. Сонячна енергія є найдоступнішою, бо кожного дня 12-13 годин сонце опромінює нашу планету.
Використання сонячної енергії має специфічні переваги та недоліки. Ця енергія необмежена, але її використання досить утруднене. Сучасні фотоелементи досить неефективні через низку фундаментальних причин, вони дорогі та мають обмежений термін служби.
Класичні фотоелементи базуються на чутливості напівпровідникових структур до світла. Вони виробляють чисту енергію, але процес виробництва та переробки після закінчення терміну експлуатації досить складний та екологічно небезпечний. Тому активно проводяться дослідження альтернативних принципів перетворення світлової енергії на електричну. Це допоможе боротися бодай з ціною та екологічною небезпекою галузі.
року М. Гретцель відкрив фотоелектрохімічні комірки на основі фоточутливих мезопористих оксидів металів[1]. Ці комірки є багатообіцяючими, бо сировина для їх виготовлення дешева, та процес не дуже складний. Вони базуються на використанні органічного барвника, тому будемо посилатися на них як на органічні фотоелементи. В період між відкриттям цих комірок та 2014 роком, багато вчених пропонували різні модифікації, зміни в конструкції, використаних матеріалах, і за допомогою цього з кожним роком КПД комірок Гретцеля зростає.
На відміну від добре відомих та широко досліджених напівпровідникових фотоелементів, органічні зараз знаходяться у стадії вивчення. Тому метою роботи буде виготовлення та дослідження властивостей органічного фотоелементу.
Для успішного досягнення мети необхідно вирішити такі завдання:
. Відпрацювати методику нанесення провідникової плівки на скло
. Виробити власне органічний фотоелемент
. Дослідити його електричні параметри
Об'єктом дослідження є вироблений органічний фотоелемент.
Робота є практичною. У результаті виготовлено органічний
фотоелемент виходячи з простих реактивів та обладнання та виміряно його
електричні параметри.
РОЗДІЛ 1. ЛІТЕРАТУРНИЙ ОГЛЯД ЯВИЩ, ЩО ВИКОРИСТОВУЮТЬСЯ В ХОДІ РОБОТИ
1.1 Електрохімія
Електрохімія вивчає електричні процеси в хімічних системах. Електричний струм це організований рух електричних зарядів у деякому контурі, тобто замкнутому ланцюгу. Не всі матеріали можуть проводити електричний струм. За механізмом провідності їх можна розділити на дві основні групи: електронні та іонні провідники. До електронних належать метали й деякі напівпровідники, до іонних - розчини, розплави солей, плазма.
Електричний контакт електронного та іонного провідника називають електродом. Електричне сполучення двох електродів дає нам електрохімічну комірку. Залежно від хімічного складу в ній можуть відбуватися певні хімічні реакції, які обов’язково супроводжуються виникненням електричного струму в ланцюгу. При цьому на одному електроді проходить процес окиснення речовини, він називається анодом, на іншому - катоді - процес відновлення.
Електрохімічні комірки можуть працювати в одному з двох режимів. Якщо при протіканні спонтанної реакції система виробляє електричну роботу, ми маємо гальванічну комірку. Якщо певна реакція проходить тільки при пропусканні електричного струму від якогось зовнішнього джерела, то така система називається електролітичною коміркою. Можливість комірки працювати в тому чи іншому режимі залежить від її хімічного складу та конструкції. Гальванічну комірку називають хімічним джерелом струму. Джерело, що може лише віддавати напругу, називається первинним джерелом струму. Типовим прикладом є звичайні батарейки, які не підлягають заряджанню. Акумулятори відносять до вторинних джерел струму. При заряджанні вони працюють як електролітична комірка [2].
Процеси, що проходять у електрохімічній комірці, можна
описати протікаючим струмом та електрорушійною силою.
1.2 Квантова теорія світла
Потік світла одночасно проявляє властивості потоку частинок
та електромагнітної хвилі[3]. Так, проявом хвильової природи є явища
інтерференції та дифракції. Хвилю можна описати швидкістю розповсюдження,
довжиною та частотою. Електромагнітна хвиля завжди розповсюджується зі
швидкістю світла, яка дорівнює близько 3∙108 м/с. Довжина хвилі світла
залежить від кольору та лежить в межах приблизно від 380 нм для фіолетового
світла до 760 нм для червоного. Залежність цих величин описується рівнянням:
c = λν,
де с - швидкість світла, λ - довжина хвилі, ν - частота коливань.
Зазвичай світло являє собою суміш хвиль з різною частотою.
Але деякі фізичні ефекти не можна описати за допомогою цієї
теорії. Наприклад, це зовнішній фотоефект. При падінні світла на поверхню
металу у вакуумі може випромінюватись електрон. Але цей ефект різко зникає,
якщо довжина хвилі світла перевищить певну величину, що залежить від хімічної
природи металу. Для пояснення цього факту Ейнштейн у 1905 році застосував
гіпотезу Планка про квантову природу світла. За нею, світло випромінюється
окремими порціями - квантами. Енергія кожного кванта пов’язана з довжиною хвилі
світла за формулою:
E = hν,
де E - енергія кванта світла, h - постійна Планка, що дорівнює 6.63∙10-34 Дж∙с, ν - частота коливань.
Треба пам’ятати, що хоча фотон і належить до числа
елементарних частинок, але є частинкою не речовини, а поля. Тобто це складова,
або структурна, частинка електромагнітного поля. Що ж таке світло? Це
випромінені джерелом електромагнітні хвилі, чи джерело світла випускає потік
фотонів, які рухаються у просторі зі швидкістю світла у вакуумі? По-перше
здається, що ці два погляди на природу світла - хвильовий і квантовий - взаємно
виключають один одного. Очевидно, що ряд ознак хвиль і частинок справді
протилежні. Наприклад, фотони, рухаючись, перебувають у певних точках простору,
а у випадку поширення хвилі не можна говорити про її перебування в якійсь
певній точці. Хвилю можна розділити на частини і такий поділ нічим не
обмежений, а фотон поділити не можна. У прояві двоїстих властивостей
випромінювання спостерігається важлива закономірність. Якщо частоти малі,
більшою мірою проявляються хвильові властивості випромінювання (наприклад,
радіопроміння), а для великих частот - квантові властивості (наприклад,
рентгенівське проміння). У видимому світлі хвильові й квантові властивості
виявляються однаковою мірою.
1.3 Органічні фотоелементи
Були винайдені Гретцелем у 1991 році [1]. Звичайні фотоелементи базуються на створенні так званого p-n переходу між двома напівпровідниками. Цей перехід має односторонню провідність, тобто струм може проходити лише в прямому напрямку. При освітленні такого переходу достатньо короткохвильовим світлом проходить формування вільних зарядів та генерація струму. Недоліком таких фотоелементів є складність та не екологічність їх виробництва. Отримання надчистого кремнію є досить складним та дорогим процесом
Натомість, у природі існує приблизно аналогічний процес - фотосинтез. Вчені дуже довго намагалися відтворити його в лабораторних умовах. Аналогія тут неповна, але і фотосинтез, і робота фотоелементу направлені на перетворенні енергії світла у більш корисну та придатну для використання форму.
В органічному фотоелементі розділені етапи поглинання світла
та генерації струму. Молекула барвника поглинає квант світла та окислюється,
виділяючи електрон. Оскільки барвник знаходиться в фотоелементі в адсорбованому
стані, електрон інжектується в оксид титану з n-провідністю, тим самим
генеруючи струм. Для замикання ланцюга та забезпечення безперервності процесу
використовується електроліт, що містить трийодид.
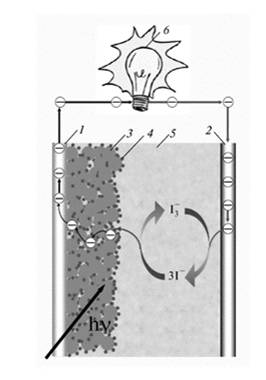
Рис. 1.1 Структура органічного фотоелементу
На рис 1.1 показано принцип роботи такого фотоелементу. Світло падає на прозорий фотоанод 1, на який нанесено шар оксиду титану 3. Адсорбований барвник 4 генерує електрони при освітленні. Вони протікають через зовнішній ланцюг 6, створюючи корисну роботу. На катоді 2 проходить відновлення трийодиду в електроліті 5. Ефективність такого елементу становить близько 7%. Це значно менше, ніж типові 22% для типових кремнієвих фотоелементів.
Також у органічних фотоелементів є певні недоліки. Органічний
барвник деградує з часом. Рідкий електроліт вступає у побічні реакції та може
випаровуватись. Але фотоелемент може бути досить просто регенерований. Заміна
барвника на новий досить проста.
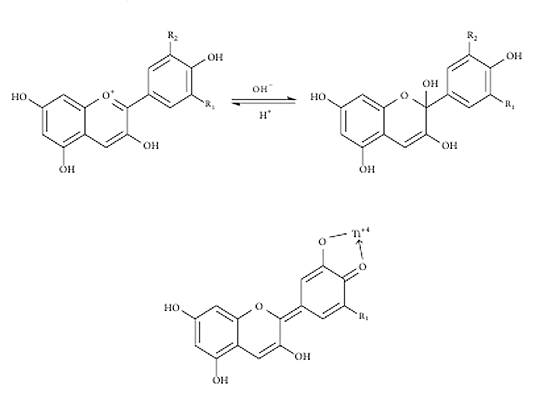
1.4 Антоцианіни
Для роботи органічного фотоелементу потрібен органічний барвник. Він формує комплекс з оксидом титану та переносить електрон від електроліту до електроду за рахунок збудження квантом світла [4]. У ролі барвника можуть виступати багато кольорових органічних сполук, більшість з них рослинного походження. Найбільша кількість досліджень присвячена використанню рослинних антоцианінів [5].
Антоцианіни належать до більш широкого класу ізофлавоноїдів,
похідних 3-фенілхроману. В даній роботі у якості джерела антоціаніну
використовується малина. Вона містить суміш антоцианінів, але найбільший вміст
припадає на цианідін-3-софорозід. Це глікозид, що містить антоцианідиновий
фрагмент цианідину та залишок дисахариду софорози.
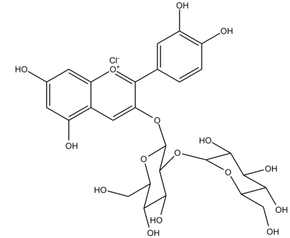
Рис. 1.2 Структура цианідін-3-софорозіду
Рис. 1.3 Основні реакції антоцианідінів
РОЗДІЛ 2. ВИГОТОВЛЕННЯ ОРГАНІЧНОГО ФОТОЕЛЕМЕНТА
2.1 Методика отримання електропровідного скла
Відомо, що на основі тонких прозорих шарів напівпровідникових оксидів металів, таких як SnO2, In2O3, TiO2 утворюються структури напівпровідник-діелектрик-напівпровідник, застосовувані для перетворення сонячної енергії в електричну. Крім того, шари SnO2 і TiO2 з успіхом можуть застосовуватися в сонячних елементах на основі Si і InP в якості антивідбиваючого покриття за рахунок прозорості у видимій області спектра і підходящих значень коефіцієнтів заломлення (n = 2,0 і n = 1,72-2,60 відповідно), що збільшує ефективність перетворення сонячної енергії в електричну [6].
Властивості напівпровідникових плівок і структур багато в чому визначаються технологією їх виготовлення. У даний роботі описана технологія отримання шарів на основі SnO2, а також досліджено їх оптичні властивості. Використаний метод піролітичної пульверизації для отримання шарів досить простий і економічний і не вимагає складного обладнання.
Плівки SnO2 утворювалися при розпиленні розчинів SnCl4 в метанолі на розігріті до 450оС пластини кварцу.
Для отримання SnO2 використовувався 0,5 М розчин SnCl4 в метанолі. У деяких випадках з метою легування плівки використовували стибій (0,1 М розчин SbCl3 в метанолі). Для приготування розчину до 11 мл 0,5 М розчину SnCl4 додавали до 2 мл 0,1 М розчину SbCl3 [6].
Було випробувано декілька методик отримання електропровідної плівки оксиду стануму на поверхні скла. Їх можна поділити на дві групи: оприскування гарячого скла спиртовими розчинами SnCl4 та сублімація SnCl2.
Розчини для обприскування готувалися з кристалогідрату SnCl4·5H2O. Масова концентрація у перерахунку на кристалогідрат становила від 30% до 80% за масою. Також в деяких випадках додатково вводилася вода у кількості до 30% за масою. Для підвищення електропровідності вводився стибій у кількості 5% від кількості речовини стануму. Стибій вводився у вигляді солянокислого розчину у метанол, потім до розчину додавався твердий кристалогідрат. Така послідовність змішування запобігає гідролізу та випадінню осаду оксиду стибію. Перед оприскуванням скла воно розігрівалося у муфельній печі до температури 400-500 градусів Цельсію [7].
Незалежно від складу розчину скло тріскалося при оприскуванні. Можливо, це пов’язано с низькою якістю оприскувача, оскільки він дає досить великі краплі. Скло, розігріте до температури близько 300 градусів не тріскається, але плівка осаджується у вигляді не повністю гідролізованого оксиду молочно-білого кольору. Він не проводить електричний струм.
Альтернативна методика заснована на сублімації кристалогідрату SnCl2·2H2O при більш помірному нагріванні та конденсації продуктів сублімації на склі. При нагріві хлориду стануму він спочатку жовтіє. А потім виділяє білій дим невідомого складу, ймовірно гідрати оксидів стануму. Якщо дати цьому диму «обтікти» скло, він конденсується у вигляді прозорої райдужної плівки. Властивості отриманої плівки невідомим нам чином залежать від температури скла, швидкості обтікання та можливо ще якихось факторів. Стабільно відтворити цей експеримент не вдалося. В ході одного з експериментів було отримано невелике за площею покриття опором порядка 10 кОм, що дозволило провести попередні дослідження [8].
Тому було вирішено повернутися до методики з оприскуванням та замінити скло на кварц. Це дозволило осадити при температурі близько 600 градусів тонку однорідну плівку з опором 100 Ом, що дозволило провести подальші експерименти. Для оприскування використовувався розчин, що містив 13 г SnCl4·5H2O, 0.2 г Sb2O3, 1 мл HCl, 7 мл метанолу.
При пульверизації на повітрі і наступному піролізі відбувається ряд реакцій, пов'язаних з гідролізом, випаровуванням і окисленням, які в загальному вигляді можна представити таким чином:+ O2 = SnO2 + 2Cl2
SbCl3 + 3O2 = 2Sb2O3+ 6Cl2
Для отриманих шарів SnO2 було виміряно спектри пропускання.
На рис. 2.1 наведено такий спектр для шарів SnO2, нанесених на кварцову основу.
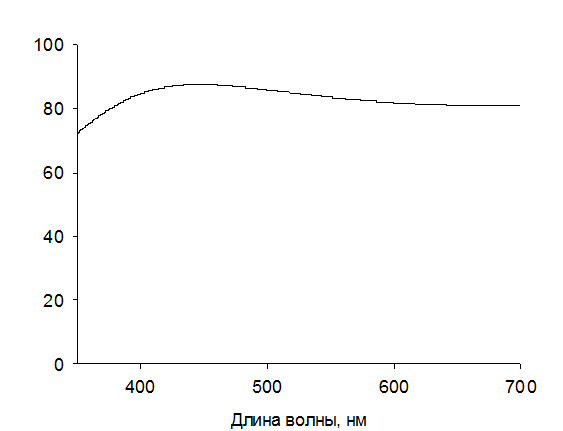
Прозорість даних шарів в видимому діапазоні довжин хвиль
досягає 87%. На рисунку 2.2 приведено фото електропровідної плівки осадженої на
кварц.

Рис. 2. 2 Фото електропровідної плівки.
Наступним кроком було нанесення шару діоксину титану.
Готувалася суспензія дрібнокристалічного оксиду титану у 2% розчині оцтової
кислоти з додаванням невеликої кількості неіонної поверхнево-активної речовини.
Діоксид титану ретельно розтирався у ступці з додаванням невеликої кількості
розчину кислоти до густини трохи рідшої, ніж зубна паста. Для нанесення тонкого
рівномірного слою по краях електропровідного скла наклеювали клейку стрічку для
утворення «лотку». У центр скла наносили декілька крапель суспензії диоксиду
титану та проводили скляною паличкою паралельно склу, спираючись на стрічки. Це
дозволяло отримати досить рівномірний шар суспензії товщиною близько 50 мкм.
Отриманий шар сушили в потоці теплого повітря до повного висихання.