Материал: В-Л-Быков-Цитогогия_и_общая_гистология
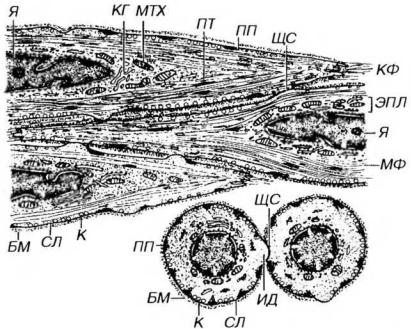
Рис. 13-15. Ультраструктурная организация гладких миоцитов. Ядро (Я) располагается в центре клетки и окружено эндоплазмой (ЭПЛ) - участком цитоплазмы, содержащим органеллы общего значения - митохондрии (МТХ), комплекс Гольджи (КГ), цистерны грЭПС. Периферическая часть цитоплазмы (эктоплазма) занята миофиламентами (МФ), связанными с плотными тельцами (ПТ) и плотными пластинками (ПП). Базальная мембрана (БМ) прилежит к сарколемме (СЛ), с которой связаны многочисленные кавеолы (К) В области углублений СЛ по краям миоцита к ней прикреплены коллагеновые фибриллы (КФ). Соседние миоциты образуют интердигитации (ИД) и щелевые соединения
(ЩС).
Тонкие (актиновые) миофиламенты образованы особым набором изоформ актина, свойственным гладким миоцитам, причем помимо мышечного актина в них обнаруживается и немышечный (цитоплазматический) актин. Тонкие филаменты преобладают над толстыми по количеству и занимаемому объему. Они более многочисленны, чем в поперечнополосатых мышечных тканях и располагаются в саркоплазме пучками по 10-20 филаментов, лежащими параллельно или под углом к длинной оси клетки и образующими сетевидные структуры. Концы актиновых филаментов закреплены в особых образованиях, находящихся в саркоплазме или связанных с сарколеммой - плотных тельцах (см. ниже); последние служат также областью фиксации промежуточных филаментов.
- 441 -
Толстые (миозиновые филаменты), в отличие от таковых в поперечнополосатой мышечной ткани, обладают различной длиной (при этом они значительно короче тонких нитей), менее стабильны, не содержат центральной гладкой части, поскольку покрыты миозиновыми головками по всей длине. Это обеспечивает более значительное перекрытие тонких и толстых филаментов, а, следовательно, и большую силу сокращения. Относительное содержание миозиновых филаментов в гладких миоцитах ниже, чем в миофибриллах поперечнополосатой мышечной ткани; на один миозиновый филамент в гладких миоцитах приходится не менее 12 актиновых. По мнению некоторых авторов, миозиновые филаменты гладких миоцитов обладают значительной лабильностью и окончательно собираются непосредственно перед сокращением, распадаясь после него.
Сокращение гладких миоцитов обеспечивается взаимодействием актиновых и миозиновых миофиламентов и развивается в соответствии с моделью скользящих нитей. Оно происходит более медленно и длится дольше, чем в скелетной мышце, что обусловлено более низкой скоростью гидролиза АТФ в гладких миоцитах.
Роль Са2+ в сокращении гладких миоцитов. Как и в поперечнополосатых мышечных тканях, сокращение гладких миоцитов индуцируется притоком Са2+ в саркоплазму, который в этих клетках выделяется саркоплазматической сетью и кавеолами (см. ниже), а также вследствие увеличения проницаемости сарколеммы для данных ионов. Однако (в отличие от поперечнополосатых мышечных тканей) основное влияние Са2+ оказывает не на актиновые, а на миозиновые филаменты. Миозин гладких миоцитов способен взаимодействовать с актином только после фосфорилирования его легкой цепи особым ферментом киназой легких цепей миозина. Этот фермент активируется под влиянием комплекса, образующегося в саркоплазме гладкого миоцита при связывании Са2+ белком кальциймодулином. Дефосфорилирование миозина, происходящее под влиянием фермента фосфатазы миозина, прекращает взаимодействие между актином и миозином и вызывает расслабление гладких миоцитов.
Образование мостиков типа "щеколды" (latch-bridges в англоязычной литературе) является особенностью сократительного аппарата гладких миоцитов: часта миозиновых мостиков после дефосфорилирования не отсоединяется от актина, а остается с ним связанной. Благодаря этому гладкая мышца способна обеспечивать длительное поддержание тонуса без существенных дополнительных энергетических затрат (так как указанные мостики обладают очень медленной циклической активностью).
- 442 -
Регуляция сокращения гладких миоцитов. Активация фермента киназы легких цепей миозина происходит, под действием не только Са2+, но и цАМФ. По этой причине гормоны, повышающие содержание цАМФ в гладких миоцитах, усиливают их сократительную деятельность. Так, эстрогены повышают, а прогестерон снижает уровни цАМФ в гладких миоцитах матки, что обусловливает их сокращение и расслабление, соответственно. Регуляция сокращения гладких миоцитов осуществляется не только на уровне миозиновых нитей, но, отчасти и на уровне актиновых - посредством ряда регуляторных белков: лейотонина (аналога тропонина), кальпонина и кальдесмона.
Опорный аппарат гладкого миоцита представлен его сарколеммой,
базальной мембраной, системой элементов цитоскелета и связанных с ними плотных телец.
Сарколемма каждого миоцита окружена базальной мембраной, в которую вплетаются тонкие ретикулярные, коллагеновые и эластические волокна; коллагеновые фибриллы, прикрепляющиеся к сарколемме в области ее углублений по краям миоцитов, воспринимают усилие, развивающееся при сокращении клеток.
Промежуточные филаменты содержатся в гладких миоцитах в значительно более высоких количествах, чем в кардиомиоцитах и волокнах скелетной мышечной ткани. В гладких миоцитах внутренних органов они образованы преимущественно десмином с небольшим содержанием виментина; в миоцитах сосудов, напротив, основным их компонентом служит виментин, а содержание десмина невелико.
Плотные тельца - овальные или веретеновидные структуры шириной до 0.35 мкм и длиной, в среднем, 1 мкм, лежащие вдоль длинной оси миоцита свободно в его саркоплазме или связанные с внутренней поверхностью сарколеммы (см. рис. 13-15 и 13-16).
Плотные тельца, связанные с сарколеммой, некоторые авторы называют плотными пластинками и считают структурами, не идентичными расположенным в саркоплазме (поскольку они различаются по химическому составу). Более того, в соответствии с современными представлениями, плотные пластинки лишь на срезах кажутся отдельными небольшими образованиями, в реальности же они имеют вид длинных непрерывных "ребер", идущих параллельно друг другу по внутренней поверхности сарколеммы вдоль длинной оси миоцита (см. рис. 13-16).
Плотные пластинки включают периферический и глубокий слои. Первый прилежит к сарколемме и образован филаментами немышечного актина, связанными с трансмембранными белками интегринами по-
- 443 -
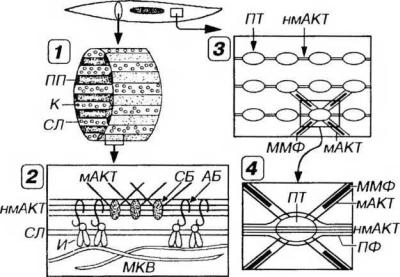
средством комплекса адгезивных белков (винкулина, талина, тензина и др.). В глубоком слое филаменты мышечного актина прикреплены к молекулам немышечного актина связующими белками (например, филамином).
Рис 13-16. Взаимосвязь элементов цитоскелета и сократительного аппарата гладкого миоцита. 1 - плотные пластинки (ПП) в виде "ребер” идут параллельно друг другу по внутренней поверхности сарколеммы (СЛ) вдоль длинной оси миоцита. Кавеолы (К) располагаются в зонах между ПП. 2 - ПП включает периферический и глубокий слои. Первый прилежит к СЛ и образован филаментами немышечного актина (нмАКТ), связанными с трансмембранными белками интегринами (И) посредством комплекса адгезивных белков (АБ). В глубоком слое филаменты мышечного актина (мАКТ) прикреплены к молекулам нмАКТ связующими белками (СБ). МКВ - межклеточное вещество (фибриллы, взаимодействующие с И). 3 - плотные тельца (ПТ) посредством филаментов нмАКТ соединены друг с другом в цепочки, продольно лежащие в саркоплазме; 4 - пучки филаментов мАКТ проникают в ПТ под углом (на фрагменте "З" изображены частично), а промежуточные филаменты (ПФ) окружают их по периферии. Сокращение клетки обеспечивается взаимодействием актиновых и расположенных между ними миозиновых миофпламентов (ММФ) в соответствии с моделью скользящих нитей.
Плотные тельца, свободно лежащие в саркоплазме, согласно новейшим данным, не разбросаны диффузно (как полагали ранее), а располагаются вдоль длинной оси клетки в виде цепочек с интервалом около 2 мкм, соединяясь друг с другом нитями немышечного (цитоплазматического) актина. Пучки филаментов мышечного актина проникают в плотные тельца под углом, а пучки промежуточных филаментов окружают их по периферии (см. рис. 13-16).
- 444 -
Плотные тельца содержат высокие концентрации α-актинина и десмина (в тельцах, связанных с сарколеммой, обнаруживаются также талин и винкулин). Из-за связи с актиновыми филаментами плотные тельца рассматривают как структуры, гомологичные Z-полоскам в поперечнополосатых тканях: их связь с промежуточными филаментами сближает их с пластинками прикрепления десмосом.
Аппарат передачи возбуждения (с сарколеммы на сократительный аппарат) в гладких миоцитах изучен недостаточно. К нему относят саркотазматическую сеть, которая в этих клетках рудиментарна и состоит из системы мелких цистерн и пузырьков, а также особые мембранные структуры - кавеолы. Т-трубочки отсутствуют.
Кавеолы - колбовидные впячивания поверхности сарколеммы диаметром около 70 нм (с более узкой "шейкой"), располженные перпендикулярно длинной оси клетки. Кавеолы открыты в сторону межклеточного пространства, часто располагаются рядами вдоль длинной оси миоцита (занимая промежутки между плотными пластинками), иногда уходят вглубь его саркоплазмы в виде ветвящихся цепочек. Они очень многочисленны (до нескольких сотен тысяч в одной клетке); площадь их суммарной поверхности составляет около 1/3 площади поверхности сарколеммы. Число кавеол не меняется при сокращении, расслаблении или растяжении клетки, они, по-видимому, не участвуют в процессах эцдоцитоза. Кавеолы содержат высокие концентрации кальция, а в их мембране имеются белки, обеспечивающие транспорт кальция в саркоплазму и из нее. Местами они контактируют с элементами саркоплазматической сети. Кавеолы, по-видимому, не только гомологичны системе Т-трубочек поперечнополосатых мышечных тканей, но и выполняют ряд функций, свойственных саркоплазматической сети.
Энергетический аппарат гладких миоцитов представлен митохондриями, а также включениями, содержащими субстраты, расщепление которых обеспечивает энергетические потребности клеток. Митохондрии в гладких миоцитах - сравнительно мелкие, с умеренно развитыми кристами, располагаются вместе с небольшими скоплениями гранул гликогена и мелкими липидными каплями преимущественно у полюсов ядра. Часть митохондрий лежит под сарколеммой. Включения гликогена наиболее многочисленны в миоцитах матки при беременности, содержание липидов особенно велико в васкулярных гладких миоцитах.
Синтетический аппарат гладких миоцитов представлен элементами грЭПС и комплексом Гольджи, лежащими у полюсов ядра,
- 445 -