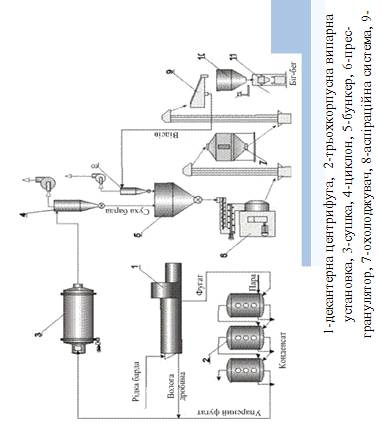
Материал: Утилізація відходів біотехнологічних виробництв
Аналізуючи переваги й недоліки анаеробного та аеробного процесів, можна зробити висновок: для очищення стічних вод молокопереробних підприємств малої потужності найбільш доцільна двоступенева схема з анаеробним очищенням на першому ступені та аеробним на другому.
Установки для анаеробного очищення стічних вод поділяються на біореактори з завислоседиментуючим біоценозом і біореактори з прикріпленим біоценозом, які, у свою чергу, можуть бути з рухомим та нерухомим завантаженням. Існують, також, комбіновані установки. Найбільш стійкі до коливань гідравлічного та органічного навантаження установки з прикріпленим біоценозом. Біореактори з нерухомим завантаженням мають простішу конструкцію, вони доступніші в експлуатації, ніж біореактори з рухомим завантаженням. Важлива проблема при використанні анаеробного методу очищення стічних вод - вибір температурного режиму та способу його підтримання. За сучасними даними швидкість анаеробного процесу зростає із збільшенням температури. Оптимальна температура для очищення стічних вод - 30-35°С, для чого потрібно додатково їх підігрівати, що не завжди можливо й доцільно.
Утилізація відходів харчових виробництв у світі
Аналіз патентних матеріалів за останні п'ять років показує, що в розвинених зарубіжних країнах ведеться інтенсивний пошук найбільш економічних і високоефективних способів очищення стічних вод харчових виробництв. Характерною рисою є поєднання класичних методів очищення (механічний, фізико-хімічний, біологічний і т.д.) з новими методами (зворотний осмос, ультрафільтрації, мікрофільтрація, електродіаліз тощо), з використанням мікроорганізмів (дріжджі, бактерії).
Це дозволяє одержати добрива, додаткове паливо (біогаз), а також кормовий протеїн з використанням спеціально підібраних для цієї мети продуцентів (США, Японія, Великобританія, Німеччина, Франція). У Японії очищають стічні води харчових виробництв з використанням також поверхнево активних речовин (ПАР), аніонообмінних смол, активної біомаси. У США очищають з застосування цеолітів, мембран, біотехнології.
За кордоном активно ведуться розробки по комплексному використанні сировини і безвідходній переробці утворених вторинних ресурсів із застосуванням мікробіологічної біотрансформації сировини, головним чином у напрямку збагачення його білком, що синтезуються бактеріями, дріжджами або грибами з метою отримання кормів, кормових і харчових добавок.
У Японії при виготовленні харчових продуктів використовують кістки риб, стебла конопель, шкірку цитрусових, висівки, макуху, спиртову барду і пивну дробину. При одержанні кормів і удобрення в Японії використовують панцирі креветок і крабів, рисове лушпиння, соєву макуху, барду і знежирені боби або залишки віджатого соєвого сиру "тофу".
У США при одержанні харчових продуктів використовують шкаралупу горіхів (мигдаль), цукрову мелясу, чайні залишки, макуху, залишки тіста і хліба, підсирної сироватку. Великобританія у виробництві продуктів харчування раціонально використовує лушпиння какао бобів та кормові білки з бурякового жому.
Проблема утилізації останнім часом
стає особливо актуальною закордоном, тому що велика кількість відходів,
вторинних матеріальних ресурсів створює не сприятливу обстановку в екологічному
відношенні.
Висновки
Діяльність будь-якого біотехнологічного виробництва може призвести до виникнення екологічних проблем загального і приватного характеру:
) виснаження і загибелі природних екосистем навколо біотехнологічних підприємств або неадекватного популяційному тиску одних видів живих істот на інші (наприклад, розростання ціанобактерій у водосховищах);
) зростанню стресових навантажень на людей, що проживають поблизу великих біотехнологічних підприємств (вихлопні гази, шум, випаровування, корпускулярні алергени в атмосфері та ін.);
) забруднення повітря, природних водойм грунтів біологічними та хімічними агентами, що використовуються в технологічному процесі і містяться у відходах виробництва.
Тому, екологічно безпечна схема біотехнологічного виробництва обов'язково повинна включати стадії ізоляції та знезараження твердих, рідких і газоподібних технологічних відходів.
Вибір системи знезараження й очищення - справа інженерного розрахунку з урахуванням економічної оцінки варіантів. Але головним критерієм завжди має бути відсутність ризиків для людини і навколишнього середовища.
І в даному випадку, держава повинна не тільки забезпечити
контроль над дотриманням нормативів з безпеки біотехнологічних виробництв, а й
централізовано покрити частину витрат на встановлення таких систем. Такого
підходу вимагають інтереси сучасного суспільства і майбутніх поколінь.
Список використаної літератури
1. Еліна Н.П. Основи біотехнології, СПб: Наука, 1995, 600 стор.
. Проект ФЗ "Про безпеку мікробіологічних і біотехнологічних виробництв та їх продукції", Москва
. Т.Ю. Жармухамедова, Т.А. Заргарова, Т.Ф. Горєлково, Т.А. Гуськова, А.Н. Мурашев. Роль служби забезпечення якості в проведенні досліджень з хімічної та біологічної безпеки відповідно до правил належної лабораторної практики. // Хімічна та біологічна безпека, 2008, №1-2
. ГОСТ Р 52249-2004 Правила виробництва і контролю якості лікарських засобів. Введено в дію 10 березня 2004
. Правила доклінічних досліджень безпечності та ефективності фармакологічних речовин (Правила якісної лабораторної практики в РФ - GLP або ПДИ). В кн. "Керівництво по експериментальному (доклінічного) вивчення нових фармакологічних речовин". Міністерство охорони здоров'я Російської Федерації, Департамент контролю якості, ефективності та безпеки лікарських засобів, Науковий центр експертизи та державного контролю лікарських засобів, Фармакологічний державний комітет. Москва, 2000.
.
Біотехнологія, під ред. Єгорова М.С., Самуїлова В.Д., у 8 кн., Кн.6:
Микробиологическое виробництво біологічно активних речовин та препаратів, М.:
"Вища школа", 1987, 143 стор.
Додаток