Материал: Усовершенствованное антиадгезионное покрытие
Часто полагают, что движущей силой диффузии является градиент концентрации. Однако перемещение, вызванное градиентом концентрации и приводящее к постепенной гомогенизации системы, не исчерпывает все возможные проявления этого сложного процесса. Весьма часто при диффузии происходит не выравнивание концентраций, а наоборот, дальнейшее разделение компонентов системы. Поэтому более правильно считать, что движущей силой диффузии является разность термодинамических потенциалов. Выравнивание термодинамических потенциалов и приближение к термодинамическому равновесию достигается за счет теплового движения атомов (молекул) [9].
В основу молекулярно-кинетической диффузии в полимерах положены представления о тепловых флуктуациях в жидкостях. Молекулы диффундирующего вещества передвигаются в конденсированном теле отдельными импульсами через «дырки» ̶ микрополости, которые возникают в результате тепловых флуктуаций кинетических единиц, атомов и молекул в массе конденсированного тела в непосредственной близости от диффундирующей молекулы [8].
Диффузионные и адсорбционные процессы это следствие контакта двух тел и вне контакта не могут, проявлятся [9].
1.3.3 Химическая теория адгезии
В ряде случаев высокая адгезия может быть обусловлена возникновением химических связей между молекулами адгезива и субстрата, например при склеивании латунной поверхности с каучуком. В присутствии серы происходит химическое соединение меди с нею и с каучуком. Химические связи возникают и при склеивании изоцианатами каучуков с металлами [9].
Видимо, когда адгезив вулканизуется или структурируется после образования контакта между ним и субстратом, образуются химические связи между молекулами адгезива и субстрата. Так, отмечено возникновение химических связей между металлами и клеями на основе аминов, отверждаемых эпоксидными смолами. Имеются сведения о возникновении химических связей между гидроксильными группами макромолекул целлюлозы и метилольными группами мочевиноформальдегидных и фенолформальдегидных смол [9].
Возникновение химических связей эффективно повышает адгезию, поэтому следует использовать подобные сочетания адгезивов и субстратов [9].
1.3.4 Электрическая теория адгезии
Из электрической теории адгезии следует, что субстрат, разделенный прослойкой адгезива, представляет собой конденсатор, разъединению обкладок которого препятствуют электрические силы. В темноте при отрыве пленки из каучука, нитроцеллюлозы и др. материалов от стекла, металла и других поверхностей можно наблюдать разряды, сопровождаемые свечением и легким треском. Исследования показали, что после отрыва поверхность каучука заряжается отрицательно, а поверхности стекла и металлаположительно. Единственным объяснением, согласующимся со всеми экспериментальными данными, является следующее. Поверхности на границе раздела фаз, образовавшиеся при отрыве пленки, наэлектризованы противоположными зарядами в силу разделения друг от друга обкладок молекулярного электрического двойного слоя [10].
Сцепление между адгезивом и подложкой образуется за счет силы
электрического притяжения, работающей в двойном электрическом слое. Энергия
отрыва (Ge) зависит от потенциала
разряда (Ve) следующим образом:
![]() (1.4)
(1.4)
где h ̶ расстояние, на котором происходит разряд,м;
![]() ̶ электрическая постоянная,
̶ электрическая постоянная,![]() .
.
1.4 Смачивание
.4.1 Краевой угол
Краевым углом (углом смачивания) обозначается угол, который образует капля жидкости на поверхности твердого вещества к данной поверхности. Размер краевого угла между жидкостью и твердым веществом зависит от взаимодействия между веществами на контактной поверхности. Смачивание является критерием адгезии для жидкостей [14].
На рисунке 1.1 рассмотрим равновесие в системе, в которой капля жидкости
помещена на твёрдую поверхность.
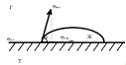
Рисунок 1.1 ̶ Теория смачивания [14]
Краевой угол q измеряется в сторону более полярной фазы (в данном случае в сторону воды). Обозначение sТ-Г показывает поверхностное натяжение между твердым телом и газовой фазой, sТ-Ж показывает поверхностное натяжение между твердым телом и жидкой фазой, а sЖ-Г показывает поверхностное натяжение между жидкой и газовой фазой [14].
Для измерения краевого угла необходимо провести касательную через 3 фазы (жидкость, газ, твердое тело). Угол между касательной и твердой фазой называют cos q, краевым углом смачивания. Угол q находится по таблице Брадиса [14].
Для состояния равновесия можно записать следующее условие:
![]() (1.5)
(1.5)
При проецировании на ось Х получим выражение:
![]() (1.6)
(1.6)
Из предыдущего выражения можно выделить cos q и получится уравнение Юнга.
![]() (1.7)
(1.7)
где q ̶ краевой угол смачивания, значение которого характеризует взаимодействие в системе Т-Г-Ж;q ̶ смачивание.
Если sТ-Г > sТ-Ж, то 0 < cos q < 1, из чего следует, что угол q - острый (наступающий), а поверхность ̶ гидрофильная. Если s Т-Г > s Т-Ж, то 1 < cos q < 0, из чего следует, что угол q - тупой (отступающий), а поверхность ̶ гидрофобная [14].
В зависимости от угла q различают следующие типы реализации явления смачивания:
а) Смачивание 0°˂ q ˂90° или 1˂ cos q ˂0.
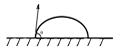
Рисунок 1.2 ̶ Схема смачивание от 0° до 90°
б) Полное смачивание (растекание) q ≈ 0° или cos q ≈ 1.
![]()
Рисунок 1.3 ̶ Схема полное смачивание ≈0°
в) Инверсия смачивания q = 90° или cos q = 0.
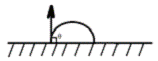
Рисунок 1.4 ̶ Схема инверсия смачивания
г) Не смачивание или 0 ˂ cos q ˂ -1.
![]()
Рисунок 1.5 ̶ Схема не смачивания
д) Полное не смачивание q =180° или cos q = -1.
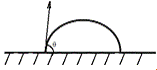
Рисунок 1.6 ̶ Схема полного не смачивания
Существуют также переходные поверхности (амфотерные), которые хорошо смачиваются как полярными, так и неполярными системами [14].
К гидрофильным поверхностям относятся силикаты, карбонаты, окислы железа. К гидрофобным поверхностям ̶ парафины, жиры, воск, чистые металлы [14].
Краевой угол смачивания зависит от строения поверхности, адсорбции жидкостей и газов, наличия ПАВ, температуры, давления, электрического заряда [14].
Изменение характера поверхности может быть реализовано при адсорбции на ней молекул ПАВ [14].
Различие во взаимодействии твердого тела с жидкостью и газом находит
применение в выделении взвешенных веществ из суспензий методом флотации.
Например, при культивировании микроорганизмов для получения кормового белка для
выделения клеток из культуральной жидкости суспензию подвергают барботированию
воздухом. Вследствие гидрофобности поверхности клетки «прилипают» к пузырькам
воздуха и всплывают на поверхность. Схему флотации рассмотрим на рисунке 1.7.

Рисунок 1.7 - Схема выделения веществ методом флотации [14]
Данный метод можно использовать после фильтрации взвешенных
мелкодисперсных веществ.
1.4.2 Работа адгезии и когезии
Равновесие в трехфазной системе определяется балансом сил взаимодействия молекул внутри каждой фазы и сил взаимодействия поверхностных молекул двух фаз между собой, т.е. явлениями когезии и адгезии соовтетственно. Прочность данных взаимодействий оценивают количеством энергии, необходимой для их разрыва, т.е. работой когезии и адгезии [11].
Для расчета работы адгезии используют уравнение Дюпре:
![]() (1.8)
(1.8)
Рассмотрим техническую схему выполнения работы адгезии по уравнению.
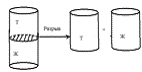
Рисунок 1.8 ̶ Схема выполнения работы адгезии [14]
Для расчета работы когезии используют уравнением Дюпре:
![]() (1.9)
(1.9)
Рассмотрим техническую схему выполнения работы когезии по уравнению.
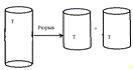
Рисунок 1.9 ̶ Схема выполнения работы когезии [14]
Для отрыва адгезива от субстрата должно соблюдаться условие - работа когезии должна быть выше работы адгезии, и тогда разрыв произойдёт между жидкой и твердой фазой. Если работа когезии ниже, чем работа адгезии, то разрыв произойдёт внутри фаз (жидкая или твёрдая) [11].
Используя уравнение Юнга, качественно оценим влияние когезии и адгезии на
равновесие в трехфазной системе.
![]() (1.10)
(1.10)
![]() (1.11)
(1.11)
Используя соотношение, мы получим уравнение Дюпре-Юнга:
![]() (1.12)
(1.12)
![]() (1.13)
(1.13)
![]() (1.14)
(1.14)
Таким образом, при смачивании если 0˂ cosq ˂1 и следовательно есть
следующая зависимость:
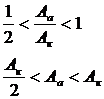
При не смачивании, должно выполнятся условие -1˂ cosq ˂0 то,
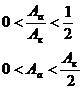 .
.
Следовательно, переход от несмачивания к смачиванию обеспечивается
снижением ![]() и увеличением
и увеличением ![]() .
.
Следует, что при смачивании свободная энергия единицы поверхности твёрдого тела уменьшается на величину sТ-Г×cosq, которую принято называть натяжением смачивания [9].
Работа когезии Ак характеризует энергетические изменения поверхностей раздела при взаимодействии частиц одной фазы [9].
Из уравнения следует, что на отрыв жидкости от поверхности твёрдого тела при полном смачивании (когда cos q = 0) затрачивается работа, необходимая для образования двух жидких поверхностей ̶ 2×sж-г.
Это значит, что при полном смачивании жидкость не отрывается от поверхности твёрдого тела, а происходит разрыв самой жидкости, т.е. при полном смачивании s ж-г £ sж-т.
Подставив в уравнение Юнга значения работ адгезии и когезии, получим:
![]() (1.15)
(1.15)
Из уравнения 15 следует, что смачиваемость жидкостью твёрдого тела тем лучше, чем меньше работа когезии и поверхностное натяжение жидкости на границе с газом [8].
Для характеристики смачивающих свойств жидкости используют также
относительную работу адгезии:
![]() (1.16)
(1.16)
где z ̶ характеристика смачивания
жидкости.
1.5 Светопропускание оксидов металла. Оптическая плотность
Свет или оптическое излучение представляет собой волны электромагнитного поля. Световые волны являются плоскопоперечными, они распространяются перпендикулярно направлению электрического и магнитного полей [13].
Различают следующие спектральные области оптического излучения: инфракрасная ̶ от 750 до 2500 нм, видимая ̶ от 400 до 750 нм и ультрафиолетовая - от 2 до 400 нм [13].
Известно, что при пропускании света через слой вещества его интенсивность уменьшается. Уменьшение интенсивности является следствием взаимодействия световой волны с электронами вещества, в результате которого часть световой энергии передается электронам. Это явление называется поглощением света [13].
Взаимодействие света с веществом описывается рядом законов, основными из которых являются:
.Закон Гротгуса-Дрейпера. Химически активным является излучение с такими длинами волн, которые поглощаются веществом [13].
.Закон Вант -Гоффа. Количество химически модифицированного светом вещества прямо пропорционально количеству поглощенной веществом энергии света [13].
.Закон Бугера -Ламберта-Бера (объединенный закон светопоглощения) для
монохроматического света. Интенсивность света, прошедшего через слой вещества (I),
и интенсивность света, падающего на него (I0), связаны
соотношением:
![]() (1.17)
(1.17)
где e×λ ̶ молярный коэффициент поглощения (экстинкции) при длине волны l, л/моль×см;
с - концентрация вещества, моль/л;
l - длина оптического пути или толщина слоя вещества, см.
Молярный коэффициент экстинкции характеризует способность молекул вещества поглощать свет определенной длины волны и определяется структурными особенностями молекул данного вещества [13].
Объединенный (основной) закон светопоглощения базируется на законе Бугера-Ламберта (первый закон светопоглощения), который определяет ослабление интенсивности светового потока в зависимости от толщины поглощающего слоя, и законе Бера (второй закон светопоглощения), описывающем зависимость светопоглощения от концентрации анализируемого раствора. Закон Бугера-Ламберта-Бера выполняется не всегда. Он выведен для достаточно разбавленных растворов при использовании монохроматического света [13].
Для характеристики поглощающей способности вещества используют такие величины, как оптическая плотность, светопропускание и светопоглощение [13].
Оптическая плотность (D) - это десятичный логарифм отношения
интенсивности света, падающего на образец, к интенсивности света, выходящего из
образца (I):
![]() (1.18)
(1.18)
Оптическая плотность является безразмерной величиной [13].
Светопропускание (коэффициент пропускания) (t) - отношение интенсивности света,
вышедшего из образца, к интенсивности света, падающего на него:
![]() ,
,
Значения t могут меняться от 0 (весь свет поглощается) до 1 (весь свет проходит). Величину t обычно выражают в процентах.
Иногда вместо t
используют cветопоглощение (коэффициент
поглощения) - величина, равная 1-t [13].