Материал: Тесты_ч_1
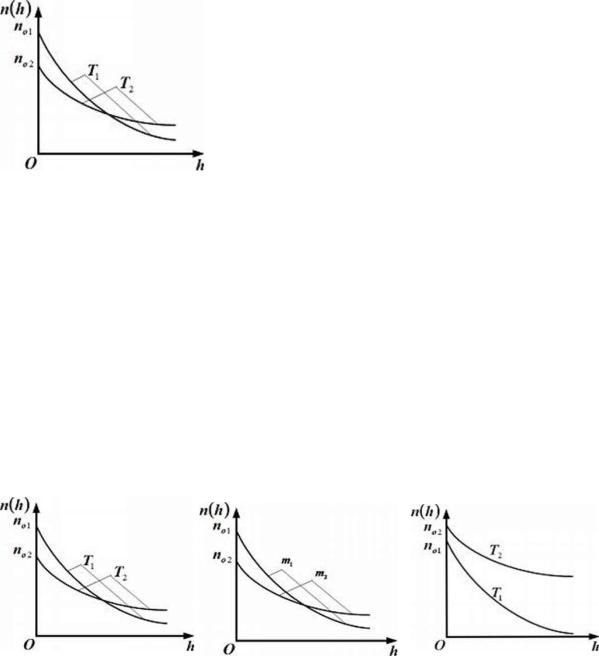
7.9. На рисунке представлены графики зависимости концентрации молекул идеального газа от высоты над уровнем моря для двух разных температур Т1 и T2 (распределение Больцмана). Для графиков этих функций верными являются утверждения (укажите не менее двух ответов), что…
1)температура Т2 выше температуры Т1;
2)концентрация молекул на «нулевом уровне» (h = 0), с повышением температуры уменьшается;
3)температура Т2 ниже температуры Т1;
4)с понижением температуры молекулы более равномерно распределяются по высоте.)
7.10. Формула |
|
|
m0 gh |
описывает распределение моле- |
|
n(h) n0 exp |
|
|
|
||
|
|||||
|
|
|
kT |
|
|
кул массой m0 по высоте в изотермической атмосфере; здесь n0 – концентрация молекул при h = 0, n – их концентрация на высоте h. Для этой зависимости справедливы следующие утверждения...
(укажите не менее двух ответов)
а |
б |
в |
1)приведенные на рисунке а кривые соответствуют распределениям для одного и того же газа при разных температурах,
причем T2 > Т1;
2)приведенные на рисунке б кривые соответствуют распределениям для двух разных газов при одинаковой температуре,
причем m1 < m2;
3)приведенные на рисунке б кривые соответствуют распределениям для двух разных газов при одинаковой температуре,
причем m1 > m2;
4)приведенные на рисунке в кривые соответствуют распределениям для одного и того же газа при разных температурах,
причем T2 < Т1.
60

7.11. Зависимости давления Р идеального газа во внешнем однородном поле силы тяжести от высоты h для двух разных температур представлены на рисунке. Для этих функций верными являются утверждения (укажите не менее двух ответов), что...
1) зависимость давления идеального газа от высоты определяется не только температурой газа, но и массой молекул;
2)температура Т1 ниже температуры Т2;
3)давление газа на высоте h равно давлению на «нулевом уровне» (h = 0), если температура газа стремится к абсолютному нулю;
4)температура Т1 выше температуры Т2.
7.12.Зависимости давления Р идеального газа во внешнем однородном поле силы тяжести от высоты h для двух разных температур представлены на рисунке предыдущего теста. Для этих функций неверными являются утверждения (укажите не менее двух ответов), что...
1)зависимость давления идеального газа от высоты определяется не только температурой, но и массой молекул;
2)температура Т1 ниже температуры Т2;
3)давление газа на высоте h равно давлению на «нулевом уровне» (h = 0), если температура газа стремится к абсолютному нулю;
4)температура Т1 выше температуры Т2.
7.13.На рисунке представлены графики за-
висимости концентрации молекул идеального газа от высоты над уровнем моря для двух разных газов. Для графиков этих функций верными являются утверждения (укажите не менее двух ответов), что…
1)масса m1 больше массы m2;
2)концентрация молекул газа с меньшей массой на «нулевом уровне» (h = 0) меньше;
3)масса m1 меньше массы m2;
4)концентрация молекул газа с меньшей массой на «нулевом уровне» (h = 0) больше.
61
8.Внутренняя энергия и теплоемкость газов
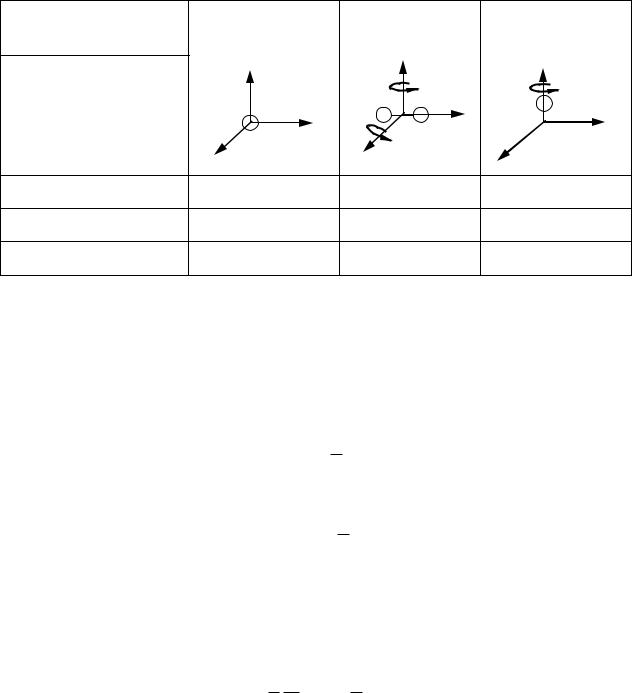
Число степеней свободы – число независимых величин, полностью определяющих положение системы в пространстве.
Число степеней |
Одноатомный |
Двухатомный |
Многоатомный |
свободы, i |
газ |
газ |
газ |
|
y |
y |
y |
|
|
|
|
|
х |
х |
х |
|
z |
||
|
z |
z |
|
|
|
|
|
Поступательные |
3 |
3 |
3 |
Вращательные |
0 |
2 |
3 |
Всего |
3 |
5 |
6 |
В реальных молекулах жѐсткой связи между атомами не существует, поэтому необходимо учитывать также степени свободы колебательного движения.
Среднее значение кинетической энергии поступательного движения одной молекулы:
0 32 kT .
Cредняя энергия одной многоатомной молекулы:
U0 2i kT ,
i iпост iвращ 2iколеб – сумма числа поступательных, вращательных и удвоенного числа колебательных степеней свободы молекулы.
Внутренняя энергия произвольной массы газа:
U 2i m RT 2i RT .
62

Теплоѐмкость газов:
CQ . dT
Удельная теплоѐмкость: |
|
|
c уд |
Q |
. |
|
||
|
dT m |
|
Молярная теплоѐмкость: |
|
|
C Q . dT
Связь удельной и молярной теплоѐмкостей:
Сμ = суд·μ.
Теплоемкости при изопроцессах
|
Изохориче- |
Изобариче- |
|
Адиаба- |
Изотерми- |
|||||||||||||||||
|
|
ский |
|
|
|
ский |
|
|
тический |
ческий |
||||||||||||
|
V = const |
Р = const |
|
|
Q = 0 |
Т = const |
||||||||||||||||
Молярная |
CV |
|
i |
|
|
R |
CP |
|
i 2 |
R |
0 |
CT |
|
|||||||||
|
2 |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|||
Удельная |
cуд |
|
i R |
уд |
|
(i 2) |
|
R |
0 |
сT |
|
|||||||||||
|
|
|
|
|
|
|
|
|
сV |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
2 |
2 |
|
|
|
|
|||||||||||||||
|
V |
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Уравнение Майера: |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
C р |
C R . |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V |
|
|
|
|
|
|
Показатель адиабаты (коэффициент Пуассона): |
|
|
||||||||||||||||||||
|
|
|
CP |
|
i 2 |
. |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
CV |
i |
|
|
|
|
|
|
|
Р |
|
|
|||||||
|
Адиабатический процесс – процесс, проте- |
Адиабата |
|
||
|
кающий без теплообмена с окружающей сре- |
Изотерма |
|
дой, δQ = 0. |
|
|
|
Уравнения адиабаты (уравнения Пуассона):
|
|
|
|
γ 1 |
|
|
|
γ 1 |
V |
|
T2 |
|
|
P2 |
|
γ |
|||
|
|
||||||||
|
|
V1 |
|
|
|
|
|
||
|
|
|
|
|
|||||
|
T |
V |
|
|
P |
|
|
const |
|
1 |
2 |
|
|
1 |
|
|
|
||
63

Тестовые задания
8.1. Для атомарного водорода (Н) число степеней свободы i равно…
1) 7; |
2) 1; |
3) 5; |
4) 3. |
8.2. Максимальное число вращательных степеней свободы молекулы азота N2 равно…
1) 5; |
2) 4; |
3) 3; |
4) 2. |
8.3. Для водяного пара (Н 2 О ) число степеней свободы i равно…
1) 6; |
2) 1; |
3) 5; |
4) 3. |
8.4. Средняя кинетическая энергия молекулы идеального газа при температуре T равна 2i kT . Здесь i = nпост + nвр,+2 nкол,, где nпост,
nвр, nкол, – число степеней свободы поступательного, вращательного и колебательного движений молекулы. Для гелия (Не) число i равно…
1) 7; |
2) 1; |
3) 5; |
4) 3. |
8.5. На каждую степень свободы движения молекулы приходится одинаковая энергия, равная 12 kT . При условии, что имеют место
все виды движения, средняя кинетическая энергия молекулы азота (N2) равна…
1) |
5 |
kT ; |
2) |
7 |
kT ; |
3) |
3 |
kT ; |
4) 3kT. |
|
2 |
2 |
2 |
||||||||
|
|
|
|
|
|
|
8.6. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. Средняя кинетическая энергия молекул кислорода (О2) (без учета колебательного движения) равна…
1) |
5 |
kT ; |
2) |
7 |
kT ; |
3) |
1 |
kT ; |
4) |
3 |
kT . |
|
2 |
2 |
2 |
2 |
|||||||||
|
|
|
|
|
|
|
|
64