Материал: Теории растворов. Закон Рауля и Генри
б) Определение g2 по тангенсу угла наклона касательной.
Экспериментальным путем определяют экстенсивное свойство раствора при различном числе молей растворенного вещества (n2) в одном и том же количестве растворителя при постоянной температуре и давлении строят графическую зависимость g=f(n2).
Для определения ![]() проводят
касательную в точке с (при n2=n2´) к кривой,
выражающей зависимость g=f(n2). В
растворе, содержащем n2´ моль растворенного вещества
проводят
касательную в точке с (при n2=n2´) к кривой,
выражающей зависимость g=f(n2). В
растворе, содержащем n2´ моль растворенного вещества ![]() = tgα.
= tgα.
в) Определение парциальной молярной величины
одного компонента по известным значениям парциальных молярных величин второго
компонента. Согласно уравнению
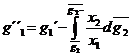
Значение интеграла находят из
графика, построенного в координатах
![]()
Площадь заштрихованной фигуры дает
величину интеграла
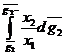
.6 ЗАКОН РАУЛЯ. ИДЕАЛЬНЫЕ РАСТВОРЫ. ПРЕДЕЛЬНО
РАЗБАВЛЕННЫЕ РАСТВОРЫ
Закон Рауля: Парциальные давления
пара Рi ,
компонента идеального раствора равно произведению давления пара чистого
компонента ![]() на его
мольную долю
на его
мольную долю ![]() в растворе
т.е
в растворе
т.е
![]() ;
; ![]()
В простейшем случае зависимость
парциального давления пара растворителя от состава бинарного раствора имеет
следующий вид:
![]()
Это уравнение можно придать и иной
вид:
![]()
Уравнения и являются выражениями закона Рауля(1886).
Обычно при повышении температуры
(пока давление насыщенного пара относительно невелико) отклонение от закона
Рауля по форме уменьшаются. Но при достаточно высоких температурах, когда
давление насыщенного пара раствора очень велико уравнение становится неточным,
так как возрастают отклонения пара от закона идеальных газов. В этих условиях
термодинамические свойства газов целесообразно связывать не с давлением, а с
летучестями fi , и
соответственно, закон Рауля выражать в форме уравнения
![]() (6.4а)
(6.4а)
аналогичного уравнению
Растворы, следующие по закону Рауля в форме уравнения (6.4а) при всех концентрациях и всех температурах, называют идеальными растворами, они являются предельными, простейшим типом жидких растворов[3].
Раствор, образование которого из компонентов, взятых в одинаковом агрегатном состоянии в любых соотношениях, не сопровождается тепловым эффектом и изменением объема, а изменение энтропии равно изменению энтропии при смешении идеальных газов. Такой раствор тоже можно считать идеальным[2].
Легко показать, что если для пара растворителя
соблюдается уравнение (6.4а), то должно соблюдаться аналогичное уравнение для
пара второго, растворенного компонента. Из уравнения (6.4а) получаем:
![]()
Представим уравнение Гиббса - Дюгема
![]()
в виде:
![]()
Преобразовав его правую часть путем
подстановки значения ![]() из
уравнения (5.4а) и соответствующего выражения для d
из
уравнения (5.4а) и соответствующего выражения для d![]() :
:
![]()
![]()
![]()
![]()
Если уравнение (5.4а) справедливо
для всех концентраций (идеальный раствор), то уравнение , также справедливо для
всех концентраций. При х=1, очевидно, ![]() и, следовательно
и, следовательно
![]()
При невысоких температурах, когда
парциальные давления компонентов невелики и летучести компонентов достаточно
близки к их парциальным давлениям, возвращаемся к выражениями для первого
компонента (закон Рауля) , а уравнение приобретает вид:
![]() (6.10)
(6.10)
Закон Генри: при постоянной
температуре раствор данного газа в данном растворителе прямо пропорционально
давлению этого газа над раствором.
![]()
где С -молярные концентрации газа в растворителе
р -парциальное давление газа под раствором
к- величина называется коэффициентом Генри.
Уравнение (6.10) выражает закон Генри: парциальное давление пара растворенного вещества пропорционально его мольной доле. Закон Генри был найден опытным путем для растворов газов в жидкостях(1803) [4].
Предельно разбавленные растворы. Раствор, в котором концентрация растворенного вещества мала[1].
В предельно разбавленных растворах для растворенного вещества справедлив закон Генри, который был установлен опытным путем на основании данных о растворимости газов в жидкостях. Уравнение Генри можно получить на основании термодинамических положений.
Согласно второму уравнению Гиббса -Дюгема, для бинарного раствора
![]()
С учетом (8.101) уравнение принимает вид
Величина
![]() (8.101)
(8.101)
называется химическим потенциалом
индивидуального i-ого вещества в газовой смеси, а
величина ![]() -
стандартным химическим потенциалом.
-
стандартным химическим потенциалом.
![]()
отсюда
Из закона Рауля
![]()
Следует ,что
![]()
При поставке и в получаем
![]()
При поставке и в получаем
![]()
После интегрирования находим
![]()
где lnK -постоянная интегрирования.
Отсюда
![]()
![]()
где Г=КР -постоянная Генри (Р0= 1,0133*105 Па).
Уравнение и представляет собой закон
Генри. Для идеальных растворов ![]() и уравнение
и уравнение ![]() принимает
вид
принимает
вид
![]()
Для неидеальных растворов, включая
предельно разбавленные, постоянная Генри ![]() . Постоянная Генри для неидеальных
растворов определяется из опытных данных по давлению пара Р2=f(x2) в
соответствие с условием
. Постоянная Генри для неидеальных
растворов определяется из опытных данных по давлению пара Р2=f(x2) в
соответствие с условием
![]() [1].
[1].
1.7 РЕАЛЬНЫЕ РАСТВОРЫ. ПОЛОЖИТЕЛЬНЫЕ
И ОТРИЦАТЕЛЬНЫЕ ОТКЛОНЕНИЯ ОТ ЗАКОНА РАУЛЯ. ДИАГРАММЫ КИПЕНИЯ
Все растворы, которые не подчиняются термодинамическим закономерностям идеальных и предельно разбавленных растворов, объединяются под общим названием - неидеальные (реальные ) растворы [5].
Среди неидеальных растворов выделяют регулярные и атермальные растворы.
Регулярные растворы -это те растворы у которых при смешивание компонентов, взятых в одинаковом агрегатном состоянии, изменение энтальпии и объема не равны нулю, но изменение энтропии такое же, как при смешение идеальных газов.
Атермальные растворы - это реальные растворы, теплота образования которых равна нулю [2].
Реальные растворы в подавляющем большинстве не подчиняются законам идеальных растворов. Очень многие из них не подчиняются, например закону Рауля, причем известны как положительные , так и отрицательные отклонения от этого закона. Если давления пара над реальным раствором больше ,чем над идеальным раствором такого же состава, отклонение от закона Рауля называют положительными, а если меньше -отрицательными. У растворов, образованных летучими компонентами, отклонения называют положительными, если общее давления пара больше аддитивной величины, и отрицательными - если оно меньше. Знак и величина отклонения зависят от природы растворителя и растворенного вещества.
Отклонения от идеальности обусловлены как физическими, так и химическими причинами (дипольные взаимодействия, поляризация, образование водородных связей, ассоциация, диссоциация, сольватация) [1]
Для изучения равновесия пар - жидкий раствор применяют два типа диаграмм состояния: 1)диаграммы давление пара -состав, при Т=const; 2) диаграммы температура кипения - состав, при р=const.
На практике чаще используют диаграммы состояния
Т - состав, называемыми диаграммами кипения. На этих диаграммах есть
фигуративные(выражающие состав двух равновесных фаз) точки, отображающие
температуры кипения чистых компонентов при данном внешнем давлении. Каждая
диаграмма имеет две кривые, разделяющие диаграмму на три области: область пара
,область жидкости, область равновесия пара и жидкости [4]
.8 АЗЕОТРОПНЫЕ СМЕСИ. ЗАКОНЫ ГИББСА -
КОНОВАЛОВА. ЗАКОНЫ ВРЕВСКОГО
Азеотропные смеси. Реальные растворы
со значительным отклонением от идеальности либо положительным, либо
отрицательным способны образовывать азеотропные смеси (азеотропы). Азеотропы -
это растворы при испарение которых получается пар того же состава, что и исходная
жидкость (![]() ). Это
условно инвариантные системы (Сусл=2-2=0)
). Это
условно инвариантные системы (Сусл=2-2=0)
Для идеальных и реальных растворов справедлив первый и второй законы Гиббса-Коновалова:
Первый закон Гиббса - Коновалова: пар по сравнению с жидким раствором, из которого он был получен, при равновесии богаче тем компонентом, прибавление которого к раствору приводит к понижению температуры кипения раствора при заданном внешнем давлении или к повышению давления пара над раствором.
Второй закон Гиббса - Коновалова: в азеотропных смесях диаграмм состояния экстремальные точки (максимум и минимум) составы жидкости и пара совпадают [1].
Основные закономерности влияния температуры на состав пара, равновесного с летучей смесью, вытекают из основных термодинамических соотношений для летучих смесей и называются законами Вревского.
Первый закон Вревского:
При повышении температуры пар, находящийся в равновесии с летучей смесью постоянного (заданного) состава, обогащается тем компонентом, парциальная молярная теплота испарения которого больше. Эта закономерность справедлива для летучих смесей как без азеотропа, так и с азеотропом.
Второй закон Вревского: В системах с максимумом на кривой давления пара при повышении температуры в азеотропной смеси возрастает относительное содержание компонента с большей парциальной молярной теплотой испарения, а в летучей смеси с минимумом на кривой давления пара изменение относительного содержания компонента обратное.
Третий закон Вревского:
При повышение температуры в системах с максимумом на кривой давления пара состав пара ,находящегося в равновесии с данной летучей смесью, и состав азеотропной смеси изменяются в одном направление. Третий закон является следствием первого и второго закона.
Законы Вревского могут быть сформулированы также для зависимости температуры кипения от состава [2].
2 ПРАКТИЧЕСКАЯ ЧАСТЬ
Выполнить задание:
На основание данных о составах жидкой «X» и паровой «Y» фаз в мольных процентах вещества А, находящихся в равновесии при температуре Т и общем давление Р(см. табл.1):
1. Постройте диаграмму кипения системы А-В при Р= const.
. Обозначьте буквами на диаграмме области существования : систем в парообразном состоянии «С», систем в жидком состояние «Е», систем в гетерогенном состояние «F». Обозначьте точки сосуществования фаз одинакового состава «G».
. Определите температуру начала и конца кипения системы D (табл.1),состав которой будет равен d молярных % вещества А (табл.2).
. Определите в молярных % состав жидкой фазы системы D, находящейся в равновесии с паровой фазой при температуре Т1.
. Определите состав в молярных % паровой фазы системы D, находящейся в равновесии с жидкой фазой при температуре Т1.
. Определите отношение числа молей жидкой фазы к числу молей паровой фазы системы D, находящейся в равновесии при температуре Т1.
. Определите количество молей веществ А и В, содержащихся в 1 кг системы D.
. Определите количество молей веществ А, содержащихся в 1 кг системы D.
. Определите количество молей веществ В, содержащихся в 1 кг системы D [3].
Таблица 1
|
№ варианта |
Система D |
P∙10-4 H/м2 |
Состав, мол.% |
T, K |
||||||||
|
|
|
|
X |
Y |
|
|||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
|||||||
|
6 |
А-H2O B-C3H7OH |
10,133 |
100,0 |
373,0 |
|
|||||||
|
|
|
|
99.0 |
89.0 |
368,0 |
|
||||||
|
|
|
|
98.0 |
78.4 |
365,0 |
|
||||||
|
|
|
|
96.0 |
68.0 |
363,5 |
|
||||||
|
|
|
|
94.0 |
64.9 |
362,3 |
|
||||||
|
|
|
|
90.0 |
62.8 |
361,5 |
|
||||||
|
|
|
|
80.0 |
60.8 |
361,1 |
|
||||||
|
|
|
|
70.0 |
59.6 |
360,9 |
|
||||||
|
|
|
|
60.0 |
57.6 |
360,8 |
|
||||||
|
|
|
|
50.0 |
54.8 |
360,9 |
|
||||||
|
|
|
|
40.0 |
50.8 |
361,3 |
|
||||||
|
|
|
|
30.0 |
44.9 |
362,0 |
|
||||||
|
|
|
|
20.0 |
35.9 |
363,5 |
|
||||||
|
|
|
|
15.0 |
29.6 |
364,5 |
|
||||||
|
|
|
|
10.0 |
22.2 |
365,8 |
|
||||||
|
|
|
|
4.0 |
10.0 |
367,0 |
|
||||||
|
|
|
|
0.0 |
0.0 |
370,3 |
|
||||||