Материал: Степень окисления. Влияние методов получения пленок SiO2 на их свойства
Степень окисления. Влияние методов получения пленок SiO2 на их свойства
Федеральное государственное образовательное учреждение высшего профессионального образования.
«НАЦИОНАЛЬНО-ИССЛЕДОВАТЕЛЬСКИЙ УНИВЕРСИТЕТ ИНФОРМАЦИОННЫХ ТЕХНОЛОГИЙ, МЕХАНИКИ И ОПТИКИ»
Факультет: «Компьютерные технологии и управления»
Специальность:
«Конструирования и технология электронных средств. Проектирования электронных
средств в защищенной интегрированной среде»
Реферат
По дисциплине: Микро-и нано технологии
На
тему: Степень окисления. Влияние методов получения пленок SiO2
на их свойства.
Выполнили: Рахмонова Манзура, Ёрова Ситора
Принял: Холецкий Р. А
Санкт-Петербург
2014
Содержание
Введение
Понятие и описание степень окисления
Получения пленок SiO2 методом термического окисления
Анализ влияния технологических параметров на процесс окисления кремния
Факторы, влияющие на скорость получения и качество пленок SiO2
Свойства пленок SiO2
Заключение
Список
литературы
Введение
Общим для диэлектрических пленок различного назначения является требование технологичности, под которой понимают, прежде всего, совместимость процессов получения покрытия с изготовлением структура ИМС в целом. Технологичными следует считать также процессы, осуществляемые при не высоких температурах нагрева пластины и обеспечивающие приемлемую для производства скорость роста пленки. Загрязнения пленки, ухудшающие электрические свойства, должны отсутствовать. Поэтому химическое и электрохимическое выращивание пленок в растворах и электролитах при производстве полупроводниковых ИМС находит ограниченное применение.
Эксплуатационным требованиям достаточно полно отвечает окись кремния, получаемая при нагревании его поверхности в присутствии кислорода (термическое окисление). Термически выращенный окисел SiO2 обладает наилучшими маскирующими свойствами и высокими электрическими параметрами. Склонность окиси кремния к стеклообразованию способствует к получению беспористо пленки. Хорошо растворяясь в плавиковой кислоте, SiO2 в то же время практически стабильна по отношению к смесям HF+HNO3 и другим реагентам, что позволяет эффективно использовать ее в качестве маски при селективном травлении кремния.
Процесс окисления выполняют в эпитаксиальных
установках или в одно зонных диффузионных печах со специальными
газораспределительными устройствами. Он хорошо согласуется с типовыми операциями
физико-термической обработки. На практике разгонку примеси при диффузии
совмещают с окислением поверхности дорожек. Окисление поверхности после
эпитаксии также выполняется на одной установке в едином цикле. При окислении
образуются химические связи между атомами кислорода, в результате чего
плотность поверхностных состояний уменьшается на несколько порядков по
сравнению с атомарно чистой поверхностью. Достаточно толстый переходный слой,
существующий на границе SiO2
и
Si, обуславливает
слабое изменение ТКР, что снижает внутренне натяжение и уменьшает коробление
пластин после их охлаждения.
Понятие и описание степень окисления
Степень окисления - вспомогательная условная величина для записи процессов окисления <https://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D0%B8%D1%81%D0%BB%D0%B5%D0%BD%D0%B8%D0%B5>, восстановления <https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D1%81%D1%81%D1%82%D0%B0%D0%BD%D0%BE%D0%B2%D0%BB%D0%B5%D0%BD%D0%B8%D0%B5> и окислительное - восстановительные реакций <https://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D0%B8%D1%81%D0%BB%D0%B8%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D0%BE-%D0%B2%D0%BE%D1%81%D1%81%D1%82%D0%B0%D0%BD%D0%BE%D0%B2%D0%B8%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D1%8B%D0%B5_%D1%80%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D0%B8>. Она указывает на состояние окисления отдельного атома <https://ru.wikipedia.org/wiki/%D0%90%D1%82%D0%BE%D0%BC> молекулы <https://ru.wikipedia.org/wiki/%D0%9C%D0%BE%D0%BB%D0%B5%D0%BA%D1%83%D0%BB%D0%B0> и представляет собой лишь удобный метод учёта переноса электронов <https://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D1%80%D0%B5%D0%BD%D0%BE%D1%81_%D1%8D%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BD%D0%B0>: она не является истинным зарядом <https://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D0%B7%D0%B0%D1%80%D1%8F%D0%B4> атома в молекуле.
Представления о степени окисления элементов положены в основу и используются при классификации химических веществ <https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D0%BD%D0%BE%D0%BC%D0%B5%D0%BD%D0%BA%D0%BB%D0%B0%D1%82%D1%83%D1%80%D0%B0>, описании их свойств, составлении формул <https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%84%D0%BE%D1%80%D0%BC%D1%83%D0%BB%D0%B0> соединений <https://ru.wikipedia.org/wiki/%D0%9D%D0%B5%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F> и их международных названий. Но особенно широко оно применяется при изучении окислительное-восстановительных реакций.
Понятие степень окисления часто используют в неорганической химии <https://ru.wikipedia.org/wiki/%D0%9D%D0%B5%D0%BE%D1%80%D0%B3%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%85%D0%B8%D0%BC%D0%B8%D1%8F> вместо понятия валентность <https://ru.wikipedia.org/wiki/%D0%92%D0%B0%D0%BB%D0%B5%D0%BD%D1%82%D0%BD%D0%BE%D1%81%D1%82%D1%8C>.
Степень окисления указывается сверху
над символом <https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D1%81%D0%B8%D0%BC%D0%B2%D0%BE%D0%BB>
элемента
<https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82>.
В отличие от указания заряда иона, при указании степени окисления первым
ставится знак, а потом численное значение, а не наоборот(при этом в формулах
почти всегда указывается заряд атома/иона, а в тексте - степень окисления +2,
+3…, отсюда и путаница; в формулах степень окисления пишут над элементом (знак
впереди - на первом месте), заряд для ионов [не для каждого элемента в сложных
ионах! - пишется верхним индексом - сверху справа после иона (знак позади
числа): ![]() - степень
окисления,
- степень
окисления, ![]() - заряды
(не совсем верное обозначение),
- заряды
(не совсем верное обозначение), ![]() - заряды (верное обозначение!).
- заряды (верное обозначение!).
Степень окисления [в отличие от
валентности] может иметь нулевое, отрицательное и положительное значения,
которые обычно ставятся над символом элемента сверху: ![]() Чтобы
облегчить обсуждение химии окислительное-восстановительных явлений, припишем
каждому атому в молекуле или комплексном ионе степень окисления согласно
следующим правилам: Степень окисления атома любого элемента в свободном
(несвязанном) состоянии (простое вещество
<https://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%BE%D1%81%D1%82%D0%BE%D0%B5_%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82%D0%B2%D0%BE>)
равна нулю <https://ru.wikipedia.org/wiki/0_(%D1%87%D0%B8%D1%81%D0%BB%D0%BE)>,
так, например, атомы в молекулах имеют нулевую степень окисления:
Чтобы
облегчить обсуждение химии окислительное-восстановительных явлений, припишем
каждому атому в молекуле или комплексном ионе степень окисления согласно
следующим правилам: Степень окисления атома любого элемента в свободном
(несвязанном) состоянии (простое вещество
<https://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%BE%D1%81%D1%82%D0%BE%D0%B5_%D0%B2%D0%B5%D1%89%D0%B5%D1%81%D1%82%D0%B2%D0%BE>)
равна нулю <https://ru.wikipedia.org/wiki/0_(%D1%87%D0%B8%D1%81%D0%BB%D0%BE)>,
так, например, атомы в молекулах имеют нулевую степень окисления: ![]()
· Степень окисления любого простого
одноатомного иона соответствует его заряду
<https://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D0%B7%D0%B0%D1%80%D1%8F%D0%B4>
или формальному заряду
<https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%80%D0%BC%D0%B0%D0%BB%D1%8C%D0%BD%D1%8B%D0%B9_%D0%B7%D0%B0%D1%80%D1%8F%D0%B4>
атома <https://ru.wikipedia.org/wiki/%D0%90%D1%82%D0%BE%D0%BC> в молекуле
<https://ru.wikipedia.org/wiki/%D0%9C%D0%BE%D0%BB%D0%B5%D0%BA%D1%83%D0%BB%D0%B0>
или в формульной единице
<https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%80%D0%BC%D1%83%D0%BB%D1%8C%D0%BD%D0%B0%D1%8F_%D0%B5%D0%B4%D0%B8%D0%BD%D0%B8%D1%86%D0%B0>,
например: Na+ = +1, Ca2+ = +2, Cl− = −1
![]()
· Степень окисления водорода в любом не ионном соединении равна +1. Это правило применимо к подавляющему большинству соединений водорода <https://ru.wikipedia.org/wiki/%D0%93%D0%B8%D0%B4%D1%80%D0%B8%D0%B4%D1%8B>, таких, как H2O, NH3 или CH4. Для ионных гидридов металлов, например NaH, степень окисления водорода −1.
· Степень окисления кислорода <https://ru.wikipedia.org/wiki/%D0%9A%D0%B8%D1%81%D0%BB%D0%BE%D1%80%D0%BE%D0%B4> равна −2 во всех соединениях, где кислород не образует простой ковалентной связи O-O, т.е. в подавляющем большинстве соединений - оксидах <https://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4%D1%8B>. Так, степень окисления кислорода равна −2 в H2O, H2SO4, NO, CO2 и CH3OH; но в пероксиде водорода, H2O2 (HO-OH), она равна −1 (другими исключениями из правила, согласно которому кислород имеет степень окисления −2, является OF2, где она +2 для кислорода и −1 для фтора; O2F2 = +1; OO2 <https://ru.wikipedia.org/wiki/%D0%9E%D0%B7%D0%BE%D0%BD> = +4 у центрального атома).
· В соединениях неметаллов, не включающих водород и кислород, неметалл с большей электро отрицательностью <https://ru.wikipedia.org/wiki/%D0%AD%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BE%D1%82%D1%80%D0%B8%D1%86%D0%B0%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D0%BE%D1%81%D1%82%D1%8C> считается отрицательно заряжённым. Степень окисления такого неметалла полагается равной заряду его наиболее распространенного отрицательного иона. Например, в CCl4 степень окисления хлора −1, а углерода +4. В CH4 степень окисления водорода +1, а углерода −4. В SF6 степень окисления фтора −1, а серы +6, но в CS2 степень окисления серы −2, а степень окисления углерода +4. В молекулах типа S4N4 <https://ru.wikipedia.org/wiki/%D0%A2%D0%B5%D1%82%D1%80%D0%B0%D0%BD%D0%B8%D1%82%D1%80%D0%B8%D0%B4_%D1%82%D0%B5%D1%82%D1%80%D0%B0%D1%81%D0%B5%D1%80%D1%8B> с ковалентными связями (где соединяющиеся атомы имеют близкие или совпадающие электро отрицательности) понятие степени окисления теряет смысл (см. Валентность <https://ru.wikipedia.org/wiki/%D0%92%D0%B0%D0%BB%D0%B5%D0%BD%D1%82%D0%BD%D0%BE%D1%81%D1%82%D1%8C>).
· Алгебраическая сумма
<https://ru.wikipedia.org/wiki/%D0%90%D0%BB%D0%B3%D0%B5%D0%B1%D1%80%D0%B0%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%81%D1%83%D0%BC%D0%BC%D0%B0>
степеней окисления всех атомов в формуле нейтрального соединения
<https://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%BE%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5>
всегда равна нулю:
![]()
![]()
· Алгебраическая сумма степеней окисления всех атомов в комплексном ионе (катионе либо анионе) должна быть равна его общему заряду (см. также выше 2-й пункт). Так, в ионе NH4+ степень окисления N должна быть равной −3 и, следовательно, −3 + 4 = +1. Поскольку в ионе SO42− сумма степеней окисления четырёх атомов кислорода равна −8, сера должна иметь степень окисления, равную +6, чтобы полный заряд иона оказался равным −2.
· В химических реакциях <https://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D0%B8%D1%81%D0%BB%D0%B8%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D0%BE-%D0%B2%D0%BE%D1%81%D1%81%D1%82%D0%B0%D0%BD%D0%BE%D0%B2%D0%B8%D1%82%D0%B5%D0%BB%D1%8C%D0%BD%D1%8B%D0%B5_%D1%80%D0%B5%D0%B0%D0%BA%D1%86%D0%B8%D0%B8> должно выполняться правило сохранения алгебраической суммы степеней окисления всех атомов. Именно это правило делает понятие степени окисления столь важным в современной химии. Если в ходе химической реакции степень окисления атома повышается, говорят, что он окисляется <https://ru.wikipedia.org/wiki/%D0%92%D0%BE%D1%81%D1%81%D1%82%D0%B0%D0%BD%D0%BE%D0%B2%D0%B8%D1%82%D0%B5%D0%BB%D1%8C>, если же степень окисления атома понижается, говорят, что он восстанавливается <https://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D0%B8%D1%81%D0%BB%D0%B8%D1%82%D0%B5%D0%BB%D1%8C>. В полном уравнении химической реакции окислительные и восстановительные процессы должны точно компенсировать друг друга.
· Максимальная положительная степень окисления элемента обычно численно совпадает с номером его группы <https://ru.wikipedia.org/wiki/%D0%93%D1%80%D1%83%D0%BF%D0%BF%D0%B0_%D0%BF%D0%B5%D1%80%D0%B8%D0%BE%D0%B4%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%BE%D0%B9_%D1%81%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D1%8B> в периодической системе (классического короткого варианта таблицы <https://ru.wikipedia.org/wiki/%D0%9A%D0%BE%D1%80%D0%BE%D1%82%D0%BA%D0%B0%D1%8F_%D1%84%D0%BE%D1%80%D0%BC%D0%B0_%D0%BF%D0%B5%D1%80%D0%B8%D0%BE%D0%B4%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%BE%D0%B9_%D1%81%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D1%8B_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82%D0%BE%D0%B2>). Максимальная отрицательная степень окисления элемента равна максимальной положительной степени окисления минус восемь (например. для халькогена <https://ru.wikipedia.org/wiki/%D0%A5%D0%B0%D0%BB%D1%8C%D0%BA%D0%BE%D0%B3%D0%B5%D0%BD> <https://ru.wikipedia.org/wiki/%D0%A1%D0%B5%D1%80%D0%B0> положительная степень окисления +6, макс. отрицательная 6 − 8 = −2).Исключение составляют фтор <https://ru.wikipedia.org/wiki/%D0%A4%D1%82%D0%BE%D1%80>, кислород <https://ru.wikipedia.org/wiki/%D0%9A%D0%B8%D1%81%D0%BB%D0%BE%D1%80%D0%BE%D0%B4>, благородные газы гелий <https://ru.wikipedia.org/wiki/%D0%93%D0%B5%D0%BB%D0%B8%D0%B9>, неон <https://ru.wikipedia.org/wiki/%D0%9D%D0%B5%D0%BE%D0%BD>, аргон <https://ru.wikipedia.org/wiki/%D0%90%D1%80%D0%B3%D0%BE%D0%BD>, а также железо <https://ru.wikipedia.org/wiki/%D0%96%D0%B5%D0%BB%D0%B5%D0%B7%D0%BE> и элементы подгрупп кобальта <https://ru.wikipedia.org/wiki/%D0%9F%D0%BE%D0%B4%D0%B3%D1%80%D1%83%D0%BF%D0%BF%D0%B0_%D0%BA%D0%BE%D0%B1%D0%B0%D0%BB%D1%8C%D1%82%D0%B0> и никеля <https://ru.wikipedia.org/wiki/%D0%9F%D0%BE%D0%B4%D0%B3%D1%80%D1%83%D0%BF%D0%BF%D0%B0_%D0%BD%D0%B8%D0%BA%D0%B5%D0%BB%D1%8F>: их высшая степень окисления выражается числом, значение которого ниже, чем номер группы, к которой они относятся. У элементов подгруппы меди <https://ru.wikipedia.org/wiki/%D0%9F%D0%BE%D0%B4%D0%B3%D1%80%D1%83%D0%BF%D0%BF%D0%B0_%D0%BC%D0%B5%D0%B4%D0%B8>, наоборот, высшая степень окисления больше единицы, хотя они и относятся к I группе. Правило о равенстве числу восемь <https://ru.wikipedia.org/wiki/%D0%9F%D1%80%D0%B0%D0%B2%D0%B8%D0%BB%D0%BE_%D0%BE%D0%BA%D1%82%D0%B5%D1%82%D0%B0> суммы степеней окисления элемента (R) по кислороду (RO) и по водороду (HR; т.е. положительных и отрицательных степеней окисления) соблюдается лишь для p-элементов <https://ru.wikipedia.org/wiki/P-%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82%D1%8B> IV - V - VI - VII групп таблицы ПСХЭ <https://ru.wikipedia.org/wiki/%D0%9F%D0%B5%D1%80%D0%B8%D0%BE%D0%B4%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B0%D1%8F_%D1%81%D0%B8%D1%81%D1%82%D0%B5%D0%BC%D0%B0_%D1%85%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D1%85_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82%D0%BE%D0%B2>
Понятие степени окисления вполне
применимо и для нестехиометрических соединений <https://ru.wikipedia.org/wiki/%D0%9D%D0%B5%D1%81%D1%82%D0%B5%D1%85%D0%B8%D0%BE%D0%BC%D0%B5%D1%82%D1%80%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D1%8F>
(КС8, Mo5Si3, Nb3B4 и др.).В некоторых случаях эта величина может быть выражена
и дробным числом: для железа в оксиде железа (II, III)
<https://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4_%D0%B6%D0%B5%D0%BB%D0%B5%D0%B7%D0%B0(II,III)>
Fe3O4 она равна +8/3. Дробные степени окисления не имеют
смысла при объяснении связи в химических соединениях, но они иногда могут быть
использованы для составления уравнений окислительно-восстановительных реакций.
К примеру, запишем схему процесса с указанием изменения степеней окисления
элементов:
![]()
Составляем электронные уравнения:
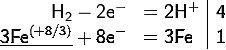
Найденные коэффициенты проставляем в
схему процесса, заменяя стрелку на знак равенства:
![]()
(то есть в электронных реакциях
(методе электронного баланса) железо с дробной степенью окисления записывается
только с коэффициентом 3).На самом деле, в растворе нет ионов Fe2+,
Fe3+ (и уж тем более Fe+8/3), также как и Cr6+,
Mn7+, S6+, а есть ионы CrO42−,
MnO4−, SO42−, а равно и
малодиссоциированные «электролиты» Fe3O4 (FeO•Fe2O3).
Именно поэтому следует отдать предпочтение методу полуреакций
(ионно-электронным методам) и применять его при составлении уравнении всех окислительно-восстановительных
реакций, протекающих в водных растворах. То есть мы можем воспользоваться
готовой реакцией стандартного электродного потенциала
<https://ru.wikipedia.org/wiki/%D0%A1%D1%82%D0%B0%D0%BD%D0%B4%D0%B0%D1%80%D1%82%D0%BD%D1%8B%D0%B9_%D1%8D%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%B4%D0%BD%D1%8B%D0%B9_%D0%BF%D0%BE%D1%82%D0%B5%D0%BD%D1%86%D0%B8%D0%B0%D0%BB>:
Fe3O4 + 8H+ + 8e− = 3Fe + 4H2O, E° = −0,085 В.
окисление пленка термический кремний
Условность степень окисления. Следует помнить, что степень окисления является сугубо условной величиной, не имеющей физического смысла, но характеризующей образование химической связи меж атомарного взаимодействия в молекуле.
Степень окисления в ряде случаев не совпадает с валентностью <https://ru.wikipedia.org/wiki/%D0%92%D0%B0%D0%BB%D0%B5%D0%BD%D1%82%D0%BD%D0%BE%D1%81%D1%82%D1%8C>. Например, в органических соединениях <https://ru.wikipedia.org/wiki/%D0%9E%D1%80%D0%B3%D0%B0%D0%BD%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%BE%D0%B5_%D1%81%D0%BE%D0%B5%D0%B4%D0%B8%D0%BD%D0%B5%D0%BD%D0%B8%D0%B5> углерод <https://ru.wikipedia.org/wiki/%D0%A3%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4> всегда четырёхвалентен, а [если предположить, что соединения ионы <https://ru.wikipedia.org/wiki/%D0%98%D0%BE%D0%BD%D0%BD%D0%B0%D1%8F_%D1%81%D0%B2%D1%8F%D0%B7%D1%8C>] степень окисления атома углерода в соединениях метана <https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D1%82%D0%B0%D0%BD> CH4, метилового спирта <https://ru.wikipedia.org/wiki/%D0%9C%D0%B5%D1%82%D0%B0%D0%BD%D0%BE%D0%BB> CH3OH, формальдегида <https://ru.wikipedia.org/wiki/%D0%A4%D0%BE%D1%80%D0%BC%D0%B0%D0%BB%D1%8C%D0%B4%D0%B5%D0%B3%D0%B8%D0%B4> HCOH, муравьиной кислоты <https://ru.wikipedia.org/wiki/%D0%9C%D1%83%D1%80%D0%B0%D0%B2%D1%8C%D0%B8%D0%BD%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0> HCOOH и диоксида углерода <https://ru.wikipedia.org/wiki/%D0%9E%D0%BA%D1%81%D0%B8%D0%B4_%D1%83%D0%B3%D0%BB%D0%B5%D1%80%D0%BE%D0%B4%D0%B0(IV)> CO2, соответственно, равна −4, −2, 0, +2 и +4.
Степень окисления зачастую не совпадает с фактическим числом электронов <https://ru.wikipedia.org/wiki/%D0%92%D0%B0%D0%BB%D0%B5%D0%BD%D1%82%D0%BD%D1%8B%D0%B5_%D1%8D%D0%BB%D0%B5%D0%BA%D1%82%D1%80%D0%BE%D0%BD%D1%8B>, которые участвуют в образовании связей <https://ru.wikipedia.org/wiki/%D0%9E%D0%B1%D1%80%D0%B0%D0%B7%D0%BE%D0%B2%D0%B0%D0%BD%D0%B8%D0%B5_%D1%81%D0%B2%D1%8F%D0%B7%D0%B8>. Обычно это молекулы с различными электрон дефицитными химическими связями и делокализацией электронной плотности. Например, в молекуле азотной кислоты <https://ru.wikipedia.org/wiki/%D0%90%D0%B7%D0%BE%D1%82%D0%BD%D0%B0%D1%8F_%D0%BA%D0%B8%D1%81%D0%BB%D0%BE%D1%82%D0%B0> степень окисления центрального атома азота равна +5, тогда как формальная валентность - 4, а координационое число - 3. В молекуле озона <https://ru.wikipedia.org/wiki/%D0%9E%D0%B7%D0%BE%D0%BD>, имеющей сходное с SO2 строение, атомы кислорода <https://ru.wikipedia.org/wiki/%D0%9A%D0%B8%D1%81%D0%BB%D0%BE%D1%80%D0%BE%D0%B4> характеризуется нулевой степенью окисления (хотя часто говорят, что центральный атом кислорода имеет степень окисления +4).