Материал: Сода. Приготування вапняного молока
Крім основних процесів на содових заводах здійснюється ряд
побічних, які не мають безпосереднього відношення до отримання соди. Амонію
хлорид (NH4Cl), який утворюється за реакцією (2.2), завод може
випускати як додатковий головний продукт. Однак зазвичай на содових заводах
аміак регенерують із амонію хлориду і повертають назад у виробництво. Із цією
метою гідрокарбонатний маточний розчин, який містить NH4Cl,
обробляють вапняним молоком за реакцією:
NH4Cl + Ca(OH)2 → 2NH3
+ 2H2O + CaCl2.
Аміак, який утворюється, відганяють із розчину і направляють у відокремлення абсорбції.
Розчин кальцію хлориду (CaCl2) є відходом виробництва. Операція регенерації аміаку протікає відокремлено від дистиляції. На деяких заводах розчин кальцію хлориду використовується для отримання продукційного CaCl2.
Для отримання вапняного молока потрібен кальцію оксид (СаО), який на содових заводах отримують шляхом випалювання карбонатної сировини (крейди або вапна) у вапняно-випалювальних печах за температури від 1100 до 1200ºС за реакцією:
3 → CaO + CO2.
Карбон(ІV) оксид, який утворюється при цьому, використовують у процесі карбонізації, а вапно (СаО) гасять надлишком води з отриманням вапняного молока за реакцією:
+ H2O ↔ Ca(OH)2.
І, нарешті, на всіх содових заводах проводиться попередня очистка водного розчину натрію хлориду (сирого розсолу) від домішок - солей кальцію, магнію за допомогою Na2CO3 і Ca(OH)2. У процесі очищення утворюються практично нерозчинні Mg(OH)2 та CaCO3, які випадають в осад:
2 + Ca(OH)2 ↔ Mg(OH)2 + CaCl2
; (2.7)2 + Na2CO3 → CaCO3
+ 2NaCl. (2.8)
Потім осад Mg(OH)2 та CaCO3 відокремлюють, а очищений розсіл надходить у виробництво.
Принципова схема виробництва соди аміачним методом наведена в
додатку А.
2.3 Технологічні розрахунки
основного реакторного процесу
.3.1 Фізико-хімічні основи процесу
Процес гасіння полягає у взаємодії кальцію оксиду з водою за реакцією:
(тв)+ H2O(р) ↔ Ca(OH)2(тв)+
65,4 кДж/моль.
Реакція супроводжується великим екзотермічним ефектом, збільшенням об’єму твердої фази за використанням звичайного вапна і самодиспергyванням вихідного вапна. У табл. 2.3.1 наведена коротка характеристика вихідних речовин і продукту реакції.
Кальцію гідроксид не утворює стійких гідратів. Тому звичайно надлишок води, що міститься в різних зразках гідроксиду (до 1 моль на 1 моль СаО) пов’язаний силами поверхневої адсорбції і залежить від умов протікання реакції гасіння, питомої поверхні і терміну зберігання.
Таблиця 2.1 - Характеристика речовин відділення гасіння
|
Властивість |
Речовина |
||
|
|
СаО |
Н2О |
Са(ОН)2 |
|
Молекулярна маса |
56,1 |
18,0 |
74,1 |
|
Густина, кг/дм3 |
3,36 |
1,0 |
2,24 |
|
Мольний об’єм, дм3/кмоль |
16,7 |
18,0 |
33,1 |
|
Пористість під час випалювання,% |
34-55 |
- |
- |
Розчинність кальцію оксиду і гідроксиду обернено пропорційна
температурі в інтервалі 0 ≤ t ≤ 100 °С і визначається за формулами:
![]() ,
% мас; (2.10)
,
% мас; (2.10)
Процеси гідратації вапна класифікують залежно від мольного відношення взаємодіючих реагентів (водовапняне відношення).
Сухою гідратацією або сухим гасінням називають процес, під час якого вода, що надходить на гасіння вапна, повністю витрачається на хімічні реакції і випаровування. Продукт такої гідратації являє собою сухий порошок. Водовапняне відношення за сухої гідратації залежить від фізико-хімічних властивостей вихідного вапна і зазвичай становить близько 2.
Більш поширеним є процес мокрої гідратації, під час якого отримують тістоподібний продукт або вапняну суспензію.
На кінетику процесу гідратації, фізико-хімічні параметри одержуваної вапняної суспензії і вихід готового продукту впливають такі основні фактори:
вид, структура і хімічний склад карбонатної породи;
температура і тривалість випалювання;
наявність домішок у застосовуваному паливі;
гранулометричний склад вапна, час та умови його зберігання;
температура води;
водо-вапняне відношення;
спосіб та інтенсивність перемішування в процесі гідратації;
застосування добавок і т.д.
Видаляють такі основні стадії процесу гідратації вапна, які в практичних умовах можуть накладатися або заміняти одна одну:
. Абсорбція і капілярне проникнення води в глиб часток вапна.
. Розчинення кальцію оксиду.
З. Утворення та дисоціація проміжногоз’єднання.
. Зародкоутворення і кристалізація Са(ОН).
. Агломерація твердої фази та структурування суспензії.
В процесі сухої гідратації друга і четверта стадії відсутні. В процесі мокрої гідратації будь-яка з перших чотирьох стадій може виявитися лімітуючою. Так, найбільше впливають на першу і другу стадії процесу гідратації вигляд, структура і хімічний склад вихідної карбонатної сировини, а також умови її обпалювання. Тому для кожної конкретної вапняної сировини встановлюють оптимальну температуру і тривалість випалювання, вид палива коефіцієнт надлишку повітря, розміри шматків гартованого матеріалу і т.д.
Вапно, що отримане за низьких температур мас велику поверхневу активність і внутрішню змочуваність із-за розгалуженого характеру пір; процес гасіння протікає з високою швидкістю і характеризується значним підйомом температури.
Загальне збільшення швидкості гетерогенного процесу неминуче викликає зміну співвідношення швидкостей окремих стадій. З підвищенням ступеня подрібнення і пористості вапна зростає пересичення розчину кальцію гідроксиду. Це призводить до збільшення швидкості процесу утворення зародків і зниження швидкості росту окремих кристалів, шо обумовлює стійкість вапняної суспензії.
Із збільшенням температури швидкість гідратації зростає згідно рівняння:
![]() ,
(2.12)
,
(2.12)
де ![]() - константа швидкості за температури
- константа швидкості за температури ![]()
![]() -
константа швидкості за температури
-
константа швидкості за температури ![]() .
.
Це свідчить про лімітування реакції гасіння дифузійними процесами.
В процесі мокрого гасіння інтенсивне перемішування збільшує ступінь диспергування і швидкість гасіння (особливо на кінцевій стадії процесу).
Домішки, що впливають на процес гасіння можна розділити на дві групи: домішки, що потрапляють в зону реакції у твердій (тобто з вапном і паливом) і в рідкій фазах. Домішки, що містяться в сирої карбонатної породі і паливі в основному побічно впливають на процес гасіння, впливаючи на ступінь декарбонізації, структуру та активність вапна.
Деякі твердо фазні домішки безпосередньо впливають на кінетику гідратації і якість вапняної суспензії. Так Fе2О3, TіО2, Сr2O3 сповільнюють процес гідратації, а добавка 5 % (мол.) MgO зменшує швидкість реакції на третину. Покриття із СаСО3, на поверхні гальмує, але не запобігає гідратації. Добавка кальцію сульфату суттєво уповільнює процес. Домішки Аl2О3 підвищують в’язкість вапняного молока.
Велике значення має проблема впливу розчинних домішок, що містятьсяв
рідині, яка подається на гасіння, на процес гасіння вапна, що обумовлено
перспективністю використання промислових стоків содових заводів (наприклад,
дистилерної рідини) для отримання вапняної суспензії. Ці домішки впливають на
кінетику реакції гасіння, її тепловий ефект, фізико-хімічні властивості
вапняної суспензії і навіть на кристалічну модифікацію Са(ОН)2.
Швидкість гідратації збільшується за допомогою добавок рідких лугів, кальцію
хлориду, натрію хлориду. Іон ![]() не
тільки уповільнює процес гасіння, але й сприяє утворенню грубо дисперсної,
вапняної суспензії, що швидко освітлюється.
не
тільки уповільнює процес гасіння, але й сприяє утворенню грубо дисперсної,
вапняної суспензії, що швидко освітлюється.
Чим більша швидкість гасіння, тим вищий ступінь дисперсності
отримуваного вапняного молока. Так при підвищенні температури води, яка
подається на гасіння, зростає не тільки швидкість гасіння, але й ступінь
дисперсності отримуваної суспензії. На содових заводах початкова температура
води, що подається складає 60…80 °С.
2.3.2 Обґрунтування обраного технологічного режиму
До найбільш важливих регламентованих показників, які характеризують якість вапняного молока і забезпечують нормальну роботу відділення дистиляції, належать концентрація Са(ОН)2 або вільного СаО і температура вапняного молока. На содових заводах концентрацію вільного СаО у вапняному молоці називають титром молока, оскільки її визначають титруванням молока соляною кислотою у присутності індикатора - фенолфталеїну.
Для виробництва необхідно, щоб вміст Са(ОН)2 у вапняному молоці був вищим, оскільки при цьому зменшується об’єм дистилятної рідини, а от же підвищується продуктивність відділення дистиляції, знищуються витрати пари та трати вапна й аміаку з рідиною дистиляту. Однак, з іншого боку, за надто високої концентрації Са(ОН)2 підвищується в’язкість суспензії, ускладняється робота гасителя та інших апаратів. Практика показала, що гранично допустима концентрація Са(ОН)2 у вапняному молоці (титр) не перевищує 250 н.д. (нормальних ділень) або 35 % (мас).
Температура вапняної суспензії не перевищує 90 °С. Побічно можливість підвищення температури вапняної суспензії обмежена необхідністю зберігати її в порівняно великих буферних ємностях - мішалках, при цьому вапняна суспензія остигає.
Продуктивність гасителя визначається потребою виробництва реакційно здатному кальцію оксиду з урахуванням ступеня диспергування цього компоненту в апаратах відділення гасіння та його виробничих трат у відділенні регенерації аміаку. Витрата рідини, що подається на гасіння , є параметром регулювання, залежним від витрати вапна і регламентованої концентрації вапняної суспензії.
Продуктивність підтримується шляхом регулювання подачі вапна на гасіння
і залежить від кількості вапняної суспензії, що витрачається споживачами.
.3.3 Матеріальний баланс
Розрахувати матеріальний баланс процесу гасіння вапна за реакцією:
![]() ,
(2.13)
,
(2.13)
Розрахунок вести на 1000 кг Ca(OH)2, концентрацією 35%, якщо у вихідному СаО міститься 80% СаО, 8% СаСОа інше домішки. Врахувати ступінь використання СаО - 95%.
Розрахунок матеріального балансу:
Схема матеріальних потоків одержання гашеного вапна наведена
на рис. 2.1.
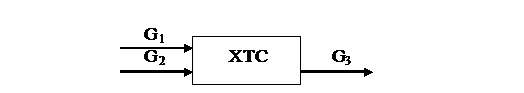
Рис. 2.1 - Схема матеріальних потоків одержання гашеного вапна
![]() .
(2.14)
.
(2.14)
На схемі прийнято такі позначення.
![]() -
маса вапна, кг. Склад цього потоку:
-
маса вапна, кг. Склад цього потоку:
![]() .
(2.15)
.
(2.15)
![]() -
маса води, кг. Склад цього потоку:
-
маса води, кг. Склад цього потоку:
![]() (2.16)
(2.16)
![]() -
маса гашеного вапна. Склад цього потоку:
-
маса гашеного вапна. Склад цього потоку:
![]() .
(2.17)
.
(2.17)
Розраховуємо масу гашеного вапна за формулою:
![]() (2.18)
(2.18)
де ![]() - маса гашеного вапна, кг;
- маса гашеного вапна, кг;
![]() -
концентрація гашеного вапна, %.
-
концентрація гашеного вапна, %.
![]() кг.
кг.
Масу вапна, яке прореагувало визначаємо по формулі:
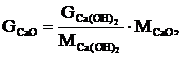 (2.19)
(2.19)
де ![]() - маса вапна, яке прореагувало, кг;
- маса вапна, яке прореагувало, кг;
![]() -
молярна маса кальцію гідроксиду, кг/кмоль;
-
молярна маса кальцію гідроксиду, кг/кмоль;
![]() -
молярна маса вапна, кг/кмоль.
-
молярна маса вапна, кг/кмоль.
![]() кг.
кг.
Масу непрореагованого вапна розраховуємо по формулі:
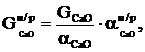 (2.20)
(2.20)
де ![]() - маса непрореагованого вапна, кг;
- маса непрореагованого вапна, кг;
![]() -
ступінь використання прореагованого вапна, %;
-
ступінь використання прореагованого вапна, %;
![]() -
ступінь непрореагованого вапна, %.
-
ступінь непрореагованого вапна, %.
![]() кг.
кг.
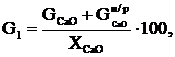 (2.21)
(2.21)
де ![]() - відсотковий вміст вапна, %.
- відсотковий вміст вапна, %.
![]() кг.
кг.
Масу вапняку розраховуємо по формулі:
![]() (2.22)
(2.22)
де ![]() - маса вапняку, кг;
- маса вапняку, кг;
![]() -
відсотковий вміст вапняку, %.
-
відсотковий вміст вапняку, %.
![]() кг.
кг.
Масу домішок розраховуємо по формулі:
![]() (2.23)
(2.23)
де ![]() - маса домішок, кг;
- маса домішок, кг;
![]() -
відсотковий вміст домішок, %.
-
відсотковий вміст домішок, %.
![]() кг.
кг.
Розраховуємо масу води, що прореагувала:
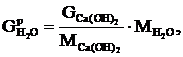 (2.24)
(2.24)
де ![]() - маса води, що прореагувала, кг;
- маса води, що прореагувала, кг;
![]() -
молярна маса води, кг/кмоль.
-
молярна маса води, кг/кмоль.
![]() кг.
кг.
Розраховуємо масу води, яка не прореагувала:
![]() .
(2.25)
.
(2.25)
де ![]() - маса води, що не прореагувала, кг;
- маса води, що не прореагувала, кг;
![]() кг.
кг.
Результати розрахунків заносимо в табл. 2.2.
Таблиця 2.2 - Матеріальний баланс гасіння вапна.
|
Прихід |
Витрата |
||||
|
Потік |
маса |
Потік |
маса |
||
|
|
кг |
% |
|
кг |
% |
|
1. Вапно |
348,5 |
100 |
3. Гашене вапно |
1000 |
100 |
|
в т. ч. СаОр СаОн/р СаСО3 Домішки |
264,9 13,9 27,9 41,8 |
76,0 4,0 8,0 12,0 |
в т.ч. Са(ОН)2 СаОн/р СаСО3 Н2Он/р Домішки |
350 13,9 27,9 566,4 41,8 |
35 1,4 2,8 56,6 4,2 |
|
2. Вода |
651,5 |
100 |
|
|
|
|
Н2Ор Н2Он/р |
85,1 566,4 |
13,1 86,9 |
|
|
|
|
Всього: |
1000 |
Всього: |
1000 |
||