Материал: Сода. Приготування вапняного молока
Сода. Приготування вапняного молока
Одеський національний політехнічний університет
Кафедра технології неорганічних речовин і екології
КУРСОВа РОБОТА
з курсу «Теоретичні основи технології неорганічних речовин»
на тему: Сода. Приготування
вапняного молока
Студентки 3 курсу ХТ-123 групи
напряму підготовки 6.0513.01 - Хімічна технологія
спеціальності 7.05130101 - Хімічні технології неорганічних речовин
Яворської О.М.
Керівник:
доцент
Іванченко Л.В.
м. Одеса - 2015 рік
ЗМІСТ
Вступ
. Розробка хімічної концепції цільового продукту
.1 Аналіз можливих варіантів одержання продукту
.2 Обґрунтування вибору способу виробництва
.3 Хімічна схема процесу
. Розробка технологічної концепції
.1 Основні і допоміжні стадії прийнятого до розробки способу
.2 Принципова технологічна схема
.3 Технологічні розрахунки основного реакторного процесу
.3.1 Фізико-хімічні основи процесу
.3.2 Обґрунтування обраного технологічного режиму
.3.3 Матеріальний баланс
. Апаратуро-технологічна схема
.1 Опис технологічної схеми
.2 Вибір типів основних апаратів
Висновок
Література
ВСТУП
Вуглекисла сода (натрію карбонат) була відома ще за давніх часів. Соду добували із золи, морських та солончакових рослин і діставали з ропи природних содових озер. Використовували соду у виробництві скла та як миючий засіб.
Кальцинована сода - традиційний продукт, що має багаторічну історію виробництва та використання. У теперішній час світове виробництво складає 34 млн. тон на рік. Найбільшими споживачами соди є хімічна (28 % від всього виробництва), скляна (26 %), металургійна (15 %) і інші галузіпромисловості.
У хімічній промисловості сода застосовується для отримання каустичної соди. Велика кількість натрію карбонату використовується у кольоровій металургії в основному в процесі виробництва глинозему з бокситів методом спікання кріоліту, під час перероблення свинцево-цинкових, кобальт-нікелевих, а також вольфрамо-молібденових руд. Велике застосування сода знаходить також у нафтохімічної і нафтопереробної промисловості в процесі виробництва синтетичних жирних кислот, синтетичних миючих засобів, а також в процесі перероблення нафти. У чорній металургії натрію карбонат використовується для видалення сірки і фосфору з чавуну. В машинобудуванні содо-продукти необхідні для пасивування і знешкодження деталей машин.
Середнє споживання кальцинованої соди з розрахунку на одну
людину в розвинутих країнах ![]() 25 кг. У країнах, що розвиваються і в країнах Азії
25 кг. У країнах, що розвиваються і в країнах Азії ![]() 2 кг. В Україні
2 кг. В Україні ![]() l5 + 16 кг. За прогнозами у 2020 р.
світове споживання соди становитиме приблизно 65 млн. тон.
l5 + 16 кг. За прогнозами у 2020 р.
світове споживання соди становитиме приблизно 65 млн. тон.
. РОЗРОБКА ХІМІЧНОЇ КОНЦЕПЦІЇ ЦІЛЬОВОГО ПРОДУКТУ
1.1 Аналіз можливих варіантів
одержання продукту
В даний час у світі виробництво соди базується на чотирьох способах її отримання:
аміачний (з натрію хлориду);
з природної соди;
з нефелінів;
карбонізацію натрію гідроксиду.
Аміачний спосіб отримання соди - це основний спосіб, що володіє низкою великих переваг:
. Необхідна для здійснення способу сировина - поварена сіль і кальцію карбонат - є недорогою, широко поширеною і легко видобуваємою.
. Основні реакції процесу здійснюються за невисоких температур (до 100 °С) і близьких до атмосферного тисків.
. Гарна вивченість способу, злагодженість і стійкість технологічних процесів.
. Висока якість вихідного продукту.
. Порівняно низька собівартість кальцинованої соди.
У аміачного способу отримання соди є й істотні недоліки, головними з яких є:
. Низький ступінь використання вихідної сировини (натрій використовується всього приблизно на 70 %, а хлор і кальцій не використовуються зовсім).
. Великі кількості рідких і твердих відходів, які потребують утилізації скидання або тривалого зберігання.
. Значна витрата енергетичних ресурсів.
. Великі питомі інвестиції, необхідні для створення содового виробництва.
Недоліки аміачного способу отримання соди стають все істотніше у міру посилення вимог до комплексного використання природної сировини і до охорони навколишнього середовища від забруднень, а також зі зростанням дефіциту і вартості енергоносіїв. Численні спроби зробити спосіб безвідходним або маловідходним досі успіхом не увінчалися. Розроблений і використовуваний промисловістю так званий модифікований аміачно-содовий процес в якому поряд з содою отримують амонію хлорид, хоча і є практично безвідходним, але широкого розповсюдження не отримав із-за невеликого попиту на амонію хлорид.
Отримання кальцинованої соди з природної содовмісної речовини - порівняно нова галузь содової промисловості світу, що стала одним з головних конкурентів аміачного способу. Цей спосіб був відомий давно, але
лише відкриття в 1938 р. в США найбагатших покладів трони (Na2CO3∙NaHCO3∙2Н2О) поклало початок розвитку технології переробки цієї сировини. В даний час кальциновану соду з трони отримують двома основними способами - сесквікарбонатним і моногідратним.
За першим з названих способів дроблену руду розчиняють з отриманням насиченого розчину, який після освітлення, фільтрування, очищення від органічних домішок випаровують і потім охолоджують. Кристали натрію сесквікарбонату, шо випали, відокремлюють і кальцинують за 200 °С. Отримують чистий продукт з насипний масою 800 кг/м3. Другий спосіб був розроблений в 1972 р. і зараз є провідним. За цим способом руду кальцинують, отриману сиру соду розчиняють, розчин освітлюють, фільтрують, обробляють активним вугіллям з метою очищення від органічних домішок і випаровують за температури нижче точки переходу натрію моногідрату карбонату в безводну соду. Отримані кристали натрію, моногідрату карбонату відокремлюють і дегідратують за температури близько 150 °С, з отриманням важкої соди, насипна маса якої 1070 кг/м3.
Отримувати кальциновану соду з природної набагато вигідніше, ніж виробляти її аміачним способом. Питомі капіталовкладення (на 1 т на рік потужності виробництва) становлять для підприємства з перероблення природної соди 300 у.о., для підприємства аміачної соди - 546 у.о., витрати робочої сили відповідно - 1,2 і 1,88 чол./год., витрата енергії - 6,З і 4,2 кДж/т.
Джерела природної соди є також у Бельгії, Бразилії, Мексиці, Пакистані, Китаї, Туреччині, Канаді, Кенії. Частку природної соди в світовому виробленні кальцинованої соди можна оцінити приблизно в 30 %.
Третій за значимістю з промислових способів отримання соди - комплексна переробка нефелінів на глинозем, кальциновану соду, поташ і цемент. Цей спосіб застосовується тільки в країнах СНД, і на його основі виробляються значні кількості кальцинованої соди, найбільшим родовищем нефелінів є Кія-Шалтирське, що знаходиться поблизу м. Ачинська. Великі родовища нефелінових порід є і в Хібінах (Кольський півострів), на півдні Донбасу - в Приазов’ї (Україна). Родовища нефеліну є в Норвегії і Гренландії. Кристали нефеліну у вулканічних породах зустрічаються в Італії (Везувій). Комплексна переробка нефелінів вигідна, оскільки дає можливість економити приблизно 15 % капіталовкладень і 20 % експлуатаційних витрат порівняно з самостійними виробництвами тих же продуктів з традиційної сировини.
У всьому світі в даний час діє лише кілька невеликих
установок по отриманню соди з каустичної соди, і частка цього способу в
світовому виробництві соди становить менше 1 %.
1.2 Обґрунтування вибору способу
виробництва
Вуглекисла сода (натрію карбонат) була відома ще за давніх часів. Соду обували із золи, морських та солончакових рослин і діставали з ропи природних содових озер. Використовували соду у виробництві скла та як миючий засіб. До кінця ХVІІІ століття ці джерела вже не могли задовольнити зростаючу потребу в соді. У 1775 р. французький фармацевт Леблан запропонував отримувати соду прожарюванням суміші натрію сульфату, подрібненої крейди або вапна та вугілля згідно за реакцією:
2SO4+СаСОз+2С→Na2CO3+CaS+2СО2.
З отриманого плаву соду вилуговували водою й розчин упарювали, виділяючи Na2SO3 у твердому вигляді. У шламі залишався CaS, який є відходом виробництва. Так як у природі натрій (Na) зустрічається частіше у вигляді сполучень NaCl (кухонна сіль), то необхідний для виробництва Na2SO4 було запропоновано отримувати взаємодією натрію хлориду з сульфатною кислотою.
Спосіб Леблана відіграв велику ролъ у розвитку хімічної промисловості та розробленні сировинних баз. Відхід содового виробництва НС1 переробляли на хлор і хлорні продукти: бемольне вапно і бертолетову сіль. З відходу CaS отримували елементарну cіpкy (S).
Сама сода використовувалась як вихідний продукт для oтримання багатьох натрієвих солей, наприклад, Na2CO3 (натрію гідрокарбонат - харчова сода), NaOH (луг - каустична сода), NаНSОз, Na2SO3 та інші.
Содові заводи стали центром хімічної промисловості, яка зароджувалась. У 1865 році бельгійським інженером Сольве було розроблено і здійснено у промисловому масштабі аміачний спосіб отримання соди.
У цілому "аміачна сода" виходила більш дешевою та кращої якості. Одночасно з розвитком аміачного способу отримування сод ивдосконалювався і спосіб Леблана. Щоб не викидати в навколишнє середовище НС1, було розроблено способи переробки HCl (водню хлорид) на хлор і хлоровмісні продукти.
У ті роки содові заводи, які працювали за способом Леблана, були єдиними постачальниками хлорних продуктів. Коли ж з 1890 р. став поширюватися електрохімічний спосіб отримання хлору, виробництво соди за способом Леблана поступово припинилось.
У більшості країн аміачний спосіб залишився провідним до наших днів. Перший содовий завод, який працював за методом Леблана було збудовано у Pocіі у l864 р. Аміачний спосіб став застосовуватися в Pocіі з 1883 р., коли було побудовано завод у Березниках на базі Солікамського родовища кухонної солі. В Україні в 1892 р. був побудований перший содовий завод у м. Лисичанську, а в 1898 р. - в м. Слов'янську, який працював за способом Гонігмана - менш досконалому в частині технологічної схеми й апаратури.
Цей спосіб був розроблений ще в 60-х роках XІX століття. Він складається з декількох дуже раціонально оформлених стадій, що забезпечує високу економічну ефективність і в даний час.
Сода являє собою натрію карбонат Na2CO3. Сировиною для одержання служать природна поварена сіль NaCl і природний вапняк CaCO3. Завдання процесу полягає в організації взаємного обміну іонами Na+ і Ca2+.
Процес полягає в тому, що в результаті випалу вапняку CaCO3
одержують негашене вапно СаО і двоокис вуглецю СО2 за реакцією
(а). Останній реагує з NaCl і NH3 з утворенням амонію хлориду NH4Cl
і двовуглекислої соди NaHCO3 за реакцією (в). При нагріванні NaHCO3
відбувається її розкладання за реакцією (д) з утворенням цільового
продукту кальцинованої соди - Na2CO3 і діоксид вуглецю
повертається в процес. Хімічна схема процесу може бути представлена в такому
вигляді:
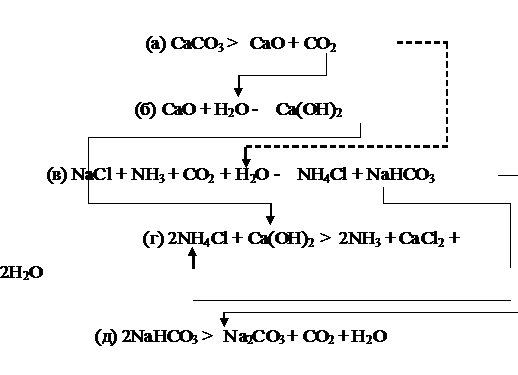
Рис. 1.1 - Хімічна схема виробництва кальцинованої соди
вапняний молоко реакторний технологічний
Оксид кальцію перетворюється в Ca(OH)2 за реакцією (б), а потім взаємодіє з NH4Cl за реакцією (г) з утворенням газоподібного аміаку і кальцію хлориду. Аміак повертається у виробничий цикл, а кальцію хлорид виводиться з процесу як відхід.
Хімічна схема виробництва соди являє вдалий приклад кваліфікованого оформлення хіміко-технологічного процесу. Саме цим пояснюється те, що, незважаючи на великі успіхи хімічної технології, поки ще не знайдені більш досконалі і більш дешеві способи одержання соди. Старий аміачний спосіб, розроблений майже 150 років тому, успішно експлуатується і в даний час. Велику частину соди в усьому світі одержують саме цим способом, навіть незважаючи на великий його недолік, який полягає в тому, що одержуваний як відхід кальцію хлорид поки не знайшов застосування. Його виводять із процесу у вигляді водяного розчину і зливають у спеціально вириті котловани - «білі моря». Ці «білі моря» отруюють ґрунт і водойми, що прилягають до них. Збереження й утилізація величезних кількостей відходів кальцію хлориду, що накопичуються, є важливою екологічною проблемою.
2. РОЗРОБКА ТЕХНОЛОГІЧНОЇ КОНЦЕПЦІЇ
2.1 Основні і допоміжні стадії
прийнятого до розробки способу
Виробництво кальцинованої соди за аміачним способом включає вісім основних переділів (цехів або відділень):
. Одержання карбонатної сировини: видобування, дроблення, сортування та транспортування.
. Перероблення карбонатної сировини: обпалювання, охолодження та очищення карбон(ІV) оксиду, гасіння вапна з отриманням вапняної суспензії.
. Очищення розсолу: взаємодія сирого розсолу з реагентами в реакторах і відстоювання розсолу.
. Абсорбція: відмивання в відмивниках газів, що виділяються на других стадіях, від аміаку, двох стадійне насищення розчину натрію хлориду аміаком і частково карбон(ІV) оксидом, що потрапляють зі стадії дистиляції, охолодження амонізованого розсолу.
. Карбонізація: відмивання від аміаку газу, що відходить зі стадії карбонізації (супроводжується уловлюванням невеликих кількостей карбон(ІV) оксиду), попередня карбонізація, карбонізація з виділенням натрію гідрокарбонату в осаджуваних колонах, компримінування (перед подачею в карбонізаційні колони) карбон(ІV) оксиду, що потрапляє зі стадій перероблення карбонатної сировини і кальцинації.
. Фільтрація: відділення натрію гідрокарбонату на фільтрах та відсмоктування повітря вакуум-насосами.
. Кальцинація: зневоднення і розкладення натрію гідрокарбонату в содових печах, охолодження та очищення карбон(ІV) оксиду після содових печей.
. Регенерація аміаку (дистиляція): попереднє
підігрівання і дисоціація в конденсаторі та теплообміннику дистиляції амонію
карбонатів і гідрокарбонатів, що містяться в фільтровій рідині, змішання і взаємодія
нагрітої рідини з вапняною суспензією в змішувачі та відгонка аміаку в
дистилері.
2.2 Принципова технологічна схема
В аміачному способі кальциновану соду отримують через гідрокарбонат амонію за реакцією:
4HCO3 + NaCl ↔ NaHCO3 + NH4Cl
На содових заводах амонію гідрокарбонат отримують NH4 та СО2 безпосередньо у водних розчинах NaCl, тобто з хімічної точки зору отримати натрію гідрокарбонат можна за реакцією:
+ NH3 + CO2 + H2O ↔
NaHCO3 + NH4Cl
Оскільки карбон(ІV) оксид погано розчиняється у воді за відсутності аміаку, то практично спочатку розчин NaCl (розсіл) збагачують аміаком, а потім отриманий амонізований розсіл обробляють CO2, тобто процес проводять у дві стадії. Перша стадія поглинання аміаку протікає у відділені абсорбції, а друга - поглинання СО2 - у відділені карбонізації.
Осад NaHCO3, який випав у процесі карбонізації,
відфільтровують, а далі він розкладається з отриманням соди за реакцією:
NaHCO3![]() Na2CO3 + CO2
+ H2O
Na2CO3 + CO2
+ H2O
В залежності від конструкції печі температура розкладання NaHCO3 складає від 100 до 180 ºС. Ця операція проходить у відділенні кальцинації. Карбон(ІV) оксид, який при цьому виділяється, використовують у відділенні карбонізації.