Материал: Синтез наноматериалов с применением нанореакторов
.1 Получение наночастиц в нульмерных
нанореакторах
К нульмерным нанореакторам относятся материалы, характеризующиеся открытой пористостью с упорядоченным расположением сферических пор. К числу таких материалов в первую очередь следует отнести цеолиты - природные и синтетические алюмосиликаты состава
ixMiiy(Alx+2ySizO2x+4y+2z)nН2О
К настоящему моменту известно более 150 типов цеолитов, из которых около 30 - природные цеолиты. Структура цеолитов построена из тетраэдров [Si04]4- n [АlO4]5-, объединенных общими вершинами в трехмерный каркас, пронизанный полостями и каналами, в которых располагаются молекулы воды и катионы щелочных (Мi) и щелочноземельных (Мii) металлов.
В отличие от атомов каркаса, связанных между собой ковалентными связями, катионы, находящиеся в каналах, связаны с матрицей только электростатически и могут легко обмениваться на другие катионы в водных растворах.
Изоморфное замещение атомов алюминия каркаса на атомы других элементов, таких как В, Ga, Fe, Со, Ti, V, и обмен катионов, содержащихся в порах, позволяют направленно изменять свойства цеолитов. Существует несколько факторов, обусловливающих возможность изоструктурного замещения [6]:
близость радиусов замещаемого и замещающего атомов (чем больше различие в радиусах, тем энергетически менее выгодна замена);
замещение меньшего по размеру атома на больший возможно при условии уменьшения координации последнего, и наоборот;
близость электроотрицательностей и потенциалов ионизации замещаемого и замещающего атомов;
достижение минимума свободной энергии в процессе изоморфного замещения с сохранением координационного числа.
По сравнению с другими тектосиликатами цеолиты имеют более открытую структуру. Тетраэдры ТО4 (первичные сборочные узлы) формируют кольца различных размеров, в результате соединения которых образуются более сложные структуры (вторичные сборочные узлы), причем различным типам цеолитов соответствуют определенные сочетания вторичных сборочных узлов. (Следует отметить, что угол Si -О -Si может изменяться в достаточно широких пределах (135-165°), в результате чего становится возможным существование кремниево-кислородных колец с различным числом атомов.) Для цеолитов с большим содержанием кремния более характерны кольца с 5 атомами кислорода, в которых угол Si-О-Si составляет около 145°. Цеолиты с большим содержанием алюминия, имеющие в структуре большое количество связей Si -О-А1, в основном построены из колец, содержащих 3 или 6 атомов кислорода. В структурах природных цеолитов наиболее часто встречаются кольца с 4 или 6 атомами кислорода.
Классификация цеолитов представляет собой достаточно сложную задачу. Каждая индивидуальная структура описывается структурным кодом, содержащим только три заглавные латинские буквы - так называемый IZA-код, принятый International Zeolite Association Structure Commission. Эта кодировка применима как к алюмосиликатам, так и к некоторым другим соединениям, имеющим аналогичную структуру и содержащим атомы элементов (Si, Al, Р, Ga, Ge, В, Be и др.) в тетраэдрическом окружении.
Наиболее общий подход к синтезу цеолитов основан на совместном гидролизе соединений кремния и трехзарядного металла (чаще всего алюминия) в присутствии щелочи и четвертичного амина (темплат). В качестве источников атомов кремния чаще всего используют кремнийорганические соединения, подвергающиеся гидролизу, силикат натрия или силикагель с большой площадью поверхности (>200 м2г-1), в качестве источников ионов М3 + - соли (сульфаты, нитраты, хлориды) или алкоксиды (изопропилаты, бутилаты) этих металлов, а в качестве темплатов - первичные, вторичные, третичные и четвертичные амины, спирты и некоторые эфиры.
Схемы синтеза цеолитов различного состава и структуры фактически одинаковы. Гели, содержащие соединения кремния и алюминия, состаривают в течение длительного времени при температуре ниже температуры кристаллизации (нередко в гидротермальных условиях) в присутствии тем платов. Это время необходимо для формирования цеолита с необходимой структурой и высоким выходом. Условия состаривания и природа темплатов оказывают решающее влияние на структуру цеолитов. Присутствие молекул темплата повышает кристалличность алюмосиликатного каркаса и влияет на его структуру. Цеолиты некоторых структурных типов могут формироваться и без использования темплата. Структурный тип получаемого цеолита зависит также от природы и концентрации источника трехзарядного металла.
В цеолитах отрицательный заряд матрицы компенсируется ионами щелочных металлов, аммония и/или алкиламмония (в зависимости от использованных в ходе синтеза реактивов). Катионы металлов, как правило, удаляют промыванием или ионным обменом на NH4+, так как присутствие катионов металлов понижает термическую стабильность получаемых матриц. Для удаления темплата готовые цеолиты отжигают в токе кислорода при 500 - 550°С, переводя их в так называемую Н-форму. Контроль соотношения Si:А1 в цеолитах осуществляют стандартными методами количественного анализа.
В силу открытой пористости цеолитов и высокой скорости диффузии газов в порах химические реакции с участием интеркалированных катионов можно проводить при повышенных температурах (например, восстановление водородом, необходимое для получения магнитных нанокомпозитов) практически без разрушения матрицы, ограничивающей реакционную зону. Указанные свойства открывают широкие возможности химического дизайна нанокомпозитных материалов на основе цеолитов.
Наибольшее распространение получили
наноматериалы на основе цеолита Y (тип FAU). Структура Y-цеолита
состоит из вторичных сборочных узлов 6-6 (гексагональная призма), 6-2
(шестиугольник и квадрат с общим ребром), 6 (шестиугольник) и 4 (квадрат) (рис.
1).
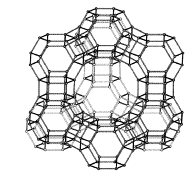
Рисунок 1 - Структура цеолита Y
Основным мотивом структуры цеолитов
FAU является усеченный кубом октаэдр - содалитовая ячейка или малая р-полость с
внутренним диаметром 0.66 нм, состоящая из четырехчленных (свободный диаметр
менее 0.1 нм) и шестичленных колец (диаметр ~0.22 нм) из Т-атомов. В вершинах
многогранника расположены 24 атома Т, а атомы кислорода находятся между ними.
При соединении таких многогранников через гексагональные призмы (диаметр
полости 0.36 нм) из Т-атомов образуется структура цеолитов (X и Y). Для них
характерна кубическая сингония с параметрами решетки а=24.345 А(рис.2).

Рисунок 2 - Усредненное изображение
кристалла NaY вдоль направления [110], полученное с помощью просвечивающей
электронной микроскопии (ПЭМ)
В структуре имеются различные типы полостей: а-полость (а-cage, supercage) - самая крупная полость (диаметр 1.2 нм), находящаяся в окружении 8 усеченных октаэдров; р-полость (p-cage, sodalite cage) - полость, ограниченная усеченным октаэдром; у-полость - гексагональная призма (см. рис. 1).
Основным методом получения нанокомпозитных материалов на основе цеолитов является обмен катионов Na+, Н и NHJ, входящих в состав цеолитов, на катионы других металлов в водных растворах с последующим восстановлением металла водородом. Получение медьсодержащего цеолита ионным обменом нитрата меди с NaY-цеолитом или отжигом смеси NaY-цеолита с хлоридом меди при 420СС. В случае твердофазного отжига исходный цеолит NaY сначала стабилизировали, добавляя NaBr для заполнения р-пол остей. Это позволило ввести медь в а-полости и повысить термическую стабильность матриц. Восстановление проводили в атмосфере водорода при температурах 300-600°С. В обоих случаях были получены частицы меди (3-7 нм), превышающие по размеру а-полости, что приводило к разрушению пористой структуры.
Аналогичным образом получали нанокомпозиты Au/NaY и Au-Fe/NaY. И в этом случае восстановление металлов приводило к формированию наночастиц, значительно превышающих размеры а-полости цеолита.
Лантанидсодержащие цеолиты (структурный тип FAU) образуются в результате ионного обмена катионов, входящих в состав цеолитов, с хлоридами или нитратами РЗЭ. Отжиг модифицированных таким путем цеолитов при 500°С приводит к образованию оксидов редкоземельных элементов и частичному замещению атомов алюминия в структуре цеолита на атомы РЗЭ, что повышает термическую стабильность цеолита. При достаточно высоких содержаниях лантанидов наблюдается также образование оксидов лантанидов вне цеолита. Помимо солей металлов можно применять также комплексные катионы.
В последнее время появились работы по синтезу наночастиц интерметаллидов с использованием цеолитов. Таким путем были получены (Pt, Pd)-за мешенные цеолиты. Аммонийные комплексы палладия и платины внедряли в Y-цеолит ионным обменом. Термолиз комплексов металлов в токе кислорода при температуре 300°С с последующим восстановлением в токе водорода при 300°С приводил к формированию наночастиц сплава, содержащего ~40% платины, однако данные относительно расположения наночастиц в матрице цеолита отсутствуют.
Для получения Au-Pd-интерметаллида в Y-цеолите в качестве источника золота использовали комплекс [Au(en)2]3 +, а в качестве источника палладия - Pd(NH3)4+. Ионный обмен проводили в две стадии. Сначала вводили в матрицу цеолита комплекс палладия, термолиз которого в кислороде сопровождался образованием атомов Pd и их перемещением в более выгодные по координации р-полости. Затем осуществляли ионный обмен с комплексом золота с последующим восстановлением композита. Образование сплава проходило в ос-полости цеолита. В зависимости от соотношения Au: Pd и состава исходного цеолита были получены частицы размером от 1 до 3 нм. Продолжительный отжиг приводил к плавлению наночастиц с одновременным их ростом (до 3.5-4 нм) и частичному разрушению пористой структуры цеолита.
Следует отметить, что синтез нанокомпозитов в цеолитах не ограничивается применением матриц структурного типа FAU. Известно немало работ, посвященных получению нанокомпозитов в цеолитах структурного типа MFI (а также ZSM, MAS и др.), которые относятся к одномерным нанореакторам.
Более удачный пример использования цеолитов в качестве нанореакторов: смешанные сульфиды кобальта и молибдена в Y-цеолите получали последовательным замещением ионов Na+ на ионы кобальта с последующим введением в цеолит гексакарбонила молибдена в токе СО. Согласно данным химического анализа, на каждую а-полость цеолита приходилось около двух молекул Мо(СО)6. Общий состав образца, полученного на этой стадии, описывается формулой Со(4мас.%)Мо(10 Mac.%)NaY. Далее образец сульфидировали в токе H2S при разных температурах (25-400°С). Образовавшиеся при этом частицы смешанных сульфидов имели размер 1 -2 нм.
Цеолиты активно применяют и в качестве матрицы для получения люминесцентных наночастиц [5].
В настоящее время основной проблемой
при создании нанокомпозитов на основе цеолитов является сложность изучения
распределения наночастиц в матрице методом прямого наблюдения, таким как
просвечивающая электронная микроскопия (ПЭМ). Поэтому большее распространение в
синтезе изолированных в матрице нанокомпозитов получили матрицы, обладающие
упорядоченной пористой структурой с размером пор 2-50 нм. К числу таких матриц
относятся мезопористые молекулярные сита и пористый оксид алюминия.
.2 Получение наночастиц в одномерных
нанореакторах
Нанореактор, 1D (англ. nano-reactor, 1D) - разновидность нанореактора, размер которого в двух измерениях не превышает 100 нм, а в третьем - существенно больше.
Одномерные нанореакторы, обеспечивающие диффузию реагирующих компонентов лишь вдоль одного из направлений, активно используются при получении протяженных нанообъектов - наностержней и нановолокон [1].
В качестве твердофазных одномерных нанореакторов могут быть использованы углеродные нанотрубки, пористый кремний, цеолиты типа MFI, мезопористые молекулярные сита и пористые структуры на основе оксида алюминия и титана, полученные методом анодирования.
Скол пленки пористого диоксида титана, синтезированного методом анодного окисления металлического титана. Может использоваться в качестве нанореактора для получения нановолокон различных металлов методом электроосаждения, осаждения из газовой фазы и т.д. (рис. 3).

Рисунок 3 - Скол пленки пористого диоксида титана
Круг материалов, которые могут быть
использованы в качестве одномерных твердотельных нанореакторов, невелик. Он
включает цеолиты типа MFI, мезопористые молекулярные сита и мезопористые
структуры на основе оксида алюминия.
.2.1 Цеолиты структурного типа MF1
Цеолиты типа MFI обладают
упорядоченной системой каналов диаметром 0.54-0.56 нм с гексагональной
упаковкой (рис. 4). Наночастицы металлов в каналах MFI-цеолитов
обычно получают ионным обменом протонов (цеолит в Н+ - форме) на
катионы металлов или комплексы металлов с последующим мягким восстановлением в
токе водорода [6].
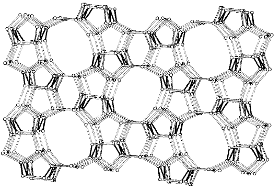
Рисунок 4 - Структура цеолита
структурного типа MFI
При восстановлении катионов металла
в матрице таких цеолитов следует ожидать формирования анизотропных наночастиц
(к сожалению, исследования распределения частиц по размерам и их анизотропии не
проводились из-за сложности, связанной с малым размером каналов).
.2.2 Мезопористые молекулярные сита
Мезопористые молекулярные сита были открыты исследователями американской компании Mobile Research and Development Corporation в 1992г. Им удалось синтезировать семейство сит на основе SiO2 (МСМ-41), обладающих однородным и высокоупорядоченным распределением пор строго контролируемого размера от 2 до 10 нм и с чрезвычайно высокой удельной поверхностью (~ 1000 м2 г-1).
Наиболее распространенным методом
синтеза мезопористого SiO2 является темплатный метод. Темплат, или
шаблон, является центром, вокруг которого организуются основные структурные
единицы матрицы и формируется каркас. Удаление темплата приводит к образованию
полости такого же размера и формы, как темплат. Точность «отпечатка» после
удаления темплата зависит от нескольких факторов: природы взаимодействия
темплат-матрица, способности матрицы принимать очертания темплата,
относительных размеров темплата и структурных единиц матрицы. Схема темплатного
синтеза изображена на рис. 5.
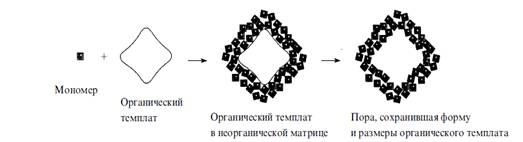
Рисунок 5 - Схема темплатного
синтеза
И хотя открытие молекулярных сит датируется 1992 г., первое описание «темплатного синтеза» относится к 1949 г., когда было изучено гелеобразование тетраэтоксисилана (TEOS) в присутствии индикатора метилоранжа (темплат). Образовавшийся в результате поликонденсации TEOS силикагель селективно адсорбировал метилоранж. С тех пор этот довольно простой и элегантный метод стал широко применяться для синтеза большого числа органических и неорганических материалов.
Рассмотрим синтез молекулярных сит на примере получения мезопористого SiO2 (МСМ-41). Образцы МСМ-41 получают поликонденсацией соединений кремния (Si(Ome)4 или Si(Oet)4) в присутствии темплата, в качестве которого могут выступать различные молекулы, в частности нековалентно связанные органические поверхностно-активные вещества (ПАВ).
Бифункциональные молекулы цетилтриметиламмоний-бромида амфифильны, т.е. содержат гидрофильную головную группу и гидрофобный «хвост». В водном растворе такие молекулы объединяются в мицеллы, в которых гидрофильные головные группы образуют внешнюю поверхность, а гидрофобные «хвосты» обращены к центру. Степень мицеллизации и форма мицелл зависят от концентрации ПАВ. При высоких концентрациях ПАВ происходит агрегация мицелл с образованием жидкокристаллических фаз, структура которых зависит от температуры и концентрации раствора. На рис. 6 приведена фазовая диаграмма системы С16H33Nme3Br.
Реакционную смесь, содержащую водный
раствор ПАВ, тетраалкоксисилан и кислоту (или щелочь) термостатируют в течение
нескольких часов при температуре 80°С. При этом в результате гидролиза
тетраалкоксисилана вокруг мицелл ПАВ образуется мезопористый оксид кремния. К
числу параметров, влияющих на процесс гелеобразования, относятся pH раствора,
природа и концентрация темплата и кремнийсодержащего соединения, температура,
тип катализа и др.