Материал: Разработка простой в исполнении титриметрической методики определения хлорат-ионов в природных водах
Вследствие различных величин ионных радиусов и термодинамических свойств ионов ClO3- и СlO4- способность к ассоциации их с ионами К(Ⅰ) неодинакова, поэтому при титровании смеси хлорат- и перхлорат-ионов на кривой титрования получается два перегиба. Это положено в основу анализа их смеси. Метод дает возможность определять ClO3- и СlO4- в смесях при их соотношениях от 4 : 1 до 1 : 4. Небольшие количества хлоратов (~0,1 мг) могут быть определены в присутствии перхлорат-, бромат-, иодат-, периодат-ионов путем измерения светопоглощения в инфракрасной области (20,4 мк) [1].
.1.3 Хроматографический метод
Настоящая методика выполнения измерений распространяется на воду питьевую централизованного водоснабжения, воду бутилированную и устанавливает определение массовой концентрации хлорит- и хлорат-ионов методом ионной хроматографии.
Отбор и хранение проб воды питьевой центрального водоснабжения и воды питьевой бутилированной производятся в пластиковые емкости с плотными крышками. Для получения достоверных результатов анализа емкости предварительно ополаскивают не менее чем 5 полными объемами отбираемой пробы, затем наполняют пробой, не допуская свободного объема воздуха под крышкой. Рекомендуется для каждой точки пробоотбора использовать одну и ту же емкость.
Пробоподготовка для пробы воды состоит из этапов отбора пробы, центрифугирования (в случае визуального обнаружения взвешенных частиц или осадка в пробе), фильтрования супернатанта или отобранной пробы при помощи одноразового пластикового шприца с фильтрующей нейлоновой насадкой и последующего хроматографического разделения.
Хранение проб производят в пластиковых емкостях с плотными крышками.
Метод основан на ионообменных процессах, приводящих к разделению ионов на разделительных ионообменных хроматографических колонках, заполненных ионообменником соответствующего типа.
Для хроматографического анализа хлорит- и хлорат-ионов необходимо использовать ионную хроматографическую систему (ионный хроматограф) с кондуктометрическим детектором и системой подавления фоновой электропроводности элюента для анионного анализа.
Для проведения анализа предварительно готовят градуировочные растворы (для приготовления градуировочных растворов целесообразно использовать стандартные сухие вещества); проводят пробоподготовку; подготавливают к работе прибор.
Перед проведением хроматографического анализа в прибор, собранный в соответствии с инструкцией по эксплуатации, должны быть установлены последовательно две аналитические колонки.
Для определения количественного содержания компонентов пробы (хлорит- и хлорат-ионов) проводят хроматографический анализ одного из градуировочных растворов и далее хроматографический анализ подготовленной пробы. Для достоверности измерений хроматографический анализ как градуировочного раствора, так и подготовленной пробы проводят не менее 2 раз подряд.
Для получения результата необходимо провести как минимум два параллельных измерения (получить две хроматограммы).
За результат измерений
принимают среднее арифметическое результатов двух параллельных определений [6].
1.1.4 Потенциометрические методы
Потенциометрические методы определения хлорат-ионов основаны на взаимодействии их с восстановителями. Для этой цели используют растворы сернокислого железа(Ⅱ) и арсенита натрия, ферроцианид калия, аптимонилтартрат калия, соли титана(Ⅲ).
Прямое потенциометрическое титрование хлорат-ионов раствором соли Мора рекомендуют проводить в среде фосфорной кислоты, так как при этом в системе протекает целевая реакция восстановления хлорат-ионов до хлорид-ионов и подавляются побочные реакции восстановления хлорат-ионов до гипохлорит-ионов и элементного хлора. Реакция катализируется 0,01 М раствором четырехоксида осмия, но требуемое количество OsO4 (0,75 мл 0,01 М раствора на 0.8-8 мг ClO3-) приводит к отрицательным ошибкам. Титрование проводят в среде H3PO4 (1 : 1) при нагревании титруемой смеси до 70-80° С с гладким платиновым электродом и насыщенным каломельным электродом сравнения. Перед точкой эквивалентности титровать следует медленно, выжидая 1-3 мин. перед прибавлением каждой порции титранта. Не мешают определению хлорат-ионов ионы SO4-, PO4-, B4O72-, Вг-, Сl- (до 30-кратного избытка), F- (до 75-кратного избытка) и NO3- (до 15-кратного избытка). Иодид- и гипохлорит-ионы мешают и должны быть удалены обработкой H2O2. Ошибка составляет 0,21%.
В связи с том, что реакция восстановления хлорат-ионов ионами железа(Ⅱ) протекает медленно, некоторые авторы рекомендуют прибавлять к исследуемому раствору избыток соли Мора в кислой среде (~ 9 Н H2SО4), нагревать для полного протекания реакций и после охлаждения определять хлорат-ионы по образующимся хлорид-ионам или по избытку ионов Fe(Ⅱ), не вступивших в реакцию. В последнем случае титруют раствором перманганата калия.
Арсенитометрическое определение хлорат-ионов проводят титрованием избытка арсенита натрия, не вступившего в реакцию с хлорат-ионом. В качестве титрантов используют раствор бромата калия, перманганата калия или церросульфата аммония в присутствии OsО4. В присутствии повышенных количеств OsО4 возможно прямое титрование хлорат-ионов арсенитом натри я. Индикаторным электродом служит гладкая платина, электродом сравнения - графитовый или каломельный электрод. В присутствии OsО4 реакция восстановления протекает с промежуточным образованием НСlO, которая легко реагирует с арсенитом натрия. Скорость реакции сильно тормозится хлорид-ионами, т. е. продуктами реакции, вследствие перехода индикатора в малоактивную форму. Лучшая среда для титрования 1,5-2 Н H2SО4 или 1 Н НСl. Титрование проводят при комнатной температуре. Ошибка не более 0,5%.
Описан вариант метода, при котором хлорат-ионы восстанавливают до хлорид-ионов раствором арсенита натрия в среде 1 М H2SО4 в присутствии катализатора OsО4. Затем образующиеся хлорид-ионы титруют в 70%-ном метаноле раствором азотнокислого серебра с хлорселективпым электродом.
В 12 Н НС1 хлорат-ионы можно титровать потенциометрически раствором ферроцианида калия.
Хлорат-ионы в 1-4 Н НСl
или H2SО4 титруют потенциометрически раствором 0,05 Н
Ti2(SО4)3 с получением двух скачков
потенциала. Первый соответствует восстановлению хлорат-иона до Сl2,
второй - до Сl-. В растворе 2-4 Н HNO3
в присутствии OsO4
хлорат-ионы можно титровать потенциометрически раствором антимонилтартрата
калия с платиновым индикаторным электродом и НКЭ в качестве электрода сравнения
[7].
1.1.5 Полярографический метод
Полярографический метод определения СlO3- основан на образовании каталитической волны восстановления на фоне раствора 10-2 М Ti(Ⅳ), 0,2 М раствора щавелевой кислоты, 0,4 М по H2SО4, 0,25 М по Na2SО4 и 0,01 %-ного раствора желатина. В этих условиях предельный ток имеет диффузионный характер и пропорционален концентрации ClO3- в пределах концентрации 10-3-1,5*10-2 М. При достаточном избытке ClO3- предельный каталитический ток пропорционален концентрации Ti(Ⅳ) и корню квадратному концентрации ClO3-. Ионы гидроксония и галогенидные увеличивают каталитический ток, но только если их концентрация ниже 0,5 и 0,05 М соответственно. При больших концентрациях они не мешают. Описываемым методом хлорат-ионы могут быть определены в присутствии 0,1 М перхлорат-ионов. Метод применен для определения хлората магния в растениях [8].
.1.6 Амперометрический метод
Предложено определять хлорат-ион восстановлением до хлорид-иона сернистой кислотой и титровать амперометрпчески с вращающимся Pi-электродом при 0 в. Можно также восстановить хлорат-ион стандартным раствором соли Мора и оттитровать избыток последней раствором бихромата калия амперометрически при 1,0 в.
Хлорат-ион титруют амперометрически раствором азотнокислой ртути(Ⅰ) в среде 1 М H2SO4 с добавлением КВг. Мешают определению элементный хлор и гипохлорит-ионы [9].
2. ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
.1 Приборы и реактивы:
Хлорат калия 1 г/л, готовили следующим образом: навеску 1 г бертолетовой соли разбавляли в мерной колбе на 1 л дистиллированной водой.
Сернокислое железо (Ⅱ) 0,01 М эквивалента, подкисленный серной кислотой 100 мл на 1 л раствора готовили следующим образом: навеску железного купороса 2,8 г растворяли в 1 л дистиллированной воды и добавляли 100 мл серной кислоты 1 М.
Перманганат калия 0,01 М эквивалента готовили следующим образом: раствор перманганата калия 0,05 М разбавили в 5 раз.
Электрод платиновый
Электрод хлорсеребряный
Пипетки на 10 и 1 мл
Бюретка
Мерная колба на 100 мл
Стаканы термостойкие
Плитка
.2 Методика определения
В два стакана налить по 100 мл раствора, содержащего 0,5-5 мг/л хлорат ионов, прибавить по 10,00 мл раствора сернокислого железа(Ⅱ) 0,01 М эквивалента. Раствор в первом стакане кипятить 20 минут, охладить до комнатной температуры, поместить на магнитную мешалку, погрузить в раствор электроды и титровать раствором перманганата калия 0,01 М эквивалента, регистрируя показания милливольтметра. Раствор во втором стакане титровать аналогично первому без кипячения.
2.3 Сущность титриметрического
метода
Определение в водных растворах хлорат-ионов титриметрическим методом, основано на их восстановлении сернокислым железом (Ⅱ) в кислой среде при нагревании и последующем определении избытка восстановителя раствором перманганата калия.
Химизм реакции восстановления хлорат-иона:
KClO3 + 6 FeSO4
+ 3H2SO4→KCl + 3Fe2(SO4)3
+ 3H2O
Определение количества избытка железа (Ⅱ)
проходит по реакции:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
2.4 Определение чувствительности
методики
Приготовили растворы KClO3
с концентрацией 0,5 - 5 мг/л хлорат-ионов. Проводили перманганатометрическое
титрование с фиксированием потенциала системы по методике, описанной в п. 2.2.
Строили графики зависимости потенциала от объёма титранта. Для определения
точки эквивалентности рассчитывали и строили дифференциальную зависимость dE/dV
= f(V).
Результаты представлены в таблицах 1-6. Проводили опыт в трёх параллелях.
Таблица 1
Зависимость потенциала системы от объёма
титранта KMnO4
в
холостой пробе, пробе после кипячения и дифференциальные зависимости
при концентрации ClO3-
0,5 мг/л
V,
мл
E,
мВ
холост.
E,
мВ после кип.
dE/dV холост.
dE/dV после
кип.
0
535
513
1
536
513
1
0
2
540
514
4
1
3
548
518
8
4
4
554
520
6
2
5
557
525
3
5
6
563
530
6
5
7
570
534
7
4
8
579
550
9
16
8,1
557
70
8,2
560
30
8,3
565
50
8,4
567
20
8,5
591
574
24
70
8,6
595
803
40
2290
8,7
600
840
50
370
8,8
608
870
80
300
8,9
779
886
1710
160
9
814
902
350
160
9,1
846
320
9,2
864
180
9,3
886
220
9,4
895
90
9,5
904
933
90
10
924
40
62
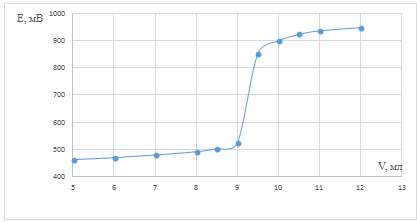
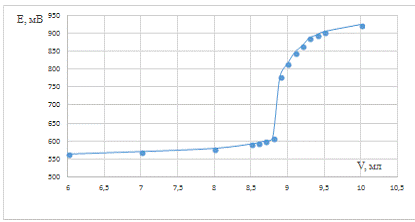
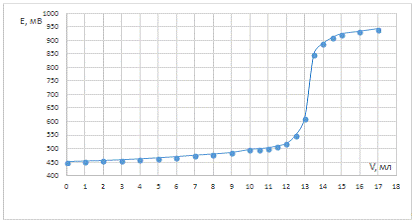
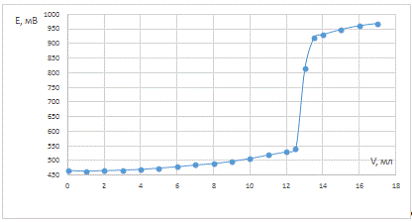
Рис. 1. Зависимость потенциала системы
от объема титранта для холостого опыта
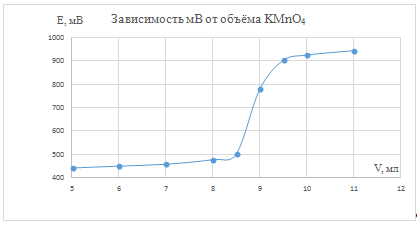
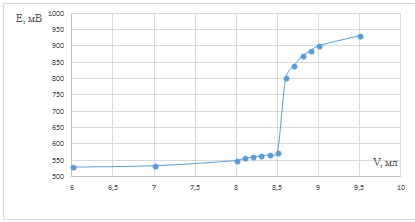
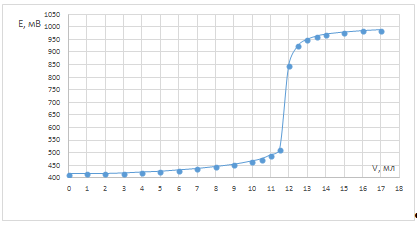
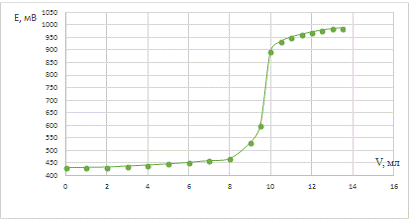
Рис. 2. Зависимость потенциала системы от
объема титранта для опыта после кипячения
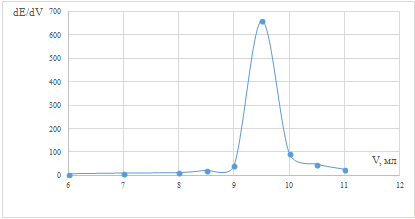
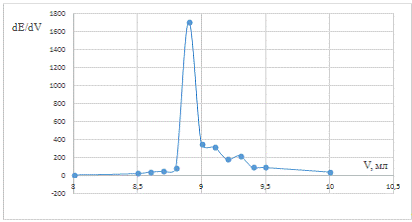
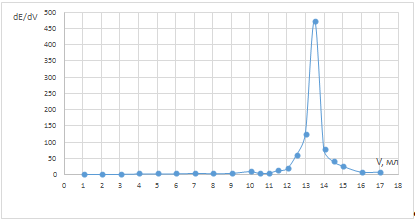
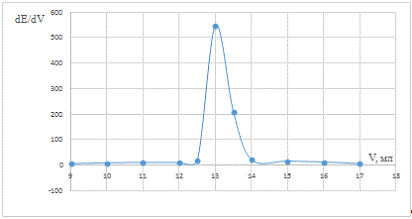
Рис. 3 Дифференциальная зависимость dE/dV
от объема титранта в холостой пробе
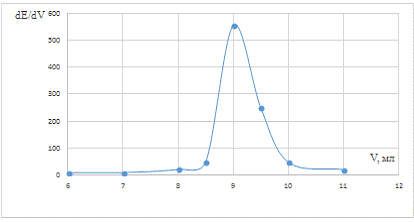
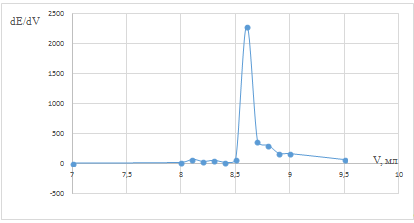
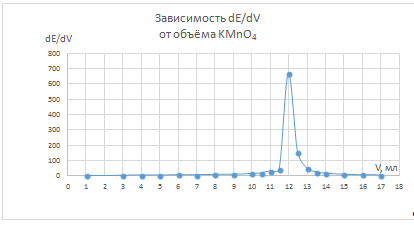
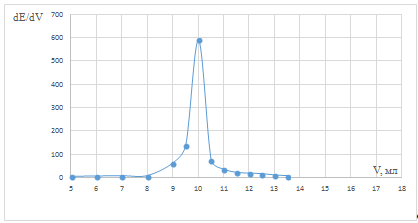
Рис. 4 Дифференциальная зависимость dE/dV
от объема титранта в пробе после кипячения
Таблица 2
Зависимость потенциала системы от объёма
титранта KMnO4
в
холостой пробе, пробе после кипячения и дифференциальные зависимости
при концентрации ClO3-
1 мг/л
V,
мл
E,
мВ
холост.
E,
мВ после кип.
dE/dV холост.
dE/dV после
кип.
0
342,5
378
1
343,9
379
1,4
1
2
345,8
381
1,9
2
3
346,6
382
0,8
1
4
348,2
383
1,6
1
5
349,1
384
0,9
1
6
351,1
385
2
1
7
355,8
386
4,7
1
8
359,3
389
3,5
3
9
366,1
393
6,8
4
10
370,2
400
4,1
7
11
378,9
408
8,7
8
12
394,4
433
15,5
25
12,5
437
8
13
410,1
514
15,7
154
13,5
426,6
893
33
758
14
450,9
932
48,6
78
14,5
784,5
952
667,2
40
15
850,9
965
132,8
26
15,5
876,4
51
16
905,7
975
58,6
10
16,5
919,7
28
17
925,3
982
11,2 18
930
988
4,7
6
19
933
992
3
4
20
942
9
21
948,8
6,8
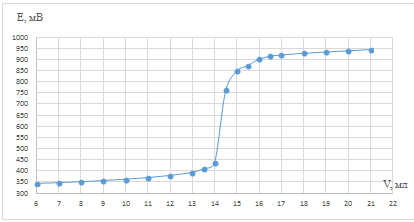
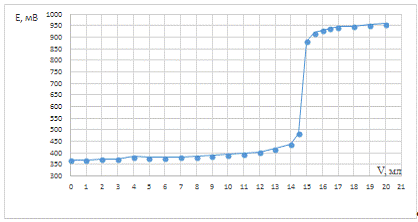
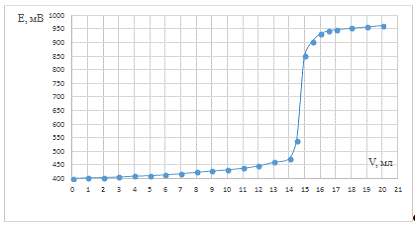
Рис. 5. Зависимость потенциала системы от
объема титранта для холостого опыта
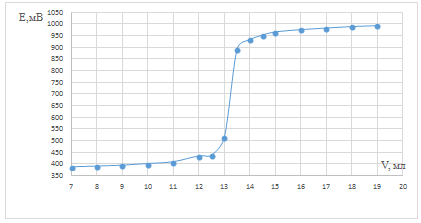
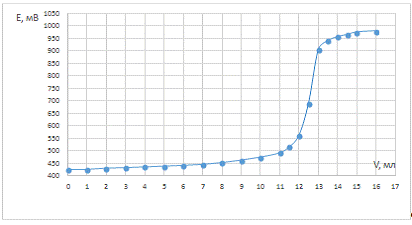
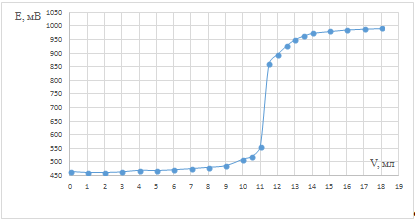
Рис. 6. Зависимость потенциала системы от
объема титранта для опыта после кипячения
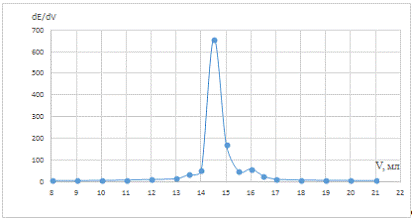
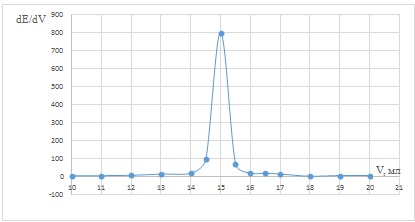
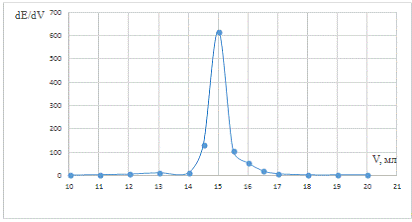
Рис. 7 Дифференциальная зависимость dE/dV
от объема титранта в холостой пробе
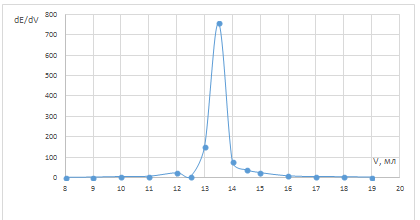
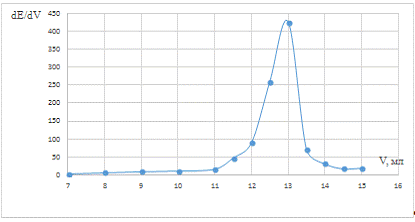
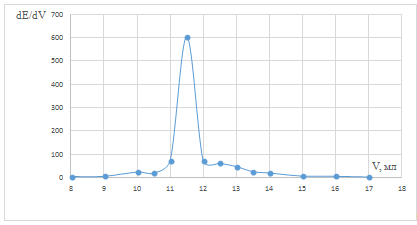
Рис. 8 Дифференциальная зависимость dE/dV
от объема титранта в пробе после кипячения
Таблица 3
Зависимость потенциала системы от объёма
титранта KMnO4
в
холостой пробе, пробе после кипячения и дифференциальные зависимости
при концентрации ClO3-
2 мг/л
V,
мл
E,
мВ
холост.
E,
мВ после кип.
dE/dV холост.
dE/dV после
кип.
0
452
416,5
1
454,4
417,6
2,4
1,1
2
456,3
417
1,9
-0,6
3
459
419,4
2,7
2,4
4
462,6
423
3,6
3,6
5
466,3
426
3,7
3
6
470,5
431,6
4,2
5,6
7
475,8
437
5,3
5,4
8
480,6
445
4,8
8
9
486
454
5,4
9
10
497
467,4
11
13,4
10,5
500
476
6
17,2
11
503
491,8
6
31,6
11,5
510
513,4
14
43,2
12
519,6
850
19,2
673,2
12,5
549,8
926
60,4
152
13
613
951
126,4
50
13,5
850,3
963,5
474,6
25
14
889,3
971,4
78
15,8
14,5
910,4
42,2
15
924,4
979,6
28
8,2
16
933,9
985,3
9,5
5,7
17
943,5
989,2
9,6
3,9
18
951,4
7,9
Рис. 9. Зависимость потенциала системы
от объема титранта для холостого опыта
Рис. 10. Зависимость потенциала системы от
объема титранта для опыта после кипячения
Рис. 11. Дифференциальная зависимость dE/dV
от объема титранта в холостой пробе
Рис. 12. Дифференциальная зависимость dE/dV
от объема титранта в пробе после кипячения
Таблица 4
Зависимость потенциала системы от объёма
титранта KMnO4
в
холостой пробе, пробе после кипячения и дифференциальные зависимости
при концентрации ClO3-
3 мг/л
V,
млE, мВ
холост.E,
мВ после кип.dE/dV холост.dE/dV после
кип.
0
368,3
424
1
370,2
425
1,9
1
2
372,5
430
2,3
5
3
374,6
432
2,1
2
4
384,3
435
9,7
3
5
380
438
-4,3
3
6
379,6
441
-0,4
3
7
381
445
1,4
4
8
385
452
4
7
9
388
462
3
10
10
392
474
4
12
11
397
491
5
17
11,5
515
48
12
404
560
7
90
12,5
690
260
13
418
903
14
426
13,5
939
72
14
437
955
19
32
14,5
485
964
96
18
15
885
974
800
20
15,5
920
70
16
930
979
20
5
16,5
939
18
17
946
14
18
948
2
19
954
6
20
960
6
21
964
4
Рис. 13. Зависимость потенциала системы от
объема титранта для холостого опыта
Рис. 14. Зависимость потенциала системы от
объема титранта для опыта после кипячения
Рис. 15. Дифференциальная зависимость dE/dV
от объема титранта в холостой пробе
Рис. 16. Дифференциальная зависимость dE/dV
от объема титранта в пробе после кипячения
Таблица 5
Зависимость потенциала системы от объёма
титранта KMnO4
в
холостой пробе, пробе после кипячения и дифференциальные зависимости
при концентрации ClO3-
4 мг/л
V,
млE, мВ
холост.E,
мВ после кип.dE/dV холост.dE/dV после
кип.
0
466,4
431
1
464,7
432,1
-1,7
1,1
2
465,9
433,4
1,2
1,3
3
467,8
437,5
1,9
4,1
4
470,5
441,6
2,7
4,1
5
474,8
446,1
4,3
4,5
6
479,3
452,1
4,5
6
7
485,4
459,2
6,1
7,1
8
490,3
467,1
4,9
7,9
9
497,7
530
7,4
62,9
9,5
600
140
10
507,7
895,6
10
591,2
10,5
933
74,8
11
519,6
950,8
11,9
35,6
11,5 21,2
12
531
970,7
11,4
18,6
12,5
541
978,7
20
16
13
816
983,8
550
10,2
13,5
920,4
987,5
208,8
7,4
14
931,3
21,8
15
948,6
17,3
16
961,8
13,2
17
969,12
7,32
18
974,1
4,98
Рис. 17. Зависимость потенциала системы от
объема титранта для холостого опыта
Рис. 18. Зависимость потенциала системы от
объема титранта для опыта после кипячения
Рис. 19. Дифференциальная зависимость dE/dV
от объема титранта в холостой пробе
Рис. 20. Дифференциальная зависимость dE/dV
от объема титранта в пробе после кипячения
Таблица 6
Зависимость потенциала системы от объёма
титранта KMnO4
в
холостой пробе, пробе после кипячения и дифференциальные зависимости
при концентрации ClO3-
5 мг/л
V,
млE, мВ
холост.E,
мВ после кип.dE/dV холост.dE/dV после
кип.
0
400
465
1
403
461
3
-4
2
404
461
1
0
3
406
463
2
2
4
409
469
3
6
5
411
468
2
-1
6
414
471
3
3
7
418
475
4
4
8
423
480
5
5
9
428
486
5
6
10
432
510
4
24
10,5
520
20
11
438
557
6
74
11,5
860
606
12
446
896
8
72
12,5
927
62
13
460
951
14
48
13,5
964
26
14
473
974
13
20
14,5
540
134
15
850
981
620
7
15,5
904
108
16
932
987
56
6
16,5
943
22
17
948
990
10
3
18
953
992
5
2
19
958
5
20
963
5
21
969
6
22
972
3
Рис. 21. Зависимость потенциала системы от
объема титранта для холостого опыта
Рис. 22. Зависимость потенциала системы от
объема титранта для опыта после кипячения
Рис. 23. Дифференциальная зависимость dE/dV
от объема титранта в холостой пробе
Рис. 24. Дифференциальная зависимость dE/dV
от объема титранта в пробе после кипячения
2.4.1 Результаты
Массовую концентрацию хлорат-ионов в исследуемых
растворах рассчитывали по формуле:
X X - Хлорат-ион, мг/л
V1 - Объём раствора
перманганата калия в холостом опыте, мл
V2 - Объём раствора
перманганата калия после кипячения, мл
С - молярная концентрация эквивалента
перманганата калия, моль/л
V0 -
Объём пробы, взятый для анализа, мл
,917 - Молярная масса эквивалента хлорат-иона,
г/моль
Результаты приведены в таблице 7.
Таблица 7
Введено
хлорат-ионов в исходный раствор, мг/л
Найдено
хлорат-ионов, мг/л
Отклонение
от добавки
Доверительный
интервал
мг/л
%
отн.
0,5
0,4
-0,08
16
0,2
1
1,2
0,16
16
0,3
2
1,8
-0,19
10
0,2
3
2,8
-0,22
7
0,4
4
4,2
0,18
4
0,3
5
4,9
-0,13
3
0,3
2.5 Определение хлорат-иона в речной
воде
Отобрали речную воду из реки Миасс. Пробу воды
отфильтровали через бумажный фильтр. Проводили перманганатометрическое
титрование с фиксированием потенциала системы по методике, описанной в п. 2.2.
Строили графики зависимости потенциала от объёма титранта. Для определения
точки эквивалентности рассчитывали и строили дифференциальную зависимость dE/dV
= f(V).
Результаты представлены в таблице 8. Проводили опыт в пяти параллелях.
Таблица 8
Зависимость потенциала системы от объёма
титранта KMnO4
в
холостой пробе, пробе после кипячения и дифференциальные зависимости
до и после кипячения речной воды.
V,
мл
E,
мВ
холост.
E,
мВ после кип.
dE/dV холост.
dE/dV после
кип.
0
435
422
1
443
426
8
4
2
445
429
2
3
3
450
432
5
3
4
455
437
5
5
5
461
442
6
5
6
468
450
7
8
7
478
458
10
8
8
490
478
12
20
8,5
501
502
22
48
9
522
780
42
556
9,5
852
904
660
248
10
899
927
94
46
10,5
923
48
11
936
946
26
19
12
948
12
Рис. 25. Зависимость потенциала системы от
объема титранта для холостого опыта
Рис. 26 Зависимость потенциала системы от
объема титранта для опыта после кипячения
Рис. 27. Дифференциальная зависимость dE/dV
от объема титранта в холостой пробе
Рис. 28. Дифференциальная зависимость dE/dV
от объема титранта в пробе после кипячения
2.5.1 Результаты
Нашли массовую концентрацию хлорат-ионов в
исследуемых пробах речной воды. Найденные концентрации приведены в таблице 9.
Таблица 9
№
Найденное
колличество хлорат-ионов, мг/л
1
1,39
2
0,70
3
0,70
4
1,39
5
0,70
Найденная концентрация хлорат ионов в реке
Миасс: С(СlO3-)
= 1,0± 0,2 мг/л
• Найденное
количество хлорат-ионов превышает ПДК для водных объектов. (ПДК 0,05мг/л)
• Найденное
количество хлорат-ионов не превышает ПДК для человека (ПДК 1г/л)
ВЫВОД
Апробирована методика титриметрического
определения хлорат-ионов в водных растворах, основанная на их восстановлении
сульфатом железа (Ⅱ) в сернокислой
среде при нагревании и последующим определении избытка восстановителя раствором
перманганата калия.
Методика позволяет определить не менее 0,5 мг/л
хлорат-ионов. Упаривание модельных растворов не привело к правильности
определения данных ионов.
Определили концентрацию хлорат-ионов в воде реки
Миасс, которая составила С(СlO3-)
= 1,0± 0,2 мг/л
СПИСОК ЛИТЕРАТУРЫ
1. Фрумина,
Н.С. Хлор [Текст]/ Н.С.Фрумина, Н.Ф.Лисенко, М.А.Чернова. - М., 1983. - 200 с.
. Перечень
рыбохозяйственных нормативов: предельно допустимых концентраций (ПДК) и
ориентировочно безопасных уровней воздействия (ОБУВ) вредных веществ для воды
водных объектов, имеющих рыбохозяйственное значение [Текст] // Издательство
ВНИРО - 1999 - С 235.
. Зефиров,
Н.С. Большая Российская энциклопедия [Текст] / Н.С. Зефиров, Н.Н. Кулов. - М.,
1999. - 783 с.
. Флис,
И.Е. Журнал аналитической химии [Текст] / И.Е. Флис, М.К. Быняева. - 1957 -743
с.
. Кольтгоф,
И.М. Объёмный анализ [Текст] / И.М. Кольтгоф, Р. Белчер, В.А. Стенгер, Дж.
Матсуяма. - М., 1964 - 840 с.
6. Свидетельство
№26-08 ФР.1.31.2008.01737 <http://www.prochrom.ru/ru/?idp=met&id=6>
Методика выполнения измерений массовой концентрации хлорит- и хлорат-ионов в
воде питьевой методом ионной хроматографии [Текст] опубл. 04.03.2008 -2с.
. Норкус,
П.К. Журнал аналитической химии [Текст]/ П.К. Норкус, Ю.Ю. Янкаускас - 1973
-2287с
8. Max, R.C. Annu. ISA Conf.
Proc. [Текст]
/ R.C. Max - 1966 - 67c
![]()