Материал: Расчет процесса получения алюминия
Длина: Lкож = Lш + 2∙20 + 2∙5=865+40+10=915
Ширина: Вкож = Вш + 2∙20 + 2∙5=335+50=385
Подина шахты ванны набирается из катодных блоков, угольной
подушки, теплоизоляционного слоя из кирпича и шамотной засыпки. Исходя из этого
высота кожуха составляет, см:
Нкож=Нш + hб + hуг + hкирп + hзac= 50+40+3+5∙6,5+2=127,5,
где hуг - толщина угольной подушки (обычно 3 - 5см); hкирп - толщина слоя из пяти рядов кирпичей по 6,5 см каждый; hзас - толщина слоя шамотной засыпки (обычно 2 - г - 5см).
Материальный расчет электролизера
В этом разделе определяют приход материалов в электролизер и выход материалов из него (расход материалов).
Расчет прихода материалов
Приход рассчитывается по расходу сырья на 1 кг алюминия и по
производительности электролизеров за 1 час. В табл.1 представлены данные по
расходу сырья, полученные на основании опыта эксплуатации электролизеров. В
расход обожженных анодов включены огарки, удаляемые из электролизера. Увеличенный
расход анодной массы и фторидов на электролизерах с верхним токоподводом
объясняется низким качеством анодов.
Таблица 1. Расход сырья (кг/кг алюминия) для различных типов
электролизеров.
Материал
Электролизеры с
Электролизеры с
самообжигающимися
обожженными
анодами
анодами (OA)
Аноды с боковым
токоподводом (БТ)
Аноды с верхним
токоподводом (ВТ)
Глинозем
1,92-1,93
1,92-1,93
1,92-1,93
Аноды
0,560
-
-
Анодная масса
-
0,540
0,590
Фториды
0,052
0,045
0,090
Производительность электролизера, т.е. количество алюминия,
образующегося за 1 час, рассчитывается, кг/час:
Р = I∙q∙ ηТ ∙10-5=155∙103∙0,335∙90∙10-5=46,733,
где q - электрохимический эквивалент, 0,335 г / (А∙ч).
Зная производительность электролизера и задавшись расходом
материалов (см. табл.1), можно рассчитать приход материалов в ванну, кг/час:
РAl2O3=pAl2O3∙P=1,92∙46,733=89,727;
Ра=ра∙Р=0,560∙46,733=26,170;
Рф= pф∙Р=0,052∙46,733=2,430,
где pAl2O3, ра, pф расходы глинозема, анода
(или анодной массы) и фторидов соответственно, кг/кг алюминия - на основе
данных табл.1).
Расчет расхода материалов
Выход материалов из электролизера состоит из следующих
статей. Алюминий. Количество полученного алюминия (Р) рассчитано ранее.
Анодные газы. Они образуются при окислении углерода анода и
состоят из двуокиси и моноокиси углерода. Содержание их в анодных газах в
мольных долях составляют 0,3-0,5 и 0,7-0,5 для СО и С02
соответственно. Содержания их заданы. Количества их, образующиеся за один час,
определяются, кг/час:
Рсо= (Nco∙Р∙28) / [
(2-Nco) ∙18] =0,475∙46,733∙28/27,45
=22,643, где Nco - мольная доля СО.
Рсо2= (Nco2∙P∙44) / [ (1+Nco2) ∙18] = (0,525∙46,733∙44)
/27,45, где Nco2 - мольная доля СО2.
Суммарная масса анодных газов, кг/час: Ра. г. =Рсо+Рсо2=
22,643+39,327=61,97.
Потери анодной массы (или обожженных анодов). Они
определяются как разность между приходом анодной массы (или обожженных анодов)
Ра и количеством израсходованного с анодными газами углерода. Потери
анодной массы, кг/час:
Ра. м. = Ра-Рс, где Рс=12
[ (Рсо/28) + (Рсо2/44)] =12 (0,809+0,894) =0,020 кг/час,
подставим в выражение для Ра. м.: Ра. м. =26,170-20,436=5,734
кг/час. Потери глинозема, кг/час:
∆РAl2O3= РAl2O3-РAl2O3 (теор) =89,727-88,279=1,448, где
РAl2O3 (теор) =102 Р /54 = 1,889Р= 88,279 кг/час.
Потери фторидов. Это потери в виде возгонов, а также на
пропитывание подины. Их принимают равными приходу фторидов Рф.
Полученные данные сводятся в таблицу табл.2.
Таблица 2. Материальный баланс электролизера.
Приход
кг/час
%
Расход
кг/час
%
Глинозем
89,727
75,83
Алюминий
46,733
39,49
Фториды
2,430
2,05
Анодные газы
61,970
52,38
Анодная масса
(или обожженные аноды)
26,170
22,12
Потери
глинозема
1,448
1,22
Потери фторидов
2,430
2,05
Потери анодной
массы (обожженных анодов)
5,734
4,85
Невязка
+0,012
0,01
Итого
118,327
100,00
Итого
118,327
100,00
Энергетический расчет фактически является расчетом теплового
баланса. Электролизер можно представить, как систему, которая снабжается теплом
за счет прохождения тока (Qэл) и сгорания анода Qaн). Система расходует
тепло на разложение глинозема (Qpaзл), теряет его с вылитым металлом (Qмeт) и с отходящими газами (Qгaз), а также расходует
тепло на потери в окружающее пространство (Qn). Таким образом,
уравнение теплового баланса может быть записано как Qэл + Qaн = Qpaзл + Qмeт + Qгaз + Qn
Все входящие в это уравнение величины рассчитываются
применительно к одному часу работы электролизера.
Приход тепла.
Приход тепла от прохождения электрического тока определяется,
кДж:
Qэл=3,6∙I∙Uгр,
где I - сила тока, А; Uгр - греющее напряжение, В. Это напряжение
слагается из падений напряжения на аноде, на подине, в электролите, от анодных
эффектов, а также напряжения разложения. Точное определение его затруднительно.
По практическим данным можно принять для всех типов
электролизеров Uгр = 0,89∙Ucp=3,757 В, Qэл=3,6∙155∙103
∙3,757=2096406 кДж
Приход тепла от окисления углерода анода определяется, кДж:
Qaн= Р′со∙∆Н?298 (со) + Р′со2∙∆Н?298 (со2),
где Р′со и Р′со2 соответственно
числа молей СО и СО2, образовавшиеся за один час работы, находятся
по формулам:
Р′со=Рсо103/М (СО)
=808,579, Р′со2=Рсо2103/М (СО2)
=893,795.
∆Н?298 (со) и ∆Н?298 (со2) тепловые эффекты реакций
образования оксида и моноксида углерода, кДж/моль. Эти данные имеются во многих
справочниках, например, в [2].
Qaн=808,579∙110,5+893,795∙393,51=441076,3
кДж.
Расход тепла. Расход тепла на разложение глинозема
определяется, кДж:
Qpaзл=Р′Al2O3 (теор) ∙ ∆Н ᵒ298
(Al2O3),
где
Р′Al2O3 (теор) =865,48 количество молей Al2O3, затрачиваемое на
получение Р кг алюминия; ∆Н ᵒ298 (Al2O3) - тепловой эффект реакции
образования оксида алюминия, кДж/моль (его также определяют по справочникам,
например, по [2]).
Qpaзл=865,48∙1675=1449679 кДж.
Расход тепла с вылитым металлом
Эта статья рассчитывается исходя из условия, что количество
вылитого алюминия соответствует количеству наработанного в то же время металла.
Температура выливаемого алюминия составляет 950-960°С. Известно, что для
алюминия разность энтальпий (∆Н?Т - ∆Н ?298), кал/моль, равна при
1200°К 8730, а при 1300°К 9430. При расчете необходимо, задавшись температурой
выливаемого алюминия, определить разность энтальпий в привычной размерности
(кДж/моль).
Выбираем Т=950°С=1223°К. Тогда (9430-8730) / (1300-1200) =7,
7∙ (1223-1200) =161, 8730+161=8891 кал/моль.
Решим пропорцию, найдем разность энтальпий
,891 ккал/моль - х,
ккал/моль - 4,1868 кДж/моль
х=37,225 кДж/моль.
Расход тепла определяется, кДж: где Р' = Р103/М (Al2O3) =1730,852 - количество
молей алюминия, нарабатываемых за один час, тогда Qмeт=64430,966 кДж.
Расход тепла с отходящими анодными газами
По практическим данным температура отходящих газов равна
550-600°С. Значение температуры задается. Также принимается, что подсос воздуха
отсутствует и, следовательно, отходящие газы состоят только из диоксида и
моноксида углерода. Разность энтальпий этих газов при заданной температуре и
температуре окружающей среды определяется из уравнения теплоемкости С?р=а + bТ + с′/Т2,
коэффициенты которого приведены ниже (табл.3) [2].
Таблица 3. Коэффициенты уравнения теплоемкости, Дж/
(моль-град)
Вещество
а
b∙1О3
с'∙10-5
СО
28,41
4,10
-0,46
СО 2
44,14
9,04
-8,53
Разность энтальпий определяется:
Н?Т - Н ?298= Для СО: Н?Т - Н
?298=14915,25+1206,476 - 100=16021,721 Дж/моль. Для СО2:
Н?Т - Н ?298=23173,5+2660,133-1876,6=
23957,033 Дж/моль.
Следует помнить, что разность энтальпий при подставлении
коэффициентов из табл.3 будет иметь размерность Дж/моль. Расход тепла
определяется, кДж:
Qгaз= [Р′со (Н?Т - Н ?298) CO+ Р′со2 (Н?Т - Н ?298) CO2] /1000=34369,
где Р′со и Р′со2 - количества
молей моноксида и диоксида углерода соответственно, образовавшиеся за один час.
Потери тепла в окружающее пространство.
Точный расчет этой статьи затруднен из-за сложной конфигурации
теплоотдающих поверхностей электролизера, различными условиями движения воздуха
вдоль его элементов. Поэтому часто для упрощения тепловые потери с поверхности
электролизера в окружающее пространство определяют по разности, кДж:
Qп = (Qэл + Qaн) - (Qpaзл + Qмeт + Qгaз +
Qn) =2537482,3 -
1449679-64430,966-34369=989003,334.
Результаты расчета заносятся в таблицу 4.
Таблица 4. Тепловой баланс электролизера.
Приход тепла
кДж
%
Расход тепла
кДж
%
От прохождения
электрического тока
2096406
82,62
На разложение
глинозема
1449679
57,131
От сгорания
анода
441076,3
17,38
С вылитым
алюминием
64430,966
2,539
С отходящими
газами
34369
1,354
С поверхности
электролизера
989003,334
38,976
Итого
2537482,3
100,00
Итого
100,00
[1]
Крутский, Ю.Л. Расчёт процесса получения алюминия. Методические указания к
выполнению курсовой работы по курсу "Общая химическая технология" для
студентов механико-технологического факультета, по специальностям 240801,
240802 и других специальностей химико-технологического профиля. - Новосибирск,
2010.
[2]
Краткий справочник физико-химических величин. /Под ред. К.П. Мищенко, И.А.
Равделя. Л.: Химия, 1974.
[3]
Технология кальцирования соды, щелочей и глинозема. Текс лекций. / Крашенников
С.А., Греф Т.С. - Москва, МХТИ им.Д.И. Менделеева, 1988г.
[4]
Троицкий И.А., Железнов В.А. Металлургия алюминия. М.: Металлургия, 1984.
Список
электронных источников:
#"793160.files/image008.gif">
Рис. 1
Анодное устройство состоит из анодной рамы 4, опирающейся
через домкраты на катодных кожух 1 или отдельно стоящие стойки.
На анодной раме с двух сторон расположена анодная ошиновка 5,
к котор зажимами прижимается токоподводящая штанга 3 с анодом 2.
Принципиальная схема самообжигающегося анода с боковым
токоподводом приведена на рис.2. Нижняя его часть под действием высокой
температуры cпекается
в сплошной электропроводный блок 1. Выше конуса спекания находится зона 2
полуобожженная тестообразная масса. Верхняя зона 3 - жидкая анодная масса.
- анодная рама;
- ребра из швеллеров;
- токоподводящие штыри;
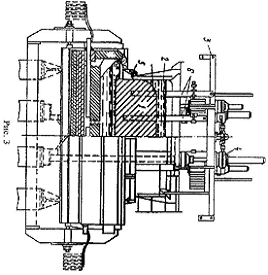
- серьги (или клинья). Схема электролизера с верхним токоподводом приведена на
рис.3. Здесь анод также самообжигающийся. Анодное устройство электролизера с
верхним токоподводом (ВТ) представляет собой угольный анод 1, расположенный
внутри анодного кожуха 2, который подвешивается к анодной раме 3 с помощью
вспомогательных домкратов 4. Анодная рама висит на основных домкратах, которые
опираются на катодный кожух или специальные стойки.
Подвод тока осуществляется штырями 6 5 - газосборный колокол.
Энергетический
расчет электролизера
![]()
![]() = a (T - 298) + b/2 (Т2 - 2982) + с' [ (1/298) - (1/T)]
= a (T - 298) + b/2 (Т2 - 2982) + с' [ (1/298) - (1/T)]
Список
литературы