Материал: Производство карбамида
Таким образом, чем больше количество исходных веществ в постоянном объеме, т. е. плотность заполнения реактора, тем выход карбамида возрастает, потому что, во - первых, увеличивается давление и тем самым меньше разлагается карбамид аммония на газообразные аммиак и двуокись углерода. Во - вторых, процесс протекает с образованием двух фаз: жидкой и газовой. При этом основной синтез карбамида происходит в жидкой фазе.
Позднее определили, что выход карбамида находиться в прямолинейной зависимости от обратной величины плотности заполнения реактора [7].
Что касается влияние температуры на синтез
карбамида, то такие ученые как Фихтер и Беккер нашли, что при плотности
заполнения реактора 0,11 г/см3 выход карбамида с ростом температуры вначале
возрастает, достигает максимально величины при 135оС, а затем уменьшается.
Позднее было установлено, что оптимальная температура процесса возрастает с
увеличением плотности заполнения реактора [7].
.2Термодинамика синтеза карбамида
.2.1 Равновесие жидкость - газ при синтезе
Для термодинамического анализа процесса синтеза карбамида, кроме сведений о зависимости степени превращения двуокиси углерода ( или карбамата аммония) в карбамид от различных факторов, необходимы также сведения о распределении компонентов между сосуществующими фазами при различных температурах, давлениях, плотностях заполнения реактора и составах исходной смеси. Четырехкомпонентная система NH3-CO2-H2O-CO(NH2)2 в условиях, соответствующих промышленным, имеет две фазы [7]: жидкую и твердую, т. е., из курса Физической химии, согласно правилу фаз Гиббса, система имеет три степени свободы (С=3). Составы равновесных жидкой и газовой фаз при стехиометрическом соотношении аммиака, двуокиси углерода и воды в зависимости от плотности заполнения реактора представлены на рис. 1. Как видно из рис. 1., что при увеличении плотности заполнения реактора до 0,2 г/см3 приводит к возрастанию концентрации карбамида в жидкой фазе, и при дальнейшем увеличении плотности заполнения реактора концентрация практически становиться постоянной
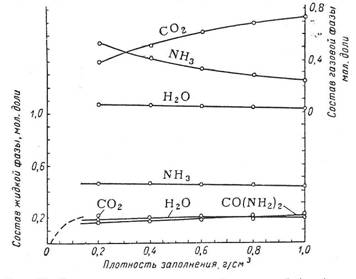
Рис. 1. Составы равновесных жидкой и газовой фаз
(мольные доли) системы NH3-CO2-H2O-CO(NH2)2 при 160о С и стехиометрическом
соотношении компонентов [7].
Так же можно добавить, что в жидкой фазе
появляется избыток аммиака, а в газовой фазе напротив, всегда избыток CO2 [7].
.2.2Равновесное давление при синтезе
При нагревании карбамат аммония разлагается с выделением газообразных NH3 и CO2 [7]. Зависимость давления диссоциации карбамата аммония, т. е. равновесного давления смеси паров аммиака и двуокиси углерода над твердым или жидким карбаматом аммония, от температуры рис. 2.
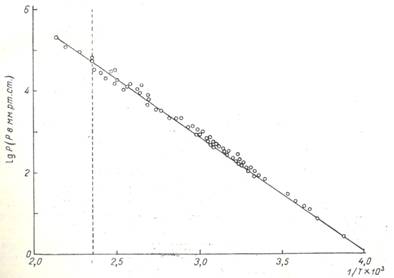
Рис. 2. Полулогарифмическая анаморфоза
зависимости давления диссоциации карбамата аммония (Р) от температуры (Т), по
данным различных авторов [7]. Пунктир - температура плавления карбамата аммония
Следует заметить, что при повышенных
температурах результаты измерений давления пара над карбаматом аммония менее
надежны, потому что последний дегидратируется с образованием карбамида.
Зависимость давления пара над карбаматом аммония от температуры описывается
уравнением (1.). Уравнение хорошо описывает опытные данные в интервале
температур 283 - 355 oK [7].
![]() (1.)
(1.)
Где P - давление, мм рт. ст.;- абсолютная температура, oK.
Так же равновесное давление газовой смеси над плавом при синтезе карбамида из карбамата аммония без добавок других компонентов (NH3, CO2 или H2O) зависит не только от температуры, но и от плотности загрузки автоклава.
Влияние избытка NH3 и CO2 на равновесное давление обуславливается
тем, что доставка CO2 к карбанату аммония
способствует повышению равновесного давления, а добавка NH3 сначала снижает, а
затем повышает его. При этом с повышением температуры минимум давления
наблюдается при несколько большом избытке аммиака и для разных температур
отвечает соотношению 2,4 - 2,5 моль NH3 на 1 моль CO2 [7].
.2.3Тепловой баланс процесса синтеза
В практике проектирования весьма важен расчет
теплового баланса колонны синтеза, необходимый для определения температуры
синтеза и ее регулирования. Разработана схема теплового баланса процесса
синтеза в присутствии избыточного аммиака, но без избытка воды. В этой схеме
аммиак условно подразделяется на стехиометрический, взаимодействующий с
двуокисью углерода с образованием сначала карбамата аммония, а затем карбамида,
и на избыточный, непосредственно не участвующий в реакции, но обеспечивающий
своим присутствием высокую степень превращения стехиометрического аммиака (или
двуокиси углерода) в карбамид. По условию схемы стехиометрический аммиак
(жидкий) сначала охлаждается, затем дросселируется до 1 ат. и превращается в
газ. Двуокись углерода (жидкая) дросселируется от заданного давления до 1 ат. И
превращается в газ при нормальной температуре. Далее карбамат подогревается до
температуры плавления при давлении синтеза, плавиться и дегидратируется, после
чего продукты реакции (вода и карбамид) и непрореагировавший карбамат аммония
подогреваются от температуры плавления карбамата аммония до температуры
синтеза. Избыточный аммиак (жидкий) подогревается от исходной температуры до
критической, превращается в газ, а затем сжимается (растворяется) при
критической температуре и давлении синтеза в стехиометрической смеси карбамата
аммония, воды и карбамида. Далее сжиженный избыточный аммиак подогревается от
критической температуры до температуры синтеза при давлении синтеза [7].
1.3Кинетика синтеза
Кинетика синтеза карбамида изучена как в статических условиях при постоянном объеме, так и в динамических условиях (в порточных системах) при постоянном давлении. При исследовании в статических условиях в качестве исходного вещества обычно применяют карбамат аммония, к которому добавляют различные количества аммиака, двуокись углерода или воды. Смесь нагревают до заданной температуры в стальных бомбах или стеклянных ампулах. Для прекращения реакции в заданный момент времени реакционный сосуд резко охлаждают [7].
Другой способ изучения кинетики карбамида при постоянном объеме заключается в том, что аммиак и двуокись углерода под давлением загружают в автоклав и нагревают смесь до заданной температуры. В этом случае о протекании процесса судят по изменению давления в автоклаве [7].
Для изучения кинетики синтеза карбамида в потоке аммиака и двуокиси углерода непрерывно подают под давлением в проточную трубу или колонну и определяют выход карбамида при различных скоростях подачи реагентов [7].
Так как синтез карбамида - двухфазный процесс и ряд фактов свидетельствует о то, что образование карбамида может проходить как в газовой, так и в жидкой фазах, то на кинетику синтеза должно оказывать влияние перемешивание фаз [7].
Следует отметить, что в промышленных условиях
синтеза (200 ат, молярное соотношение L = 4.200оС) при взаимодействии аммиака и
двуокиси углерода в колонне несмотря на то, что в начале процесса карбамат
аммони не может образоваться (его давление диссоциации при этих условиях 550
ат) и синтез протекает в газовой фазе, уже первые порции образующихся при
реакции карбамида и воды дают жидкую фазу [7].
1.4 Представления о химизме синтеза
Фаусит, выдерживая водные растворы карбамида при 100оС, отметил медленный переход его в углеаммонийные соли. Например, за 20 ч. Превращалось всего 16% карбамида. В то же время при этих условиях за 2 - 3 ч. завершался процесс изомеризации карбамида в цианат аммония по реакции [7]:
(NH2)2 D NH4NCO
Процесс превращения карбамида в цианат легко происходит только в растворах; при нагревании твердого карбамида до 110 оС этого не наблюдается. Напротив, цианат аммония легко превращается в карбамид даже при низких температурах, и это дает основание полагать, что при разложении карбамида в водных растворах цианат является обязательным промежуточным продуктом. С другой стороны, можно предположить, что и при образовании карбамида из углеаммонийных солей цианат также является обязательным промежуточным продуктом [7].
Впервые предложение о цианатном механизме
образования карбамида из карбамата аммония было высказано Вернером. Он считал,
что карбамат аммония при нагревании разлагается на аммиак и карбаминовую
кислоту, которая в свою очередь, превращается в циановую кислоту и воду.
Циановая кислота, взаимодействую с аммиаком, образует цианат аммония и далее
карбамид. Указанные три стадии можно записать в виде следующих уравнений [7]:
![]() (I)
(I)
![]() (II)
(II)
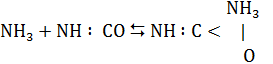 (III)
(III)
Имеются лишь сведения о реакции (III). Процесс перехода цианата аммония в карбамид ен и происходит с выделением 7500 кал / моль тепла в растворе и 4900 кал / моль в твердом состоянии. Эта реакция в растворе является бимолекулярной. При возрастании температуры скорость реакции быстро увеличивается, а равновесие сдвигается в сторону образования цианита. Основываясь на этих данных вычислил энергию активации реакции превращения цианата в карбамид, которая оказалась равной 23170 кал / моль. Следует отметить, что эта реакция аномальна быстрая с высокой энтропией активации. Таким образом реакция (III) не может лимитировать скорость образования карбамида. Что касается первых двух реакций, то они не изучены. Поэтому доказательств правильности этого механизма пока еще нет [7].
Рассмотренная выше теория кинетики синтеза карбамида и теории, которые не затронуты в реферате, приносят определенную практическую пользу, так как позволяют вычислить производительность колонн синтеза и предсказать роль ряда параметров при интенсификации процесса [7].
Что касается влияния давления на кинетику синтеза карбамида, то можно отметить то, что давление является мощным фактором интенсификации процесса синтеза карбамида, что подтверждается практикой. Однако при повышении давления может в конце концов полностью перевести процесс в жидкую фазу, и дальнейшее его увеличение окажется нецелесообразным. Подтвердил роль давления в кинетики синтеза карбамида Альтшулер [7].
Другим важным фактором, который пока не удается объяснить с помощью существующих теорий, является наличие обнаруженного Ченоветом максимума подачи реагентов. Следует отметить, что при более высоких давлениях синтеза (~400 ат.) указанный максимум исчезает [7].
.Схема производства карбамида
.1 Блок - схема производства карбамида и ее
описание
Блок - схема промышленного производства
карбамида приведена на рис. 3.
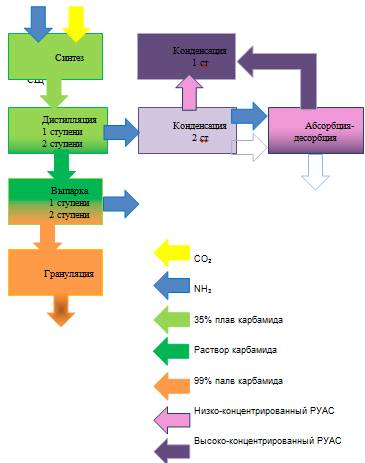
Рис. 3. Блок - схема производства карбамида [8].
На рис. 3. Изображена блок - схема синтеза карбамида с двухступенчатой дистилляцией плава и жидкостным рециклом.
Исходные сырьевые компоненты являются NH3, CO2 и
РУАС (раствор углеаммонийных солей), которые поступают на отделение синтеза,
где при температуре T = 185 - 190оС и давлении P = 20 МПа в две ступени
протекает реакция образования плава карбамида. Плавом называется смесь,
содержащая менее 30% воды [8].
NH3 + CO2 = NH2COONH4 + Q
NH2COONH4
= (NH2)2CO
+ H2O
- Q
Поскольку обе реакции обратимы, то после синтеза в выходящем плаве содержатся [8]:
целевой продукт - (NH2)2CO (карбамид);
непрореагировавшие сырьевые компоненты - NH3 (аммиак) и CO2 (двуокись углерода);
побочные продукты и промежуточный продукт NH2COONH4 (карбамат) [8].
Плав поступает на отделение дистилляции с целью извлечения непрореагировавшего сырья NH3 и CO2. Дистилляция протекает в две ступени, в ходе которых постоянной увеличивается концентрация карбамида благодаря разложению карбамата (реакция 2) и удалению непрореагировавших сырьевых компонентов [8].
После отделения дистилляция 70% - ый раствор карбамида поступает на выпарку для удаления воды. Выпарка проходит в две ступени. На первой ступени концентрация карбамида возрастает до 92 - 95%, а на второй ступени до 99,5 - 99,8%. Плав карбамида направляется на грануляцию с целью образования твердого продукта - гранул карбамида [8].
К вспомогательным этапам синтеза так же относятся конденсация первой и второй ступени, а также отделение абсорбции - десорбции [8].
Непрореагировавшие газообразные сырьевые компоненты поступают на отделение конденсации образования жидкого раствора углеаммонийных солей (NH4HCO3, (NH4)2CO3, NH4OH). Несконденсировавшиеся сырьевые компоненты направляются на отделение абсорбции - десорбции и удаления инертных казов и избыточной воды [8].
.2Технологическая схема производства карбамида
Полученный в виде плава карбамид, содержащий в своем составе карбамид, карбамат, аммиак, карбонаты аммония и воду, подвергаются дистилляции. При термообработке плава разлагают содержащийся в нем карбамат и карбонаты и извлекают аммиак и двуокись углерода, после чего водный раствор карбамида перерабатывают в твердый продукт [3].
Существующие способы получения карбамида различаются в основном методами улавливания и использования газов дистилляции плава - смеси аммиака с двуокисью углерода, степень превращения которых в карбамид не превышает соответственно 50 - 70% [3].
Современные производства карбамида большой мощности работают по замкнутым системам, по которым продукт дистилляции полностью возращают на синтез карбамида [3].
Рецикуляцию газов дистилляции осуществляют двумя способами:
С газовым рециклом - продукты дистилляции полностью возвращаются в газообразной форме;
С частичным или полным жидкостным рециклом - в цикл возвращаются жидкий аммиак или растворы (суспензии) углеаммонийных солей [3].
Непосредственный возврат в систему синтеза газовой смеси (аммиак и двуокись углерода), получаемой в процессе дистилляции, требует ее сжатия до давления синтеза при высокой температуре во избежание процесса образования твердого карбамата аммония. В способах с газовым рециклом предварительно разделяют газы дистилляции, обрабатывая их селективными абсорбентами для извлечения аммиака и двуокиси углерода. Для этого в абсорбете газы промывают раствором нитрата карбпмида и извлекают аммиак, а оставшийся диоксид углерода в газовой форме вновь используют. В процессе регенирации поглотительного раствора в десорбере выделяют аммиак, который возвращают в цикл синтеза [3].
Если применяемый абсорбент моноэтаноламин NH2CH2CH2OH, то из газов дистилляции извлекают двуокись углерода, а остающийся газообразный аммиак сжижают и возвращают в цикл. В процессе нагревания вытекающего из абсорбера поглотителя из него десорбируют диоксид углерода, а регенерированный раствор вновь направляют в абсорбент [3].
.2.1Получение карбамида с полным жидкостным рециклом
Одним из вариантов получения карбамида с
двухступенчатой дистилляцией плава и жидкостным рециклом приведен на рис. 4.
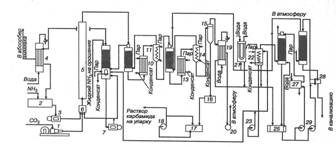
Рис. 4. Схема получения карбамида с жидкостным рециклом (синтез и дистилляция сплава) [3]:
- четырехступенчатый компрессор для диоксида
углерода; 2 - танк жидкого аммиака; 3 - плунжерный насос для аммиака; 4 -
конденсатор I ступени; 5 - колонна синтеза; 6 - смеситель; 7 - плунжерный насос;
8 - промывная колонна; 9 - ректификационная колонна I ступени; 10 -
подогреватель I ступени; 11 - сепаратор I ступени; 12 - ректификационная
колонна II ступени; 13 - подогреватель II ступени; 14 - сепаратор II ступени;
15 - вакуум-испаритель; 16 - сборник раствора карбамида; 17 - маслоотделитель;
18 - центробежный насос; 19 - конденсатор; 20 - вакуум-насос; 21 - конденсатор
II ступени; 22 - резервуар; 23 - центробежный насос; 24 - абсорбер; 25 -
сборник раствора карбонатов аммония; 26 - десорбер; 27 - холодильник; 28 -
теплообменник; 29 - центробежные насосы .