Материал: Принцип действия аккумуляторов
Снижению газовыделения способствуют и рекомендуемые для герметизированных аккумуляторов режимы заряда, при которых ток понижается по мере их заряжения.
И все-таки все реализованные варианты безуходного свинцово-кислотного аккумулятора оснащены клапаном, который время от времени открывается для сброса излишнего количества газа, главным образом водорода. Именно поэтому аккумулятор называется не герметичным, а герметизированным.
Герметизированные свинцово-кислотные аккумуляторные
батареи емкостью до 10-20 Ач применяются как источники питания для
разнообразной портативной аппаратуры и инструментов в тех случаях, когда масса
не является определяющим критерием для выбора источника тока, а также в
системах бесперебойного питания, телекоммуникаций, информационных системах, для
аварийного оборудования и т.д., где они работают в буферном режиме. Схема
строения простейшего свинцово- кислотного аккумулятора представлена на рисунке
2. [4]
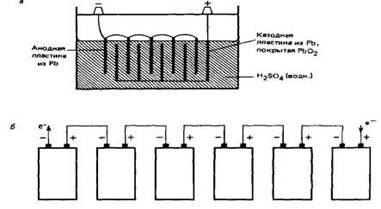
Рис 2. Свинцовые аккумуляторы. а)
свинцовый аккумулятор-блок аккумуляторной батареи; б) схема автомобильной
батареи.
Никель-кадмиевые аккумуляторы
(Ni-Cd).

Рис 3. Никель кадмиевый аккумулятор в быту
Щелочные никель-кадмиевые аккумуляторы (Ni-Cd) были изобретены еще в 1899 г. Вальдмаром Юнгнером. Однако материалы для производства таких аккумуляторов стоили дороже материалов для производства аккумуляторов других типов, и поэтому в то время широкого использования они не нашли. Только в 1932 г. была разработана технология нанесения активного материала пластин путем осаждения на губчатый (пористый) покрытый никелем электрод. А в 1947 г. стали известны работы над созданием герметичных никель-кадмиевых аккумуляторов, в которых была осуществлена возможность рекомбинации газов, выделявшихся в процессе заряда, без их отвода. Конечным результатом этих разработок и стало появление герметичных никель-кадмиевых аккумуляторных батарей, используемых и в настоящее время.Cd аккумуляторы любят быстрый заряд, медленный разряд до состояния полного разряда и подзарядку импульсами тока, в то время как батареи других типов предпочитают частичный разряд и умеренные токи нагрузки. Это тип аккумуляторов, которые способны работать в самых жестких условиях.
Для никель-кадмиевых аккумуляторов крайне необходим полный периодический разряд: если его не делать, на пластинах элементов формируются крупные кристаллы, значительно снижающие их емкость (так называемый "эффект памяти").
Реагентами в никель-кадмиевых аккумуляторах служат гидроксид никеля и кадмий, электролитом - раствор КОН, поэтому они именуются щелочными аккумуляторами. Существуют три основных вида никель-кадмиевых аккумуляторов: негерметичные с ламельными (ламельные аккумуляторы) и спеченными электродами (безламельные аккумуляторы) и герметичные. Наиболее дешевые ламельные никель-кадмиевые аккумуляторы характеризуются плоской разрядной кривой, высокими ресурсом и прочностью, но не низкой удельной энергией. Удельная энергия, скорость разряда Ni-Cd аккумуляторов со спеченными электродами выше, они работоспособны при низких температурах, но дороже, характеризуются эффектом памяти и способностью к тепловому разгону.
Применяются никель-кадмиевые аккумуляторы для питания шахтных электровозов, подъемников, стационарного оборудования, средств связи и электронных приборов, для запуска дизелей и авиационных двигателей и т.п.
Герметичные Ni-Cd аккумуляторы характеризуются горизонтальной разрядной кривой, высокими скоростями разряда и способностью действовать при низких температурах, но они дороже герметизированных свинцовых аккумуляторов и характеризуются эффектом памяти. Применялись для питания портативной аппаратуры (сотовых телефонов, магнитофонов, компьютеров и т.д.), бытовых приборов, игрушек и т.д. Недостатком никель-кадмиевых аккумуляторов является применение токсичного кадмия. [5]
Преимущества Ni-Cd аккумуляторных
батарей
возможность быстрого и простого заряда, даже после длительного хранения аккумулятора;
большое количество циклов заряд/разряд: при правильной эксплуатации - более 1000 циклов;
хорошая нагрузочная способность и возможность эксплуатации при низких температурах;
продолжительные сроки хранения при любой степени заряда;
сохранение стандартной емкости при низких температурах;
наибольшая приспособленность для использования в жестких условиях эксплуатации;
низкая стоимость;
Недостатки Ni-Cd аккумуляторных батарей:
относительно низкая по сравнению с другими типами аккумуляторных батарей энергетическая плотность;
присущий этим аккумуляторам эффект памяти и необходимость проведения периодических работ по его устранению;
токсичность применяемых материалов, что отрицательно сказывается на экологии, и некоторые страны ограничивают использование аккумуляторов этого типа;
относительно высокий саморазряд - после хранения необходим цикл заряда.
Основные электрохимические процессы
Ni-Cd аккумулятора
Основной процесс, происходящий на положительном оксидно-никелевом электроде в цикле заряда-разряда аккумуляторов, описывается следующим образом:
(OH)2 + OH- → NiOOH + H2O
+ e- (заряд) NiOOH + H2O + e- → Ni(OH)2
+ OH- (разряд)
На отрицательном кадмиевом электроде аккумулятора проходит реакция:
(OH)2 + 2e- → Cd + 2OH-
(заряд) Cd + 2OH- → Cd(OH)2 + 2e-
(разряд)
Общая реакция в Ni-Cd аккумуляторе имеет вид:
Ni(OH)2 + Cd(OH)2 → 2NiOOH
+ Cd + 2H2O (заряд) 2NiOOH + Cd + 2H2O → 2Ni(OH)2
+ Cd(OH)2 (разряд)
При перезаряде никель-кадмиевых аккумуляторов на
положительном электроде идет побочный процесс выделения кислорода:
OH- → 1/2O2 + H2O
+ 2e- (перезаряд) [6]
Кислород сквозь пористый сепаратор достигает
отрицательного электрода и восстанавливается на нем:
/2O2 + Cd + H2O → Cd(OH)2
(перезаряд)
Последняя реакция воплощает в жизнь замкнутый
кислородный цикл и обеспечивает стабилизацию давления в герметичном
никель-кадмиевом аккумуляторе при его перезаряде. Нужно отметить, что давление
в аккумуляторе определяется не только скоростями протекания указанных реакций,
но, главным образом, скоростью доставки кислорода от положительного электрода к
отрицательному. Так же, при перезаряде отрицательного кадмиевого электрода
может иметь место реакция выделения водорода:
H2O + e- → OH-
+ 1/2H2
который окисляется на оксидно-никелевом электроде в соответствии с реакцией:
+ 1/2H2 → Ni(OH)2
Реакция образования водорода опасна для герметичного
аккумулятора, так как она может привести к накоплению водорода из-за низкой скорости
реакции его поглощения. Для того чтобы в стандартной ситуации, условий для
протекания реакции выделения водорода не возникало, в герметичном аккумуляторе
емкость отрицательного электрода объемно заметно превосходит емкость
положительного. Поэтому емкость герметичного никель-кадмиевого аккумулятора
определяется емкостью его положительного оксидно-никелевого электрода.[7]
Механизмы электродных реакций Ni-Cd аккумулятора
Положительный электрод. Исходный гидроксид никеля может существовать в двух формах: α- и β-Ni(OH)2, отличающихся степенью гидратации и плотностью. В разряженном электроде могут присутствовать обе формы Ni(OH)2. При заряде β-Ni(OH)2 переходит в β-NiOOH (при небольших изменениях кристаллической решетки вещества). На последней стадии заряда может образовываться γ-NiOOH. Соотношение β- и γ-фаз NiOOH зависит от условий заряда. γ-Фаза образуется при больших скоростях заряда и/или при существенных перезарядах. Ее образование приводит к коренной перестройке структуры оксидов. Плотность β-NiOOH равна 4,15 г/см3, плотность γ-NiOOH - 3,85 г/см3, поэтому при существенном перезаряде при образовании оксидов высшей валентности объем активной массы оксидно-никелевого электрода изменяется.
Электрохимическое поведение двух форм гидроксида никеля также различное. Заряд γ-NiOOH протекает с меньшей эффективностью, а коэффициент использования по току ниже, чем у β-NiOOH. Разрядный потенциал γ-NiOOH ниже на 50 мВ. Но при хранении его саморазряд в 2 раза медленнее.
Для обеспечения большего ресурса следует вести заряд с небольшим перезарядом до образования β-NiOOH, который обеспечивает малые объемные изменения электрода в цикле заряда-разряда.
Отрицательный электрод. В новых герметичных никель-кадмиевых
аккумуляторах емкость кадмиевого электрода обычно выше емкости
оксидно-никелевого электрода на 20-70%. Поэтому потенциал кадмиевого электрода
в цикле заряда-разряда аккумулятора может считаться неизменным.
Электрические характеристики никель-кадмиевого аккумулятора
Номинальное напряжение герметичных Ni-Cd аккумуляторов - 1,2 В. Номинальный (стандартный) режим заряда никель-кадмиевого аккумулятора - током 0,1 С в течение 16 ч. Номинальный режим разряда никель-кадмиевого аккумулятора - током 0,2 С до напряжения 1 В.
Стандартный вид разрядных характеристик герметичных
цилиндрических никель-кадмиевых аккумуляторов при разных режимах показан на
рисунке 4.

Рис.4. Разрядные характеристика
никель-кадмиевого аккумулятора (Ni-Cd) при различных токах разряда.
Работоспособность аккумуляторов также отображается в
кривых зависимости разрядной емкости от температуры и токов нагрузки (рисунок 5
и 6). [8]

Рис.5. Разрядная характеристика
никель-кадмиевого аккумулятора (Ni-Cd)
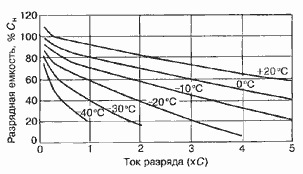
Рис.6. Разрядная характеристика
никель-кадмиевого аккумулятора (Ni-Cd)
Никель-водородные аккумуляторы
Отрицательным электродом служит пористый газодиффузионный электрод с платиновым катализатором, на котором обратимо реагирует газообразный водород. Характеризуются высокой удельной энергией и очень высоким ресурсом, но значительным саморазрядом и очень дороги. Применялись в космической технике. [11]
Литий-ионные (Li-ion) аккумуляторы

Рис 7. Li-ion аккумулятор 18650
Наиболее часто в мобильных устройствах (ноутбуки, мобильные телефоны, КПК и другие) применяют литий-ионные (Li-ion) аккумуляторы. Рис 7. Это связано с их преимуществами по сравнению с широко использовавшимися ранее никель-металлгидридными (Ni-MH) и никель-кадмиевыми (Ni-Cd) аккумуляторами.
У Li-ion аккумуляторов значительно лучшие параметры. Однако следует учитывать, что Ni-Cd аккумуляторы имеют одно важное достоинство: способность обеспечивать большие токи разряда. Это свойство не является критически важным при питании ноутбуков или сотовых телефонов (где доля Li-ion доходит до 80% и их доля становится все больше и больше), но существует достаточно много устройств, потребляющих большие токи, например всевозможные электроинструменты, электробритвы и т.п. До сих пор эти устройства являлись вотчиной почти исключительно Ni-Cd аккумуляторов. Однако в настоящее время, особенно в связи с ограничением применения кадмия в соответствии с директивой RoHS, резко активизировались исследования по созданию бескадмиевых аккумуляторов с большим разрядным током.
Первичные элементы ("батарейки") с литиевым анодом появились в начале 70-х годов 20 века и быстро нашли применение благодаря большой удельной энергии и другим достоинствам. Таким образом, было осуществлено давнее стремление создать химический источник тока с наиболее активным восстановителем - щелочным металлом, что позволило резко повысить как рабочее напряжение аккумулятора, так и его удельную энергию. Если разработка первичных элементов с литиевым анодом увенчалась сравнительно быстрым успехом и такие элементы прочно заняли свое место как источники питания портативной аппаратуры, то создание литиевых аккумуляторов натолкнулось на принципиальные трудности, преодоление которых потребовало более 20 лет.
После множества испытаний в течение 1980-х годов выяснилось, что проблема литиевых аккумуляторов закручена вокруг литиевых электродов. Точнее, вокруг активности лития: процессы, происходившие при эксплуатации, в конце концов, приводили к бурной реакция, получившей название "вентиляция с выбросом пламени". В 1991 г. на заводы-изготовители было отозвано большое количество литиевых аккумуляторных батарей, которые впервые использовали в качестве источника питания мобильных телефонов. Причина - при разговоре, когда потребляемый ток максимален, из аккумуляторной батареи происходил выброс пламени, обжигавший лицо пользователю мобильного телефона.
Из-за свойственной металлическому литию нестабильности, особенно в процессе заряда, исследования сдвинулись в область создания аккумулятора без применения Li, но с использованием его ионов. Хотя литий-ионные аккумуляторы обеспечивают незначительно меньшую энергетическую плотность, чем литиевые аккумуляторы, тем не менее Li-ion аккумуляторы безопасны при обеспечении правильных режимов заряда и разряда. [11]
Химические процессы Li-ion
аккумуляторов
Революцию в развитии перезаряжаемых литиевых аккумуляторов произвело сообщение о том, что в Японии разработаны аккумуляторы с отрицательным электродом из углеродных материалов. Углерод оказался весьма удобной матрицей для интеркаляции лития.
Для того чтобы напряжение аккумулятора было достаточно большим, японские исследователи использовали в качестве активного материала положительного электрода оксиды кобальта. Литерованный оксид кобальта имеет потенциал около 4 В относительно литиевого электрода, поэтому рабочее напряжение Li-ion аккумулятора имеет характерное значение 3 В и выше.
При разряде Li-ion аккумулятора происходят деинтеркаляция лития из углеродного материала (на отрицательном электроде) и интеркаляция лития в оксид (на положительном электроде). При заряде аккумулятора процессы идут в обратном направлении. Следовательно, во всей системе отсутствует металлический (нуль-валентный) литий, а процессы разряда и заряда сводятся к переносу ионов лития с одного электрода на другой. Поэтому такие аккумуляторы получили название "литий-ионных", или аккумуляторов типа кресла-качалки.
Процессы на отрицательном электроде Li-ion аккумулятора
Углеродная матрица, применяемая в качестве анода, может иметь упорядоченную слоистую структуру, как у природного или синтетического графита, неупорядоченную аморфную или частично упорядоченную (кокс, пиролизный или мезофазный углерод, сажа и др.). Ионы лития при внедрении раздвигают слои углеродной матрицы и располагаются между ними, образуя интеркалаты разнообразных структур. Удельный объем углеродных материалов в процессе интеркаляции-деинтеркаляции ионов лития меняется незначительно.
Кроме углеродных материалов в качестве матрицы отрицательного электрода изучаются структуры на основе олова, серебра и их сплавов, сульфиды олова, фосфориды кобальта, композиты углерода с наночастицами кремния.
Процессы на положительном электроде
Li-ion аккумулятора
Если в первичных литиевых элементах применяются разнообразные активные материалы для положительного электрода, то в литиевых аккумуляторах выбор материала положительного электрода ограничен. Положительные электроды литий-ионных аккумуляторов создаются исключительно из литированных оксидов кобальта или никеля и из литий-марганцевых шпинелей.
В настоящее время в качестве катодных материалов все чаще применяются материалы на основе смешанных оксидов или фосфатов. Показано, что с катодами из смешанных оксидов достигаются наилучшие характеристики аккумулятора. Осваиваются и технологии покрытий поверхности катодов тонкодисперсными оксидами.