Материал: Патан Серов учебник
несостоятельностью иммунитета у таких детей часто возникают инфекционные заболевания, которые имеют рецидивирующее течение и дают тяжелые осложнения (пневмония, менингит, сепсис), отмечается задержка физиологического развития. При комбинированных иммунодефицитных синдромах часто возникают пороки развития и злокачественные мезенхимальные опухоли (атаксия-телеангиэктазия Луи-Бар).
Синдромы недостаточности клеточного иммунитета в одних случаях наследуются обычно по аутосомно-доминантному типу (иммунодефицит с ахондроплазией, или синдром Мак-Кьюсика), в других являются врожденными (агенезия или гипоплазия вилочковои железы, или синдром Дайджорджа). Помимо агенезии или гипоплазии вилочковои железы и Т- зависимых зон периферической лимфоидной ткани, что определяет дефицит клеточного иммунитета, для этих синдромов характерны множественные пороки развития (см. табл. 4). Дети погибают от пороков развития либо от осложнений инфекционных заболеваний.
Синдромы недостаточности гуморального иммунитета имеют наследственную природу,
причем установлена сцепленность их с Х-хромосомой (см. табл. 4). Болеют дети первых пяти лет жизни. Для одних синдромов
Таблица 4. Первичные иммунодефицитные синдромы
Клинико-морфологические Название синдрома Тип наследования Иммунные наруш
проявления Комбинированные иммунодефицитные синдромы
Комбинированный тип Гланцманна и Риникера, или агаммаглобулинемия швейцарского типа
Атаксия-телеангиэказия Луи-Бар
Комбинированный тип с наличием В-лимфоцитов и иммуноглобулинов (синдром Незелофа)
|
Гипоплазия вилочковой железы и |
Тотальный дефект |
|
|
и гуморального им |
||
|
периферической лимфоидной |
||
|
|
||
Аутосомнорецессивныйткани, лимфопения, частые |
потеря способност |
||
|
инфекционные заболевания |
синтезировать |
|
|
иммуноглобулины |
||
|
|
||
|
Гипоплазия вилочковой железы и |
|
|
|
периферической лимфоидной |
|
|
|
ткани, лимфопения, атрофия |
Дефект клеточного |
|
То же |
коры мозжечка (атаксия), |
иммунитета, недос |
|
телеангиэктазия бульбарной |
иммуноглобулинов |
||
|
|||
|
конъюнктивы, мезенхимальные |
дефицит IgA |
|
|
злокачественные опухоли, |
|
|
|
рецидивирующая пневмония |
|
|
|
|
Содержание |
|
|
Гипоплазия вилочковой железы и |
иммуноглобулинов |
|
|
нормальное, возмо |
||
»» |
периферической лимфоидной |
||
дисгаммаглобулин |
|||
|
ткани, лимфопения, сепсис |
||
|
Дефект клеточного |
||
|
|
||
иммунитета
Синдромы недостаточности клеточного иммунитета |
|
|||
Агенезия или гипоплазия |
Не известен |
Отсутствие вилочковой железы и Содержание |
||
вилочковой железы |
околощитовидных желез |
иммуноглобулинов |
||
|
||||
|
|
|
206 |
|
(синдром Дайджорджа) |
|
(тетания), отсутствие Т- |
нормальное. Дефе |
|
|
|
лимфоцитов |
клеточного иммуни |
|
Окончание табл. 4 |
|
|
|
|
Название синдрома |
Тип |
Клинико-морфологические |
Иммунные |
|
наследования проявления |
нарушения |
|||
|
||||
Синдромы недостаточности гуморального иммунитета |
|
|||
Агаммаглобулинемия, |
|
Вилочковая железа сохранена. |
Дефект гуморального |
|
|
Отсутствие В-зависимых зон и |
иммунитета, потеря |
||
сцепленная с Х- |
Сцепленный с клеток плазмоцитарного ряда в |
|||
хромосомой (синдром |
Х-хромосомой лимфатических узлах и |
способности к |
||
синтезу |
||||
Брутона) |
|
селезенке, частные |
||
|
иммуноглобулинов |
|||
|
|
инфекционные заболевания |
||
|
|
|
||
|
|
Структура лимфоидной ткани |
|
|
|
|
сохранена. Проявления |
|
|
|
|
аллергии. Частые инфекции |
|
|
Избирательный |
|
дыхательных путей и |
Потеря способности к |
|
дефицит IgA (синдром |
То же |
желудочнокишечного тракта в |
||
синтезу IgA |
||||
Веста) |
|
сочетании с аутоиммунными |
||
|
|
|||
болезнями, синдром нарушенного всасывания, иногда с опухолями
(агаммаглобулинемия, сцепленная с Х-хромосомой, или синдром Брутона) характерна потеря способности к синтезу всех иммуноглобулинов, что морфологически подтверждается отсутствием В-зависимых зон и клеток плазмоцитарного ряда в периферической лимфоидной ткани, прежде всего в лимфатических узлах и селезенке. Другим синдромам свойствен дефицит одного из иммуноглобулинов (например, избирательный дефицит IgA, или синдром Веста), тогда структура лимфоидной ткани остается сохранной. Однако при всех синдромах недостаточности гуморального иммунитета развиваются тяжелые бактериальные инфекции с преобладанием гнойно-деструктивных процессов в бронхах и легких, желудочнокишечном тракте, коже, ЦНС, нередко заканчивающихся сепсисом.
Помимо иммунодефицитных, известны синдромы недостаточности системы моноритарных фагоцитов и нейтрофилов, среди которых наследственные заболевания и синдромы - хроническая гранулематозная болезнь, синдромы Чедиака-Хигаси и Джоба и др.
Вторичные иммунодефицитные синдромы
Вторичные (приобретенные) иммунодефицитные синдромы в отличие от первичных возникают в связи с болезнью или определенным видом лечения.
Среди заболеваний, ведущих к развитию недостаточности иммунной системы, основное значение имеет безудержно распространяющийся во многих странах мира синдром приобретенного иммунного дефицита,или СПИД, - самостоятельное заболевание, вызываемое определенным вирусом (см. Вирусные инфекции). К развитию вторичных иммунодефицитных синдромов ведут также другие инфекции, лейкозы, злокачественные
207
лимфомы (лимфогранулематоз, лимфосаркома, ретикулосаркома), тимома, саркоидоз. При этих заболеваниях возникает недостаточность гуморального и клеточного иммунитета в результате дефекта популяции как В-, так и Т-лимфоцитов, а возможно, и их предшественников.
Среди видов лечения, ведущих к вторичной недостаточности иммунной системы, наибольшее значение имеют лучевая терапия, применение кортикостероидов и иммунодепрессантов, антилимфоцитарной сыворотки, тимэктомия, дренирование грудного протока и др.
Недостаточность иммунной системы, развивающаяся в связи с лечением той или иной болезни, рассматривается как патология терапии (ятрогения).
При вторичных, как и при первичных, иммунодефицитных синдромах часто наблюдаются гнойные инфекции, обострение туберкулезного процесса, сепсис.
РЕГЕНЕРАЦИЯ
Общие сведения
Регенерация (от лат. regeneratio - возрождение) - восстановление (возмещение) структурных элементов ткани взамен погибших. В биологическом смысле регенерация представляет собой приспособительный процесс,выработанный в ходе эволюции и присущий всему живому. В жизнедеятельности организма каждое функциональное отправление требует затрат материального субстрата и его восстановления. Следовательно, при регенерации происходит самовоспроизведение живой материи, причем это самовоспроизведение живого отражает принцип ауторегуляции и автоматизации жизненных отправлений (Давыдовский И.В., 1969).
Регенераторное восстановление структуры может происходить на разных уровнях - молекулярном, субклеточном, клеточном, тканевом и органном, однако всегда речь идет о возмещении структуры, которая способна выполнять специализированную функцию.
Регенерация - это восстановление как структуры, так и функции. Значение регенераторного процесса - в материальном обеспечении гомеостаза.
Восстановление структуры и функции может осуществляться с помощью клеточных или внутриклеточных гиперпластических процессов. На этом основании различают клеточную и внутриклеточную формы регенерации (Саркисов Д.С., 1977). Для клеточной формы регенерации характерно размножение клеток митотическим и амитотическим путем,
для внутриклеточной формы, которая может быть органоидной и внутриорганоидной, - увеличение числа (гиперплазия) и размеров (гипертрофия) ультраструктур (ядра, ядрышек, митохондрий, рибосом, пластинчатого комплекса и т.д.) и их компонентов (см. рис. 5, 11, 15).Внутриклеточная форма регенерации является универсальной, так как она свойственна всем органам и тканям. Однако структурно-функциональная специализация органов и тканей в фило- и онтогенезе «отобрала» для одних преимущественно клеточнуую форму, для других - преимущественно или исключительно внутриклеточную, для третьих - в равной мере обе
208
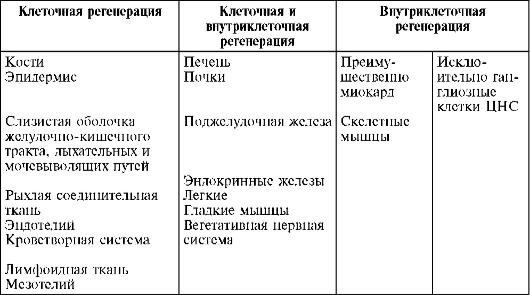
формы регенерации (табл. 5). Преобладание той или иной формы регенерации в определенных органах и тканях определяется их функциональным назначением, структурнофункциональной специализацией. Необходимость сохранения целостности покровов тела объясняет, например, преобладание клеточной формы регенерации эпителия как кожи, так и слизистых оболочек. Специализированная функция пирамидной клетки головного
мозга, как и мышечной клетки сердца, исключает возможность деления этих клеток и позволяет понять необходимость отбора в фило- и онтогенезе внутриклеточной регенерации как единственной формы восстановления данного субстрата.
Таблица 5. Формы регенерации в органах и тканях млекопитающих (по Саркисову Д.С., 1988)
Эти данные опровергают существовавшие до недавнего времени представления об утрате некоторыми органами и тканями млекопитающих способности к регенерации, о «плохо» и «хорошо» регенерирующих тканях человека, о том, что существует «закон обратной зависимости» между степенью дифференцировки тканей и способностью их к регенерации. В настоящее время установлено, что в ходе эволюции способность к регенерации в некоторых тканях и органах не исчезла, а приняла формы (клеточную или внутриклеточную), соответствующие их структурному и функциональному своеобразию (Саркисов Д.С., 1977). Таким образом, все ткани и органы обладают способностью к регенерации, различны лишь ее формы в зависимости от структурно-функциональной специализации ткани или органа.
Морфогенез регенераторного процесса складывается из двух фаз - пролиферации и дифференцировки. Особенно хорошо эти фазы выражены при клеточной форме регенерации. В фазу пролиферацииразмножаются молодые, недифференцированные клетки. Эти клетки называют камбиальными (от лат. cambium- обмен, смена), стволовыми
клетками и клетками-предшественниками.
Для каждой ткани характерны свои камбиальные клетки, которые отличаются степенью пролиферативной активности и специализации, однако одна стволовая клетка может быть родоначальником нескольких видов
209
клеток (например, стволовая клетка кроветворной системы, лимфоидной ткани, некоторые клеточные представители соединительной ткани).
В фазу дифференцировки молодые клетки созревают, происходит их структурнофункциональная специализация. Та же смена гиперплазии ультраструктур их дифференцировкой (созреванием) лежит в основе механизма внутриклеточной регенерации.
Регуляция регенераторного процесса. Среди регуляторных механизмов регенерации различают гуморальные, иммунологические, нервные, функциональные.
Гуморальные механизмы реализуются как в клетках поврежденных органов и тканей (внутритканевые и внутриклеточные регуляторы), так и за их пределами (гормоны, поэтины, медиаторы, факторы роста и др.). К гуморальным регуляторам относят кейлоны (от
греч. chalaino - ослаблять) - вещества, способные подавлять деление клеток и синтез ДНК; они обладают тканевой специфичностью. Иммунологические механизмырегуляции связаны с «регенерационной информацией», переносимой лимфоцитами. В связи с этим следует заметить, что механизмы иммунологического гомеостаза определяют и структурный гомеостаз. Нервные механизмы регенераторных процессов связаны прежде всего с трофической функцией нервной системы, афункциональные механизмы - с функциональным «запросом» органа, ткани, который рассматривается как стимул к регенерации.
Развитие регенераторного процесса во многом зависит от ряда общих и местных условий, или факторов. Кобщим следует отнести возраст, конституцию, характер питания, состояние обмена и кроветворения, кместным - состояние иннервации, крово- и лимфообращения ткани, пролиферативную активность ее клеток, характер патологического процесса.
Классификация. Различают три вида регенерации: физиологическую, репаративную и патологическую.
Физиологическая регенерация совершается в течение всей жизни и характеризуется постоянным обновлением клеток, волокнистых структур, основного вещества соединительной ткани. Нет таких структур, которые не подвергались бы физиологической регенерации. Там, где доминирует клеточная форма регенерации, имеет место обновление клеток. Так происходит постоянная смена покровного эпителия кожи и слизистых оболочек, секреторного эпителия экзокринных желез, клеток, выстилающих серозные и синовиальные оболочки, клеточных элементов соединительной ткани, эритроцитов, лейкоцитов и тромбоцитов крови и т.д. В тканях и органах, где клеточная форма регенерации утрачена, например в сердце, головном мозге, происходит обновление внутриклеточных структур. Наряду с обновлением клеток и субклеточных структур постоянно совершаетсябиохимическая регенерация, т.е. обновление молекулярного состава всех компонентов тела.
Репаративная или восстановительная регенерация наблюдается при различных патологических процессах, ведущих к повреждению клеток и тка-
210