Материал: Парциальное давление веществ в состоянии насыщения
Парциальное давление веществ в состоянии насыщения
Парциальное
давление веществ в состоянии насыщения
Уравнение, более точно, чем известные, описывающее зависимость упругости паров от температуры, выведено на основе использования параметров межмолекулярного взаимодействия в виде энергии системы, отклоненной от равновесия сил притяжения и отталкивания, и собственной энергии молекул.
Парогазовые потоки, являющиеся важнейшей составляющей большинства химических производств, образуются в результате перехода вещества из жидкого состояния в газообразное. При этом ключевым показателем, отражающим специфические особенности вещества и потому используемым для различных расчетов в физической химии и химической технологии, а также для характеристики органических соединений, является упругость пара j-того вещества [1-17].
Упругостью пара называют давление, при котором пар находится в состоянии равновесия с жидкой (или твердой [18]) фазой при данной температуре. Поэтому вместо упругости пара часто говорят о давлении пара в состоянии насыщения Pjн при температуре Т.
Экспериментально определяемые упругости пара лежат всегда в определенном интервале и всегда дискретны, из-за чего необходимо иметь уравнение, дающее непрерывное описание зависимости упругости пара от температуры во всем интервале Pjн - Т.
Теоретически в основу такого уравнения можно
положить выражение, полученное Клаузиусом и Клапейроном:
![]() . (1)
. (1)
Интегрируя (1) в предположении, что пар обладает свойствами идеального газа, а теплота испарения (DHj)V в исследуемом интервале не зависит от температуры, получаем
![]() , (2)
, (2)
где Т³Т0, так что при Т=Т0
![]() , а при
Т>Т0
, а при
Т>Т0 ![]() .
.
Практика, однако, показывает, что уравнение (2) дает ощутимые отклонения от эксперимента из-за невыполнения предположений об идеальности свойств насыщенного пара и независимости теплоты испарения от температуры.
Поэтому было предложено множество
уравнений для описания зависимости упругости пара от температуры, различающиеся
структурой, но требующих оценки параметров (коэффициентов) для каждого
вещества. К предложениям, уточняющим уравнение (2) путем введения эмпирических
коэффициентов, следует отнести предложения- Антуана
![]() , (3)
, (3)
пар давление уравнение
(в оригинале [19,20] для паров воды ![]() , где Q=230+t);
, где Q=230+t);
Гутмана и Симмоса [7]
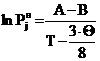 (4)
(4)
(метод расчета величины Q рассмотрен Дройсбахом [7]).
Абсолютное большинство других предложений сводится к описанию упругости пара полиномами различной степени от температуры [7].
Согласно [7] из всех уравнений, предложенных для расчета упругости пара по величине температуры, уравнение Антуана оказалось наиболее полезным. Тем не менее, в теоретическом и практическом анализе химико-технологических задач уравнение Антуана приходится уточнять введением дополнительных параметров или сужением области исследования по группам веществ и интервалам Pjн-Т [2,3,8].
Поэтому в настоящей работе сделана попытка установить зависимость упругости паров от температуры, исходя из иных соображений и, в частности, на основе параметров потенциалов межмолекулярного взаимодействия в виде энергии системы, отклоненной от равновесия сил межмолекулярного притяжения и отталкивания, и собственной энергии молекул.
Будем исходить из того, что переход вещества из твердого состояния в жидкое обусловлен нарушением равновесия межмолекулярных сил притяжения и отталкивания. При этом колебательное движение молекул заменяется поступательным прямолинейным, так что с ростом собственной энергии молекулы у нее появляется возможность “вырваться” из жидкой фазы в газовую.
Оценим энергию межмолекулярного взаимодействия в
состоянии, отклоненном от равенства разнонаправленных сил, отношением
потенциальной энергии (теплоты) неравновесной системы, состоящей из N
моль, к теплоемкости j-того
вещества:
![]() . (5)
. (5)
Измеряя Qj
в кДж, удельную теплоемкость CPj
в кДж/(кмольqград) и Nj
в кмоль, находим, что
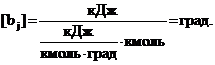
Отсюда следует, что bj оценивает энергию межмолекулярного взаимодействия числом градусов, на которое могла бы повыситься температура системы, если бы ее потенциальная энергия межмолекулярного взаимодействия перешла в кинетическую.
Таким образом, bj оценивает в градусах энергетический барьер, который должна преодолеть молекула, чтобы превысить силы межмолекулярного притяжения и “вырваться” из жидкой фазы в газообразную.
Теперь положим, что по величине
собственной энергии молекулы вещества распределены симметрично (например,
нормально) относительно некоторого среднего значения mj c дисперсией ![]() . Очевидно,
что с ростом температуры за счет вешнего или внутреннего источника теплоты1
растет собственная энергия молекул, так что
. Очевидно,
что с ростом температуры за счет вешнего или внутреннего источника теплоты1
растет собственная энергия молекул, так что
![]() , град., (6)
, град., (6)
где cj - безразмерный коэффициент; tu - температура в системе, град; u=(1,2,…,n).
Ясно, что с ростом температуры согласно (6)
средняя собственная энергия молекул mj
приближается к энергетическому барьеру bj,
увеличивая число молекул j-того
вещества, способных перейти из жидкой в газообразную фазу и, тем самым,
увеличить скорость прямого процесса2 (см. рис. 1).
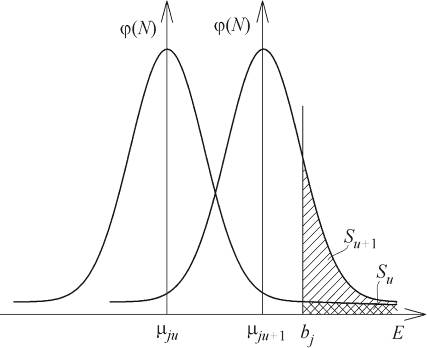
Рис. 1. К соотношению bj и mj при температурах tu и tu+1
Е - энергия; j (N)
- плотность распределения молекул по величине собственной энергии; - площадь
под кривой плотности - общее число N
молекул; - площадь заштрихованных участков - числа молекул, совершивших переход
из жидкой фазы в газовую (Su<<Su+1).
Скорость обратного процесса определяется достигнутым содержанием j-того вещества в газовой фазе, которое принято оценивать фактическим парциальным давлением Pj.
При постоянной температуре tu (u=1,2,…,n), достаточном количестве жидкости и достаточном времени контакта фаз Pj растет и, как следствие, растет скорость обратного процесса. Когда она становится равной скорости прямого процесса, наступает равновесие между жидким и газообразным состояниями j-того вещества, которому соответствует равновесное парциальное давление Pju*. Это давление называют парциальным давлением j-того вещества в состоянии насыщения или упругостью паров j-того вещества и обозначают Pjuн
С изменением температуры равновесие сдвигается:
-при увеличении температуры до tu+1 в сторону
газовой фазы, так что ![]() ;
;
при снижении температуры до tu-1 в сторону
жидкой фазы, так что ![]() .
.
В последнем случае часть парообразного j-того вещества переходит в жидкое состояние (конденсируется).
Таким образом, следует считать, что:
. Парциальное давление насыщенного пара, как предельно возможное при данной температуре содержание j-того вещества в газовой фазе, отражает степень неравновесности межмолекулярных сил притяжения и отталкивания в жидкости, которая сама зависит от размера, состава, строения и свойств молекул вещества.
. Соотношение сил межмолекулярного взаимодействия
и собственной энергии молекул определяет зависимость ![]()
![]() от температуры и независимость от
содержания в газовой фазе других веществ.
от температуры и независимость от
содержания в газовой фазе других веществ.
. При ограниченном времени контакта фаз, что характерно для промышленных потоков и эквивалентно недостатку жидкой фазы, равновесие между жидким и газообразным состояниями не достигается и пар оказывается ненасыщенным с парциальным давлением Pju.
. Связь между парциальными
давлениями насыщенного и ненасыщенного паров описывают выражением
![]() , (7)
, (7)
где jj - степень насыщенности пара j-того вещества.
Поскольку из (7) следует, что
![]() , (8)
, (8)
т.е. является отношением фактического содержания j-того вещества в газовой фазе к предельно возможному при данной температуре, jj можно назвать относительным выходом j-того вещества из жидкости в газовую фазу.
Из сформулированных выше положений, касающихся
механизма парообразования,
следует, что приращение равновесного парциального давления j-того
вещества в интервале температур от tu
до tu+1
пропорционально уже достигнутому давлению при tu:
![]() . (9)
. (9)
Из (9) для относительного приращения
равновесного давления получаем:
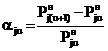 , (10)
, (10)
так что относительное приращение равновесного
давления во всем температурном диапазоне t1¸tn
составит
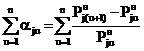 . (11)
. (11)
Чтобы установить температурную зависимость
равновесного парциального давления j-того
вещества, представим его относительное приращение aju
как отношение энергетического барьера bj,
создаваемого силами межмолекулярного взаимодействия в жидкости, к квадрату
отклонения1 от него средней собственной энергии молекул mj,
приходящегося на единицу температуры в интервале от tu
до tu+1:
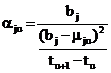
или, с учетом (6):
![]() . (12)
. (12)
Теперь, подставляя (12) в левую часть (11),
получаем выражение
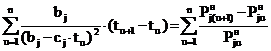 . (13)
. (13)
Сохраняя величину температурного диапазона (tn-t1)
и увеличивая n (полагая n®¥),
получаем, что
![]() , а
, а ![]() и
и ![]() .
.
С учетом этого перехода уравнение
(13) принимает вид:
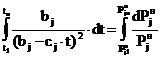 . (14)
. (14)
Принимаем, что u=bj-cjqt, так что du=-cjqdt.
С учетом этого интегрируем левую часть (14):
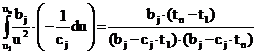 . (15)
. (15)
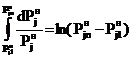 .
. ![]() (16)
(16)
Подставляя (15) и (16) в(14), находим
![]() . (17)
. (17)
Из (17) следует, что при условии tn=t1 получаем![]() , т.е.
упругость паров без увеличения температуры сохраняет уже достигнутый уровень,
что полностью соответствует исходному выражению (9). Поэтому, если взять t1=00C, то
уравнение (17) принимает вид:
, т.е.
упругость паров без увеличения температуры сохраняет уже достигнутый уровень,
что полностью соответствует исходному выражению (9). Поэтому, если взять t1=00C, то
уравнение (17) принимает вид:
![]() , (18)
, (18)
где Pj0н - упругость паров j-того вещества, достигнутая при подъеме температуры до 00С.
Из (18) видно, что температурная зависимость парциального давления насыщенного пара j-того вещества, полученная теоретически, является экспоненциальной функцией 3-х параметров, величины которых зависят от давления при температуре 00С, сил межмолекулярного взаимодействия в жидкости и собственной энергии молекул.
Для оценки этих параметров использовали экспериментальные данные по Pjuн и tu, взятые из [23]1 (табл. 1)2.
Значения Pj0н=aj, bj
и cj находили по алгоритму и программе, минимизирующим среднее
квадратическое отклонение рассчитанных по (18) величин ![]() при tu от
экспериментальных
при tu от
экспериментальных ![]() :
:
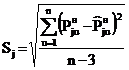 . (19)
. (19)
Область поиска задавали в виде:
![]() ; (20)
; (20)
![]() ; (21)
; (21)
![]() . (22)
. (22)
Приближенное значение aj0 берем из
экспериментальных данных, учитыая, что при t=0 по (18)
получаем ![]() .
.
Например, согласно табл.1 для бензола линейное приближение зависимости PБн=fБн(t) в интервале 2,6£t£7,6 дает aБ0=3,35 кПа.
Размер области начального поиска
определяли величиной ![]() . Для примера
с бензолом она составит 3,350±0,8375
кПа.
. Для примера
с бензолом она составит 3,350±0,8375
кПа.
Чтобы задать начальные значения bj0 и cj0, уравнение
(18) представим в виде
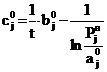 . (23)
. (23)
Запишем уравнение (23) для u-той
и (u+1)-той пар
значений (t, Pjн):
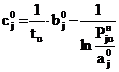 ; (24)
; (24)
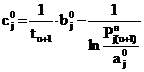 . (25)
. (25)
Вычитая (25) из(24), находим
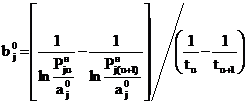 . (26)
. (26)
Подставляя (26) в (24), получаем
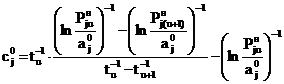 . (27)
. (27)
Те же значения сj0 получим, если (26) подставим в (25).
Алгоритм и программа поиска параметров уравнения(18), реализованные для веществ, представленных в табл.1, привели к значениям параметров aj, bj и cj, обеспечивающим минимальные значения остаточного среднего квадратического отклонения SB (табл. 2).
Для сравнения в этой же таблице приведены оценки SA, характеризующие точность результатов, найденных по уравнению Антуана с использованием значений его коэффициентов, найденных методом наименьших квадратов [21].
По значениям отношения SA/SB видно, что уравнение (18) для всех веществ, приведенных в табл. 1, превосходит по точности уравнение Антуана.
Для подтверждения того, что этот вывод имеет общий характер, дополнительно исследовали экспериментальные данные по упругости паров воды и аммиака (табл. 3) в области температур, расширяющей диапазон парциальных давлений до более 6 МПа.
Результаты расчетов по уравнению (18) и уравнению Антуана представлены в табл. 4.