Материал: Очистка конвертированного газа в производстве аммиака от диоксида углерода растворами горячего поташа
Таблица 4.1.2
Значения константы равновесия основной реакции при различных температурах
|
Температура, К |
K2CO3 + H2O + CO2=2 KHCO3 |
|
|
|
lgKp |
Kp |
|
300 |
6,073 |
9,3 1013 |
|
400 |
2,174 |
149,250 |
|
430 |
1,358 |
22,790 |
|
460 |
0,648 |
4,447 |
|
500 |
-0,166 |
0,683 |
|
600 |
-1,726 |
0,019 |
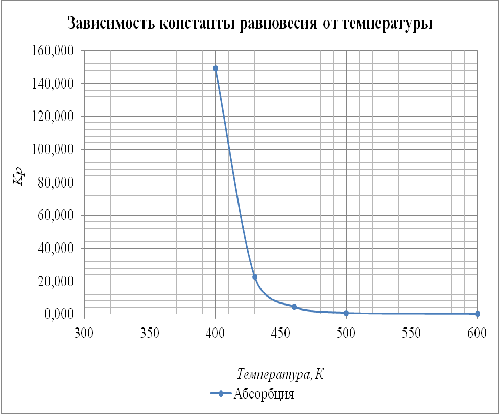
Рис. 4.1.2 ![]()
![]() График зависимости константы
равновесия от температуры
График зависимости константы
равновесия от температуры
Термодинамический анализ процесса очистки конвертированного газа от диоксида углерода раствором поташа позволил сделать следующие выводы:
1. В рассматриваемом интервале температур (300-600 К) термодинамическая вероятность самопроизвольного протекания процесса уменьшается, о чем свидетельствует значение энергии Гиббса.
. Согласно принципу Ле-Шателье увеличение давления способствует смещению равновесия в сторону продуктов реакции (Растворимость СО2 в горячем растворе поташа в значительной степени зависит от парциального давления двуокиси углерода над раствором)
. Увеличение концентрации раствора поташа
по сравнению со стехиометрическим ведет к смещению равновесия в сторону
продуктов реакции (предельная концентрация соли в горячем растворе 40%, т.к.
дальше наблюдается выпадение осадка); горячие растворы поташа вызывают
коррозионное разрушение углеродистой стали, поэтому в растворы добавляют
ингибиторы коррозии.
4.2 КИНЕТИЧЕСКИЙ
АНАЛИЗ
В качестве побочной реакции рассмотрим процесс, который применяют для выделения поглощенного газа (абсорбтива) из абсорбента и получения его в чистом виде, а также для повторного использования абсорбента в процессе абсорбции. Для проведения десорбции газа из жидкости необходимо, чтобы концентрация этого газа в газовой фазе была ниже концентрации, соответствующей равновесной в системе газ - жидкость. На практике для проведения процесса десорбции используют три следующих метода:
· отгонку в токе инертного газа или водяного пара;
· отгонку под действием подводимой к абсорбенту теплоты;
· отгонку при снижении давления над абсорбентом
Учитывая термодинамическую вероятность самопроизвольного протекания основной реакции, заключаем, что в интервале температур 300-600 К возможно протекание обратной реакции (десорбции газа), при подведением тепла к системе.
В общем случае метод хемосорбционной очистки обладает рядом особенностей оп сравнению с физической абсорбцией:
· Возможность абсорбции при низком парциальном давлении вследствие более высокой поглотительной абсорбции раствора;
· Относительно малая циркуляция раствора и соответственно небольшой расход энергии на перекачку сорбента;
· Регенерацию осуществляют, как правило, путем нагревания в сочетании со сбросом давления, при этом расход тепла на десорбцию относительно невелик;
· Регенерацию проводят часто при кипении абсорбента, его пары могут играть роль десорбирующего агента;
· Возможность проведения весьма тонкой очистки;
· Увеличение коррозии и протекание побочных реакций, обусловленных применением повышенных температур и щелочных агентом - сильных и слабых электролитов
Метод поташной очистки основан на применении относительно дешевого абсорбента, но имеет ряд недостатков: малая растворимость карбоната в воде (особенно бикарбоната) при обычной температуре, низкая скорость абсорбции, что приводит к необходимости значительной циркуляции раствора и обуславливает увеличение габаритов аппаратов. Кроме того, равновесное парциальное давление СО2 над растворами поташа относительно велико, и не удается достичь тонкой очистки газа (0,08 -0,15% СО2 в газе после очистки). Преимущество метода - сравнительно низкий расход тепла на регенерацию.
Скорость процесса абсорбции может быть
рассмотрена через применение основного уравнения массопередачи[4]. Если
выразить движущую силу процесса в концентрациях газовой фазы (парциальные
давления), то оно принимает следующий вид:
![]()
Где ![]()
![]() - средняя движущая сила процесса,
выраженная в единицах давления;
- средняя движущая сила процесса,
выраженная в единицах давления;
![]()
![]() - коэффициент массопередачи,
отнесенный к единице движущей силы, выраженной через парциальные давления
поглощаемого газа;
- коэффициент массопередачи,
отнесенный к единице движущей силы, выраженной через парциальные давления
поглощаемого газа;
Химическая реакция, сопровождающая
процесс абсорбции, оказывает существенное влияние на кинетику процесса, т.к.
скорость определяется не только интенсивностью массопереноса, но и скоростью
протекания химической реакции. Благодаря химической реакции растворенный CO2 переходит
в связанной состояние (KHCO3). Концентрация свободного
газа в жидкости уменьшается, а процесс абсорбции ускоряется (рост величины ![]()
![]() ), в сравнении с абсорбцией без
химического взаимодействия фаз[1]. Скорость хемосорбция зависит как от скорости
химической реакции, так и от скорости массопереноса между фазами. В зависимости
от лимитирующего процесса различаются кинетическую и диффузионную области
процесса хемосорбции.
), в сравнении с абсорбцией без
химического взаимодействия фаз[1]. Скорость хемосорбция зависит как от скорости
химической реакции, так и от скорости массопереноса между фазами. В зависимости
от лимитирующего процесса различаются кинетическую и диффузионную области
процесса хемосорбции.
Кинетическая область определяется как протекание процесса, при котором скорость химического взаимодействия меньше скорости массопереноса. В диффузионной области лимитирующая стадия - скорость диффузии компонента в зоне реакции, которая зависит от гидродинамических условий в системе и физических свойств.
Абсорбция, как и другие процессы, протекает на границе раздела фаз. Как следствие - абсорбционные аппараты (далее - абсорберы) должна иметь развитую поверхность контакта между жидкой и газовой фазами. Абсорберы по своим конструктивным особенностям делят на следующие основные группы: пленочные, насадочные, тарельчатые, распыливающие. На практике очистка конвертированного газа от CO2 проводится в насадочных колоннах. Варьирование площади поверхности раздела фаз происходит за счет смены насадки. Основные применяемые виды - кольца Рашига и седловидная насадка Берля.
Значения коэффициентов абсорбции CO2 растворами
карбонатов могут быть вычисленные по уравнениям[4]:
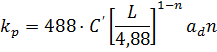
Где ![]()
![]() - объемный коэффициент абсорбции,
отнесенный к газовой пленке, кмоль/(м3·ч·атм)
- объемный коэффициент абсорбции,
отнесенный к газовой пленке, кмоль/(м3·ч·атм)
L - расход жидкости, кг/(м3·ч)
![]()
![]() - удельная поверхность несмоченной
насадки, м2/м3
- удельная поверхность несмоченной
насадки, м2/м3
C’, n -
константы, зависящие от типа насадки
![]()
Где ![]()
![]() - объемный коэффициент абсорбции,
отнесенный к газовой пленке, кмоль/(м3·ч·атм)
- объемный коэффициент абсорбции,
отнесенный к газовой пленке, кмоль/(м3·ч·атм)
![]()
![]() - удельная поверхность насадки,
м2/м3
- удельная поверхность насадки,
м2/м3
a - 0,288 +
0,00316u, (u - плотность
орошения), м3/(м2![]()
![]() ч)
ч)
b = 0,0059
![]()
![]() - вязкость раствора
- вязкость раствора
Таблица 4.2
|
Насадка |
|
n |
|
|
Кольца Рашига d=9,5 мм d=25 мм |
1,53 0,81 |
0,56 0,36 |
485 190 |
|
Седловидная (насадка Берля), l = 25 мм |
1,00 |
0,42 |
259 |
Выводы теоретического анализа:
. По условиям равновесия абсорбция происходит тем полнее, чем ниже температура. Однако, скорость абсорбции тем выше, чем выше температура. На основании сопоставления термодинамических и кинетических факторов выбираем оптимальную температуру абсорбции 35-100оС. Реакции, протекающие при очистке, являются экзотермическими и обратимыми, при повышении температуры раствора химическое соединение разлагается с выделением исходных компонентов, регенерация раствора протекает при 120-135оС.
. Согласно принципу Ле-Шателье увеличение давления способствует смещению равновесия в сторону продуктов реакции. На производстве применяется абсорбционный метод с давлением 2,5 - 2,8 мПа, с последующей тонкой очисткой растворами моноэтаноламина или едкого натра.
. При десорбции применяется дросселирование поглотительного раствора, при котором раствор вскипает и CO2 выдувается образующимся водяным паром.
. На основании справочных данных о влиянии степени карбонизации на температуру выпадения твердой фазы в водных растворах K2CO3, выбираем оптимальную концентрацию раствора 30 - 40%.
.
СИНТЕЗ И АНАЛИЗ ХТС
5.1 ХИМИЧЕСКАЯ
МОДЕЛЬ
Абсорбционная очистка газа - циклический процесс, на стадии абсорбции диоксид углерода поглощается растворителем, очищенный газ отправляется на последующую переработку, а насыщенный раствор регенерируют, что требует дополнительного расхода энергии. Процесс абсорбции проводим в массообменном аппарате типа насадочной колонны (насадка - кольца Рашига или седловидная насадка Берля).
Первоначально происходит физическая абсорбция CO2 раствором, после чего поглощенный диоксид углерода вступает в реакцию с карбонатом калия. Благодаря химической реакции растворенный CO2 переходит в связанной состояние (KHCO3). Концентрация свободного газа в жидкости уменьшается, а процесс абсорбции ускоряется. Особую важность представляет десорбция компонента и вторичное использование поташного раствора в целях экономии сырья. При десорбции применяется дросселирование поглотительного раствора, при котором раствор вскипает и CO2 выдувается образующимся водяным паром.
Очистка газа поташным раствором основана на взаимодействии диоксида углерода с карбонатом калия по суммарному уравнению
2CO3
+ H2O
+ CO2 = 2 KHCO3
Скорость реакции практически полностью
лимитируется скоростью медленно протекающей реакции в жидкой фазе
СO2 + ОН- = HCO3-
5.2 СТРУКТУРНАЯ СХЕМА

Схема 4.2.1 Структурная схема очистки
конвертированного газа от СО2 раствором горячего поташа
Метод основан на применении относительно дешевого абсорбента, но имеет ряд недостатков: малая растворимость карбоната в воде (особенно бикарбоната), низкая скорость абсорбции, что приводит к необходимости значительной циркуляции раствора и обуславливает увеличение габаритов аппаратов. Кроме того, равновесное парциальное давление СО2 над растворами поташа достаточно велико, и не удается достичь тонкой очистки газа (0,08 - 0,15% СО2 в газ после очистки). Преимущество метода - сравнительно низкий расход тепла на регенерацию.
5.3 ТЕХНОЛОГИЧЕСКАЯ СХЕМА
Проведен анализ различных технологических схем, представленных в литературе[1] [4] [5] [8] [9]. Выделены следующие виды схем: с разделенным потоком, схема поташной очистки с активатором, схема поташной очистки без активатора.
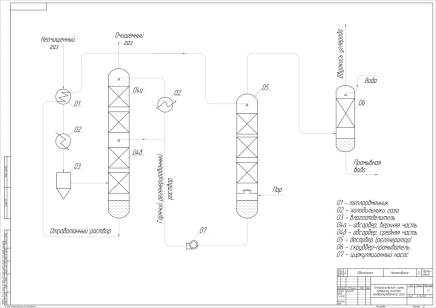
Описание технологической схемы
Газ под давлением 12,5 - 15 атм при температуре 155оС, которая развивается при сжатии его в компрессоре, поступает в теплообменник 1, куда подводится отработанный раствор после абсорбции. Часть тепла газ передает раствору, охлаждаясь при этом до температуры 125-130 оС, затем проходит водяной холодильник 2, где охлаждается до 122оС, и через влагоотделитель 3 поступает в абсорбер 4.
В абсорбере имеется несколько слоев насадки из колец Палля. Сюда подается регенерированный раствор поташа, 2/3 которого из регенератора 5 поступает в нижнюю часть абсорбера при температуре 102 °С. Примерно 1/3 раствора охлаждается в водяном холодильнике до 80 °С и затем подается в верхнюю часть абсорбера. Такая схема циркуляции раствора способствует снижению остаточного содержания СО2 в газе.
В абсорбере 4 газ очищается с 18 - 19% начальной концентрации СО2 до остаточного содержания 0,3 - 1,5% и при температуре 80 °С выходит из абсорбера. Далее очищенный газ охлаждается в водяных холодильниках и, пройдя влагоотделитель, поступает на сжатие в газовые компрессоры.
Отработанный поташный раствор удаляется из абсорбера через автоматический клапан регулятора уровня, проходит теплообменник 1 и дросселируется в верхнюю часть регенератора 5, где поддерживается избыточное давление порядка 0,06 - 0,07 атм. При этом из раствора выделяется двуокись углерода, концентрация которой достигает 99,5 - 99,8% СО2.
Регенератор представляет собой вертикальный колонный аппарат с двумя слоями насадки из колец Палля. Раствор стекает сверху вниз по насадке; при нагревании его парам из раствора выделяется двуокись углерода. К низу регенератора подключен выносной подогреватель, в котором раствор нагревается глухим паром до 104 - 105 °С.
Горячий регенерированный раствор перекачивается из регенератора насосом 8 на орошение абсорбера 4. Уровень раствора в регенераторе регулируется изменением подачи свежего конденсата в куб этого аппарата.
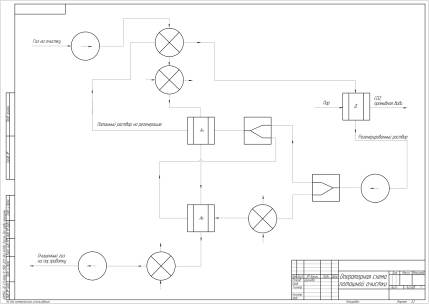
Операторная и технологическая схема поташной
очистки конвертированного газа от СО2 приведены в приложениях 1 и 2
соответсвенно.
.
ВЫБОР И ОСНОВАНИЕ КОНСТРУКЦИЯ ОСНОВНОГО АППАРАТА
Основными аппаратами на стадии очистки являются абсорберы[7] и регенераторы, в которых осуществляются массообменные процессы поглощения и выделения диоксида углерода.
К массообменной температуре очистки предъявляют следующие требования:
· Большая пропускная способность по газу и жидкости, что позволяет создать малогабаритные аппараты и делает возможным их транспортирование по железной дороге с завода изготовителя
· Высокая степень насыщения хемосорбента а абсорбере, что обеспечивает высокие технико-экономические показатели процесса
· Глубокая степень извлечения СО2 из газа, остаточное содержание не должно превышать 0,03 - 0,15% об.
· Минимальный расход тепла в регенераторе