Материал: Очистка конвертированного газа в производстве аммиака от диоксида углерода растворами горячего поташа
Недостатками метода очистки синтез-газа моноэтаноламином являются коррозионные свойства растворителя, высокий расход электроэнергии и пара для отгонки растворителя. Промывку синтез-газа горячим раствором карбоната калия выгодно применять при давлениях 14 ат.
Щелочная очистка газа от СО2
Очистка газов от СО2 водным раствором едкого натра NaOH основана на необратимой реакции:
+ СО2 = Na2СО3 + Н2О
Парциальное давление СО2 над раствором едкого
натра NaOH в процессе поглощения равно нулю до тех пор, пока вся щёлочь не
перейдёт в карбонат. Поглощение СО2 раствором карбоната натрия протекает с
образованием бикарбоната:
СО2 + Na2СО3 + Н2О = 2NaHСО3
Скорость абсорбции СО2 щёлочью возрастает с повышением температуры. Увеличение концентрации карбоната в растворе способствует снижению скорости абсорбции. В азотной промышленности очистка водным раствором едкого натра NaOH применяется в качестве последней ступени тонкой доочистки от СО2 конвертированного и коксового газа после водной очистки (когда концентрация СО2 в газе составляет не более 0,3% объёмных).
Процесс проходит в жидкой фазе при 90 - 95 °С и перемешивании. Установка регенерации щёлочи известью является громоздкой и процесс недостаточно удовлетворяет современным санитарно - гигиеническим требованиям (измельчение и гашение извести, транспортирование шлама в отвал и т. д.). Поэтому регенерацию отработанной щёлочи предусматривают только при значительном расходе щёлочи и необходимости привоза её со стороны. В остальных случаях водные растворы отработанной щёлочи стараются использовать для вспомогательных процессов нейтрализации и сбрасывают в специальные системы химически загрязнённых стоков.
Очистка газа от СО2 методом низкотемпературной абсорбции метанолом
В интервале температур от -30 до -60 °С и при давлении 1 - 3 МПа метанол является эффективным абсорбентом не только двуокиси углерода, но и сероводорода, органических соединений серы и некоторых других примесей, присутствующих в газовой смеси. Растворимость СО2 в метаноле значительно выше, чем в воде, и возрастает с понижением температуры и увеличением давления. Так, при -60 °С растворимость двуокиси углерода в метаноле в 75 раз превышает её растворимость в воде при 25 °С. Поэтому при промывке газа метанолом в условиях низких температур расход абсорбента на очистку единицы объёма газа значительно меньше, чем при водной очистке от СО2.
Благодаря этому соответственно уменьшаются энергетические расходы в процессе абсорбции. Потери водорода при низкотемпературной абсорбции также снижаются по сравнению с их потерями при водной промывке газа под давлением. Это связано не только с сокращением удельного расхода абсорбента, но и с уменьшением растворимости водорода в метаноле при понижении температуры. Процесс низкотемпературной абсорбции наиболее целесообразно проводить при 1 - 3 МПа. Нижний предел давления составляет 0,5 МПа. Этот метод эффективен в случае одновременного удаления из газовой смеси нескольких примесей при их достаточно высоком начальном содержании. Несмотря на необходимость применения холодильной машины, энергетические расходы в описанном процессе не превышают расхода энергии при промывке газа водой.
Сравнение различных методов очистки
При выборе процесса очистки окончательным критерием является величина приведенных затрат, зависящих в основном от энергетических и капитальных затрат.
Однако в каждом случае необходимо учитывать факторы, зависящие от конкретных условий и влияющие на экономику процесса. Эти факторы можно разбить на три группы:
· внешние технологические параметры процесса - состав, давление и температура очищаемого газа, требуемая степень очистки, параметры энергоресурсов (давление пара, наличие отбросного тепла, возможность использования вторичных энергоресурсов и т. д.);
· внутренние параметры процесса - расход тепла, электроэнергии, растворителя, отходы, тип и вес аппаратов;
· экономические факторы - цены на энергию, сырье, отходы, аппаратуру, а также дефицитность каких-либо видов сырья и энергии.
Кроме того, следует иметь в виду, что для крупнотоннажных агрегатов при сравнении методов очистки необходимо учитывать степень надежности процесса и оборудования.
Наиболее распространенный производственный вариант достаточно полной очистки - очистка горячим раствором поташа. Метод не требует больших затрат на энергию и сырье, протекание процесса позволяет повторно использовать некоторые ресурсы.
.
ОБОСНОВАНИЕ ОПТИМАЛЬНЫХ ПАРАМЕТРОВ ТЕХНОЛОГИЧЕСКОГО ПРОЦЕССА
Очистка конвертированного газа от CO2 - процесс, протекающий в несколько стадий. Во-первых, происходит физическая абсорбция газа (растворение), во-вторых - химическая реакция, результатом которой является связывание растворенного (абсорбированного) газа. Протекание абсорбционных процессов характеризуется их статикой и кинетикой:
Статика абсорбции, т. е. равновесие между жидкой и газовой фазами, определяет состояние, которое устанавливается при весьма продолжительном соприкосновении фаз. Равновесие между фазами определяется термодинамическими свойствами компонента и поглотителя и зависит от состава одной из фаз, температуры и давления.
Кинетика абсорбции, т. е. скорость процесса массообмена определяется движущей силой процесса (т. е. степенью отклонения системы от равновесного состояния), свойствами поглотителя, компонента и инертного газа, а также способом соприкосновения фаз (устройством абсорбционного аппарата и гидродинамическим режимом его работы). В абсорбционных аппаратах движущая сила, как правило, изменяется по их длине и зависит от характера взаимного движения фаз (противоток, прямоток, перекрестный ток и т. д.).
Различают физическую абсорбцию и хемосорбцию.
При физической абсорбции растворение газа не сопровождается химической реакцией (или, по крайней мере, эта реакция не оказывает заметного влияния на процесс). В данном случае над раствором существует более или менее значительное равновесное давление компонента и поглощение последнего происходит лишь до тех пор, пока его парциальное давление в газовой фазе выше равновесного давления над раствором. Полное извлечение компонента из газа при этом возможно только при противотоке и подаче в абсорбер чистого поглотителя, не содержащего компонента.
При хемосорбции (абсорбция,
сопровождаемая химической реакцией) абсорбируемый компонент связывается в
жидкой фазе в виде химического соединения. При необратимой реакции равновесное
давление компонента над раствором ничтожно мало и возможно полное его
поглощение. При обратимой реакции над раствором существует заметное давление
компонента, хотя и меньшее, чем при физической абсорбции. Уравнение реакции,
лежащей в основе хемосорбции рассматриваемого процесса при очистке
конвертированного газа:
K2CO3
+ H2O
+ CO2=2 KHCO3
Бикарбонат калия взаимодействует с растворенным
углекислым газом, связывая его, что влияет на изменение парциального давления
над раствором. С помощью термодинамического анализа определим термодинамические
условия протекания процесса, температуру, давление, концентрацию компонентов;
определим тепловой эффект реакции и температуру начала реакции. Так же найдем
условия протекания побочных реакций и условия максимального выхода целевого
продукта (в случае очистки подразумеваем максимальное связывание примесей в
ходе протекающей реакции).
4.1 ТЕРМОДИНАМИЧЕСКИЙ
АНАЛИЗ
Воспользуемся энтропийным методом для расчета
энергии Гиббса:
![]()
Термодинамические константы исходных веществ и продуктов реакции взяты из справочной литературы[3] и представлены в таблице 3.1.
Проводим расчет ![]()
![]() и
и ![]()
![]() по формулам:
по формулам:
![]()
![]()
![]()
![]()
![]() 89,48 кДж/моль
89,48 кДж/моль
![]()
![]() 89,48 кДж/моль
89,48 кДж/моль
Таблица 4.1.1
Термодинамические константы участников основной реакции
|
Термодинамическая величина |
Вещество |
|||
|
|
K2CO3 |
H2O |
CO2 |
KHCO3 |
|
|
|
|
|
|
|
|
|
|
|
|
Реакция идет с небольшим выделением тепла (экзотермична), для смещения равновесия к продуктам необходимо отводить тепло от системы. За счет последующего применения отведенного тепла к другим процессам можем снизить затраты на энергию (вторичный энергоресурс).
![]()
![]()
![]() Дж/моль·K
Дж/моль·K
Процесс трудно осуществить при
атмосферном давлении, так как энтропия отрицательна. Определим температуру
начала реакции, используя следующее условие:
![]()
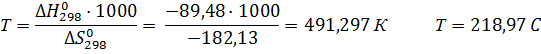
На основе температуры начала реакции
выберем температурный интервал расчета энергии Гиббса: 300![]()
![]() 600 К. С помощью энтропийного метода
проведем расчет
600 К. С помощью энтропийного метода
проведем расчет ![]()
![]() при различных температурах:
при различных температурах:
![]()
![]() =
= ![]()
![]() 89480
89480 ![]()
![]() 300· (
300· (![]()
![]() 182,13) =
182,13) = ![]()
![]() 34841 Дж/моль
34841 Дж/моль
![]()
![]() =
= ![]()
![]() 89480
89480 ![]()
![]() 400· (
400· (![]()
![]() 182,13) =
182,13) = ![]()
![]() 16628 Дж/моль
16628 Дж/моль
![]()
![]() =
= ![]()
![]() 89480
89480 ![]()
![]() 430· (
430· (![]()
![]() 182,13) =
182,13) = ![]()
![]() 11164 Дж/моль
11164 Дж/моль
![]()
![]() =
= ![]()
![]() 89480
89480 ![]()
![]() 460· (
460· (![]()
![]() 182,13) =
182,13) = ![]()
![]() 5700,2 Дж/моль
5700,2 Дж/моль
![]()
![]() =
= ![]()
![]() 89480
89480 ![]()
![]() 500· (
500· (![]()
![]() 182,13) = 1585 Дж/моль
182,13) = 1585 Дж/моль
![]()
![]() =
= ![]()
![]() 89480
89480 ![]()
![]() 600· (
600· (![]()
![]() 182,13) = 19798 Дж/моль
182,13) = 19798 Дж/моль
Отобразим полученные данные на
графике (рис. 4.1) в координатах ![]()
![]() . Сделаем вывод о влиянии
температуры на протекание реакции. Термодинамическая вероятность протекания
основной реакции с увеличением температуры уменьшается, необходимость отведения
тепла от системы подтверждается.
. Сделаем вывод о влиянии
температуры на протекание реакции. Термодинамическая вероятность протекания
основной реакции с увеличением температуры уменьшается, необходимость отведения
тепла от системы подтверждается.
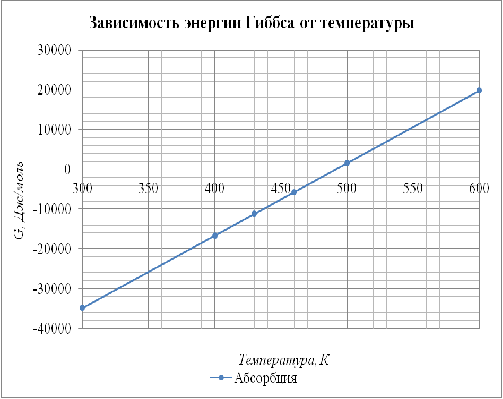
Рис. 4.1.1 ![]()
![]() График зависимости энергии Гиббса
от температуры
График зависимости энергии Гиббса
от температуры
аммиак двуокись углерод абсорбция
Зависимость константы равновесия от
температуры может быть представлена в виде уравнения:
![]()
![]()
![]()
![]()
![]()
![]()
Рассчитаем значения констант равновесия в указанном интервале температур, результаты представим в виде таблицы 4.2. Построим график зависимости константы равновесия от температуры протекания процесса.