Материал: Оценка токсичности наночастиц серебра in vitro
.3 Методы
изучения цитотоксичности наноматериалов в культурах клеток млекопитающих
2.3.1 Метилтетразолиевый тест
МТТ-тест предназначен для выявления метаболических нарушений, а именно нарушений функции митохондрий, отражающих влияние на жизнеспособность клеток. Клетки выращивали в СО2-инкубаторе (Herra Cell) при 37°С, 5% СО2, относительной влажности воздуха 80 % на 96-луночных планшетах (посевная концентрация - 50-70 тыс. кл./мл). В лунки с прикрепившимися клетками (вторые сутки культивирования) вносили исследуемые концентрации наносеребра, растворенного в сыворотке (Fetal Bovine Serum, Sigma, USA). После 24-часовой экспозиции исследуемых образцов фотометрически измерялась суммарная активность митохондриальных дегидрогеназ клеток в каждой лунке в метилтетразолиевом тесте (МТТ). Этот тест основан на способности живых метаболически активных клеток переводить соль тетразолина (MTS) в формазан, растворимый в среде культивирования. Таким образом, поглощение формазана прямо пропорционально количеству жизнеспособных клеток в культуре.
Для проведения МТТ использовали набор CellTiter 96® AQueous One Solution Cell Proliferation Assay (MTS), Promega. Для измерения поглощения формазана клетки инкубировали с МТS в течение 20 минут в термостате, измерение поглощения формазана при λ = 492 нм проводили на приборе для иммуноферментного анализа фирмы Awareness, Microplate Rider Stat Fax 3200.
.3.2 Метод оценки жизнеспособности клеток в культуре с помощью окраски трипановым синим (метиленовым синим)
Оценка целостности клеточной мембраны является одним из наиболее распространенных способов измерить жизнеспособность клетки и цитотоксические эффекты. Соединения, обладающие цитотоксичностью, часто вызывают нарушение целостности клеточной мембраны, что можно установить с помощью витального окрашивания трипановым синим (метиленовым синим), который свободно проникает через поврежденную мембрану и окрашивает внутриклеточные компоненты, но в здоровых клетках отсутствует.
Для оценки жизнеспособности более надежным способом является окрашивание клеточных суспензий, поскольку при окрашивании прикрепленных клеток они могут открепляться от субстрата и теряться. Главным недостатком этого метода является невозможность выявления клеток с нарушенной способностью к размножению [14].
Для проведения эксперимента с различными
концентрациями НЧ серебра (100, 300 мкг/мл) клетки линии А549 рассевали в
24-луночные планшеты. После окончания экспозиции (8 и 24 ч) клетки отмывали от
наночастиц физиологическим раствором, окрашивали 0,4% раствором красителя.
Количество мертвых окрашенных клеток подсчитывали в пяти произвольных полях
зрения.
.3.3 Метод оценки жизнеспособности клеток в культуре с помощью определения активности ЛДГ
Измерение активности лактатдегидрогеназы используется как один из основных тестов на цитотоксичность. Метод базируется на увеличении активности присутствующего в цитоплазме живых клеток фермента в среде культивирования, куда он выделяется через поврежденные мембраны мертвых или умирающих клеток. Небольшие количества культуральной среды берутся через определенные промежутки времени после воздействия на клетки для измерения высвобожденной лактатдегидрогеназы и определения зависимости токсического эффекта от временного фактора. В данном тесте можно оценить общую цитотоксичность в режиме реального времени.
Лактатдегидрогеназа - оксидоредуктаза, которая катализирует превращение пирувата и лактата. Клетки выделяют ЛДГ в кровяное русло после повреждения или гемолиза эритроцитов. Поскольку ЛДГ является стабильным ферментом, его широко используют для оценки наличия повреждения или токсичности для тканей и клеток. ЛДГ также повышается при определенных патологических условиях, таких как рак. В используемом наборе ЛДГ восстанавливает НАД+ в НАДН+, который специфически детектируется колориметрическим методом (450 нм).
Исходные растворы наночастиц готовили путем диспергирования в дистиллированной воде с добавлением альбумина при помощи четырехкратной ультразвуковой обработки общей продолжительностью 1 ч. Концентрация наносеребра - 100, 300, 600, 800, 1000 мкг/мл. Для проведения теста использовали набор MAK066 Lactate Dehydrogenase Activity Assay Kit, Promega. Содержание ЛДГ определяли в бесклеточной среде путем добавления субстрата (НАД+, соль тетразолина, натрия лактат и др.). В ходе определения происходят следующие реакции: первая реакция - ЛДГ восстанавливает НАД+ в НАДН путем окисления лактата до пирувата). Во второй реакции катализатор (диафораза) передает H/H+ от НАДН к соли тетразолина, образуя формазан. Для анализа использовали пробы сыворотки. Добавляли 2-50 мкл пробы в лунки 96-луночного планшета в двух повторностях. Пробы доводили до окончательного объема 50 мкл буфером для анализа ЛДГ. В каждую лунку вносили по 50 мкл основной реакционной смеси. Хорошо перемешивали пипетированием. Через 2-3 минуты определяли Tисходное. Измеряли оптическую плотность (A450) при длине волны λ=450 нм в начальный момент времени. Планшеты инкубировали при 37 °C, проводя измерения (A450) каждые 5 минут. Время предпоследнего измерения - Tконечное. Для измерения поглощения формазана пробы инкубировали в течение 5 минут в термостате, измерение поглощения формазана проведено на приборе для иммуноферментного анализа фирмы Awareness, Microplate Rider Stat Fax 3200.
Определение концентрации продукта реакции превращения 7-этоксирезоруфина в 7-гидроксирезоруфин осуществляли на основании калибровки, построенной по экспериментальным данным (рисунок 3).
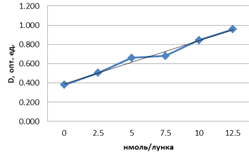
Рисунок 3 - Калибровочная прямая для определения
активности ЛДГ
Согласно калибровке относительная единица
оптической плотности соответствовала содержанию ЛДГ 0,430 нмоль/мин/мл (мЕ/мл).
2.4 Перечень
испытательного оборудования
Все работы с культурами клеток проводились в стерильном ламинарном боксе, культивирование клеток - в СО2-инкубаторе.
Перечень необходимого оборудования представлен в
таблице 1
Таблица 1 - Испытательное оборудование, средства
измерения
Наименование,
тип
Центрифуга
лабораторная ОПН-3,02
Микроскоп
Axioskop40
Термостат
ТС 80М-2 электрический суховоздушный
Сушильный
шкаф СНОЛ-67/350
Микроскоп
АУ-12
Весы
электронные Adventurer OHAUS
Инкубатор
СО2
3. Результаты
исследований
.1 Влияние
наночастиц серебра на жизнеспособность клеток линий А549, SHR и сублинии FL по
результатам МТТ-теста
Гибель клеток, индуцированную наночастицами,
оценивали по изменению оптической плотности раствора по отношению к контролю.
Результаты представлены на рисунках 4.
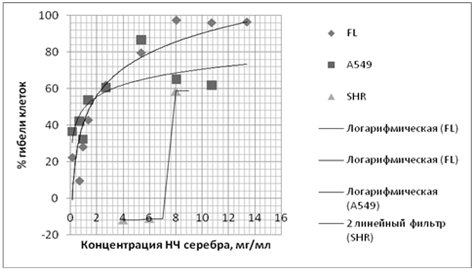
Рисунок 4 - Влияние НЧ серебра на клетки
различных линий
Как показали результаты МТТ-теста, средняя
ингибиторная концентрация (IC50) наночастиц серебра - концентрация, которая на
50 % подавляет способность клеток переводить соль тетразолина в формазан,
определенная графическим способом, для клеток линии А549 и сублинии FL
практически совпала и составила 1,3 и 1 мг/мл соответственно. В эксперименте на
кардиомиоцитах крысы IC50 наночастиц серебра определена на уровне 8 мг/мл.
Таким образом, данные, полученные в
эксперименте, свидетельствуют о более высокой чувствительности клеток линий
А549 и FL к действию наночастиц по сравнению с кардиомиоцитах крысы. Вероятно,
это связано с более высокой скоростью деления трансформированных клеток и
клеток амниона, а также интенсивностью метаболизма.
.2 Влияние
наночастиц на жизнеспособность лимфоцитов человека по результатам МТТ-теста
В эксперименте на лимфоцитах человека, которые
культивировали в течение 48 ч, продемонстрирована с наночастицами серебра (IC50
= 100 мкг/мл). Средняя ингибиторная концентрация определялась графически.
Результаты эксперимента представлены на рисунках 5.
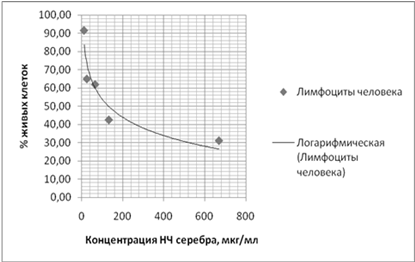
Рисунок 5 - Влияние НЧ серебра на лимфоциты
человека
Сопоставив результаты МТТ-теста на лимфоцитах
человека и предыдущего эксперимента, можно сделать вывод о том, что НЧ серебра
для лимфоцитов на порядок токсичнее, чем для любой использованной ранее
культуры клеток.
3.3 Изучение
цитотоксичности наноматериалов для клеток линии А549 с помощью окраски
метиленовым синим
Клетки линии А549 высевали в 24-луночные
планшеты, куда вносили НЧ серебра. Для оценки жизнеспособности клеток
использовали 0,4 % раствор метиленового синего. Окрашивание проводили через 8 и
24 ч после внесения наночастиц. Подсчет числа клеток проводили в 5 произвольных
полях зрения, рассчитывали среднее значение Результаты эксперимента
представлены в таблице 2.
Таблица 2 - Влияние НЧ серебра в различных
концентрациях на жизнеспособность клеток линии А549
Вариант
опыта
Число
клеток
8
ч
24
ч.
Общее
число клеток
Число
окрашенных клеток
%
гибель
Общее
число клеток
Число
окрашенных клеток
%
гибель
НЧ
серебра, 100 мкг/мл
67,2
4,6
6,8
88,4
5,6
6,3
НЧ
серебра, 300 мкг/мл
74
29
37,3
42,2
32,6
77,2
Показано, что при увеличении времени воздействия
эффект наночастиц серебра на клетки возрастает. Можно
сделать вывод о применимости метода окраски клеток в культуре метиленовым синим
для определения цитотоксического действия НЧ путем оценки целостности мембран
клеток.
.4 Изучение
жизнеспособности клеток в культуре по активности лактатдегидрогеназы в среде
культивирования
Изучена активность лактатдегидрогеназы (далее -
ЛДГ) в среде культивирования клеток А549 при добавлении НЧ серебра в
концентрациях от 100 до 1000 мкг/мл, экспозиция составила 24 ч (таблицы 3).
Таблица 3 - Результаты изучения влияния НЧ
серебра на активность ЛДГ в среде культивирования клеток линии А549
Концентрация
НЧ, мкг/мл
Активность
ЛДГ, мЕ/мл
100 300
302
600
366
800
414
1000
420
В результате активность ЛДГ при максимальных
концентрациях наноматериала возрастала в 1,5 раза.
Заключение
Наиболее перспективными объектами для изучения
являются наночастицы серебра т.к установлено, что наночастицы серебра являются
одним из наиболее перспективных типов наночастиц металлов. По меньшей мере, 235
видов товаров народного потребления, включая зубную пасту, перевязочные
материалы, средства для депиляции, содержат наносеребро. Вероятно, наночастицы
серебра найдут широкое применение в производстве текстиля, косметических
средств, антисептиков, полимеров, лакокрасочных материалов.. Их производство и
сфера применения увеличиваются, что может привести к негативному воздействию на
здоровье человека и окружающую среду.
В MTT тесте среднесмертельная концентрация
наночастиц серебра для клеток линии А549 и сублинии FL практически совпала и
составила 1,3 и 1 мг/мл соответственно, что на порядок выше, чем
среднесмертельная концентрация для лимфоцитов человека. В эксперименте на
кардиомиоцитах крысы LC50 наночастиц серебра определена на уровне 8 мкг/мл.
В эксперименте на клетках линии А549 оценивали
пригодность окраски трипановым синим для определения числа погибших (с
нарушенной проницаемостью мембраны) клеток. Число погибших клеток, определенное
по числу окрашенных клеток, оказалось несколько завышенным по сравнению с
результатами подсчета разницы между живыми клетками в контроле и в опыте после
смывания округлившихся и открепленных клеток. Можно сделать вывод о
применимости метода окраски клеток в культуре метиленовым синим для определения
цитотоксического действия НЧ путем оценки целостности мембран клеток.
При изучении влияния наноматериалов на
целостность мембраны клеток установлено, что активность ЛДГ при максимальных
концентрациях наноматериалов возрастала в 1,5 раза.
Список литературы
1 KemI (2008) Nanotechnology -
high risk with small particles? / KemI Report 6/07. - Swedish Chemicals Agency,
2008. - 74 p.
Toxic potential of materials at
the nanolevel / A. Nel [at al.] // Science. - 2006. - N 5761, Vol. 311. - P.
622 - 627.
Webster, T.J. Nanotechnology
for the regeneration of hard and soft tissues / T.J. Webster. - Singapore,
2007. - P. 207-214.
Air pollution, oxidative stress
and dietary supplementation: A review / I. Romieu [et al.] // European
respiratory journal. - 2008. - Vol. 31. - P. 179-197
Pulmonary applications and
toxicity of engineered nanoparticles / J. Card [et al.] // Aamerican journal of
physiology and lung cell molecular physiology. - 2008. - Vol. 295. - P.
400-411.
Long-term air pollution
exposure is associated with neuroinflammation, an altered innate immune
response, disruption of the blood-brain barrier, ultrafine particulate
deposition, and accumulation of amyloid β-42
and α-synuclein
in children and young adults / L. Calderón-Garcidueñas
[et al.] // Toxicologic pathology. - 2008. - Vol. 36. - P. 289-310.
Seaton, A. Nanotechnology and
the occupational physician / A. Seaton // Occupational medicine. - 2006. - Vol.
56, N 5. - P. 312-316.
The toxicity of diesel exhaust:
implications for primary care / I. Krivoshto [et al.] // Journal of the
American board of family medicine. - 2008. - Vol. 21, N1. - P. 55-62.
Assessing toxicity of fine and
nanoparticles: comparing in vitro measurements to in vivo pulmonary toxicity
profiles / C.M. Sayes [et al.] // Toxicological sciences. - 2007. - Vol. 97,
N1. - P. 163-180.
Dreher, K.L. Health and
environmental impact of nanotechnology: toxicological assessment of
manufactured nanoparticles / K.L. Dreher // Toxicological sciences. - 2004. -
Vol. 77. - P. 3-5.
Meng, H. A predictive
toxicological paradigm for the safety assessment of nanomaterials / H. Meng et
al. // ACS. - 2009. - Vol. 3, N 7. - P. 1620-1627.
Riss, T.L., Moravec, R.A. Use
of multiple assay endpoints to investigate the effects of incubation time, dose
of toxin, and plating density in cell-based cytotoxicity assays / T.L. Riss,
R.A. Moravec // Assay Drug Dev. Technol.
Decker, T., Lohmann-Matthes, M.L.
A quick and simple method for the quantitation of lactate dehydrogenase release
in measurements of cellular cytotoxicity and tumor necrosis factor (TNF)
activity / T. Decker, M.L. Lohmann-Matthes // J. Immunol. Methods.
- Vol. 115, N 1. - P. 61-69.
Культура животных клеток. Методы:
пер. с англ. / под ред. Р. Фрешни. - М.: Мир, 1989. - 333 с.
Комплексная биологическая оценка
объектов природного и искусственного происхождения на Tetrahymena pyriformis:
метод. рекомендации / разраб.: Белорус. науч.-иссл. сан.-гиг. ин-т; авт.-сост.
А.С.
Богдан.
- Минск,
1996. - 19 с.
Maron, D.M. Revised Methods for
the Salmonella Mutagenicity Test / D.M. Maron, B.N. Ames // Mutat. Res. - 1983.
- Vol. 113, N 3-4. - P. 173-215.
OECD Guideline 471, Bacterial
Reverse Mutation Test, updated and adopted July 21, 1997.
18 Фонштейн, Л.М. Методы первичного
выявления генетической активности загрязнителей среды с помощью бактериальных
тест-систем: Методические указания / Л.М. Фонштейн [и др.]. - М., 1985. - 34 с.
Гузев, B.C., Левин, C.B. Техногенные
изменения сообщества почвенных микроорганизмов / B.C. Гузев, C.B. Левин // Тез.
докл. конф. "Перспективы развития почвенной биологии". - Москва,
2001. - С. 178-219.
Наплекова, H.H. Микробная индикация
состояния почв / Н.Н. Наплекова // Тез. докл. конф. "Оценка современного
состояния микробиологических исследований в Восточно-Сибирском регионе". -
Иркутск, 2002.