Материал: Оценка токсичности наночастиц серебра in vitro
Абсорбция и распределение в нервной системе. Транслокация твердых частиц в дыхательных путях может происходить посредством аксонов нейронов. В назальной и трахеобронхиальной части дыхательных путей находятся чувствительные окончания обонятельного и тройничного нервов. Обонятельный нерв может являться путем поступления наночастиц в ЦНС человека. Имеются также дополнительные пути - через тройничный нерв, окончания чувствительных нервов, находящиеся в трахее и бронхах, как показано в экспериментах при интраназальной инстилляции наночастиц.
Воздействие через желудочно-кишечный тракт и кожу. Наночастицы, которые удаляются из дыхательной системы мукоцилиарным эпителием, могут попадать в ЖКТ. Наночастицы могут также поступать в ЖКТ с системами доставки лекарств. Многочисленные исследования показали, что наночастицы при попадании в ЖКТ быстро выводятся из организма. Другой потенциально важный путь поступления - через кожу. Установлено, что наночастицы, поступившие в дерму, локализуются впоследствии с помощью макрофагов кожи и дендритических клеток в регионарных лимфоузлах. Это поднимает вопрос о потенциальном изменении иммунного ответа на наночастицы после взаимодействия макрофагов и дендритических клеток, содержащих наночастицы, с Т-лимфоцитами.
Легочная канцерогенность. Малотоксичные, плохо
растворимые частицы, такие как углерод, диоксид титана индуцируют хроническое
воспаление, фиброз, неопластические изменения и рак легких у крыс. Опухоли
легких, связанные с воздействием таких частиц, происходят из альвеоцитов 2-го
типа (бронхоальвеолярные опухоли), либо из участков сквамозной метаплазии
(эпидермоидные опухоли). Продолжительное присутствие высоких уровней
нетоксичных частиц приводит к ухудшению их выведения альвеолярными макрофагами,
затем вызывает их быстрое накопление, хроническое воспаление, фиброз, опухолеобразование.
Воспалительный процесс является основной причиной возникновения опухолей
легких, так как наночастицы реализуют мутагенный потенциал и действуют на
пролиферативную активность[11].
.6 Системные эффекты наночастиц
Независимо от пути поступления после попадания в кровеносную систему наночастицы с кровью разносятся по всему организму и могут вмешиваться в процессы передачи сигналов. Наночастицы диаметром > 40 нм по размеру сопоставимы с большими протеинами, могут формировать с ними различные комплексы в зависимости от свойств поверхности. Комплексы могут иметь другую биокинетику, активность и даже функцию. Если частица не распадается и ее размер свыше 5 нм, наночастица не может быть выведена через почки и, таким образом, может вызвать более выраженные повреждающие эффекты в организме. Высвобождение медиаторов воспаления вследствие накопления наночастиц в легких может стать причиной гиперкоагуляции крови и увеличить кардиоваскулярный риск. Развитие атеросклероза также связывают с воздействием наночастиц. Наночастицы способны преодолевать гематоэнцефалический барьер и проникать в ЦНС.
Основной путь воздействия UFPs ингаляционный. Считается, что размер UFPs позволяет им долгое время оставаться в воздухе, попадать в нижние отделы дыхательных путей, проникать в межклеточное пространство, что препятствует выведению из организма. UFPs, даже если по химическому составу не являются токсичными, могут вызвать окислительный стресс [12], высвобождение медиаторов воспаления и способствовать возникновению заболеваний легких и других системных эффектов [13, 14].
Воздействие на человека может быть
профессиональным, непосредственно в процессе производства, либо опосредованно
через контаминацию воздуха рабочей зоны или офисного помещения [15], а также
случайным, в результате загрязнения атмосферного воздуха, эмиссии побочных
продуктов [16]
.7 Иисследование цитотоксичности наночастиц
Реализация токсичности наноматериалов обеспечивается следующими свойствами: физическое сродство к биологическим структурам, например посредством электростатического или гидрофобного взаимодействия; каталитическиие свойства, с активацией окислительно-восстановительных реакций, например индукция молекул кислорода и воды с образованием АФК; распад наночастиц с образованием токсичных соединений
К основным проблемам токсичности наноматериалов можно отнести следующие. Во-первых токсичность наночастиц не может быть производной токсичности аналогов в макродисперсной фазе или в форме сплошной фазы, а во-вторых, имеющиеся токсикологические методологии основаны на определении токсичности вещества относительно массовой концентрации, что не приемлемо для наноматериалов, для которых определяющим свойством может быть площадь поверхности или число наночастиц.
Недавние инновации в науке и технике позволили разработать ряд тестов in vitro, позволяющих прогнозировать токсичность для животных. Поскольку требования для тестирования нанматериалов еще законодательно не установлены, ученые имеют возможность осуществлять поиск методов, основанных на новейших достижениях науки и применять их на практике.
Многие модели in vitro превосходят методы изучения токсичности, основанные на использовании животных, которые традиционно применялись в области токсикологии. Модели с использованием животных не только негуманны, но и часто недостаточно надежны с точки зрения прогнозирования эффектов у человека. Область нанотоксикологии обязана включить доступную технологию. Далее представлены наиболее многообещающие методы in vitro, доступные в настоящее время для проведения оценки безопасности наноматериалов.
Для изучения действия наноматериалов на типы клеток, соответствующие "входным воротам", применяется ряд методов, позволяющих определить цитотоксичность, способность наноматериалов вызывать воспаление, окислительный стресс, а также генотоксичность.
Токсические эффекты НЧ связывают, в первую очередь, с формированием окислительного стресса и накоплением свободнорадикальных продуктов [17].
Методы in vitro на культурах клеток позволяют изучить: окислительный стресс и АОЗ, воспаление, жизнеспособность клеток, пролиферацию, апоптоз, некроз, нарушение функции митохондрий, влияние на мембраны, клеточную локализацию наночастиц.
Тесты на цитотоксичность традиционно используют в фармацевтической промышленности для скрининга биологически активных соединений. В настоящее время их широко применяют для оценки наноматериалов. Существует множество способов оценки цитотоксического действия. Один из них - определение числа живых и погибших клеток.
Оценка целостности клеточной мембраны является одним из наиболее распространенных способов измерить жизнеспособность клетки и цитотоксические эффекты. Соединения, обладающие цитотоксичностью, часто вызывают нарушение целостности клеточной мембраны, что можно установить с помощью витального окрашивания трипановым синим или йодидом пропидия, которые свободно проникают через поврежденную мембрану и окрашивают внутриклеточные компоненты, но в здоровых клетках отсутствуют [18]. Целостность мембран может быть оценена другим способом - путем определения лактатдегидрогеназы, имеющей в норме внутриклеточную локализацию, во внешней среде [19]. Цитотоксичность может также быть определена с использованием MTT теста, основанного на способности митохондриальных дегидрогеназ конвертировать водорастворимый 3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-2Н-тетразолиум бромид (МТТ) в формазан. Подобный тест, основанный на окислительно-восстановительном потенциале, был разработан с применением флуоресцентного красителя - диазорезорцина. В дополнение разработан тест in vitro с АТФ в качестве маркера жизнеспособности [20].
Доказана неодинаковая чувствительность к наночастицам различных линий клеток, что обязательно следует учитывать при оценке цитотоксичности наночастиц.
Таким образом, иисследование цитотоксичности может включать:
.Определение повреждения мембран;
подсчет с помощью световой микроскопии поврежденных и погибших клеток, окрашенных красителем (например, трипановым синим), пассивно поступающим внутрь;
спектрофотометрическое определение живых клеток, активно захватывающих краситель (например, нейтральный красный);
лизис клеток с высвобождением внутриклеточных ферментов (например, ЛДГ) в культуральную среду, спектрофотометрическое определение (доступны диагностические наборы).
.Изучение внутриклеточных метаболических изменений;
определение активности ферментов I и II фазы биотрансформации с помощью спектрометрии, масс-спектрометрии, газовой хроматографии, высокоэффективной жидкостной хроматографии и др.;
определение в МТТ-тесте нарушения функции митохондрий;
определение содержания АТФ в клетках.
. Изучение процессов апоптоза, вызывающего ряд биохимических и морфологических изменений, определяемых количественно;
каспазной активности (в частности, каспазы-3);
экспрессии Apaf-1, Bcl-2 протеинов Bax и Bid, p53.
Изучение воспалительных эффектов наноматериалов на различных культурах клеток человека in vitro необходимо для оценки потенциальной токсичности наночастиц. Цитокины, хемокины наряду с другими маркерами воспаления часто позволяют получить представление о механизме действия и токсичности наноматериалов. Использование соответствующих типов клеток человека имеет критическое значение.
Показано, что наночастицы способны проникать в клетки, минуя любые барьеры. Они способны к трансцитозу через эпителиальные и эндотелиальные клетки, распространяются по ходу дендритов и аксонов нервов, циркулируют в кровеносных и лимфатических сосудах, имеют тропность к определенным тканям. Опасение по поводу поступления наноччастиц в клетки, связанное с влиянием на здоровье человека и окружающую среду, побудило исследовтелей оценивать способность наноматериалов проникать через клеточные мембраны во внутриклеточные компартменты и ядро. Чтобы оценить риск, важно определить способ воздействия и решить, способны ли данные наночастицы проникать через мембраны клеток. Перемещение можно регистрировать с помощью конфокальной флюоресцентной микроскопии, трансмиссионной электронной микроскопии.
Из-за уникальных свойств и активности, наноматериалы могут пересекать клеточные мембраны, встраиваться в ДНК, повреждать белки. Как только "входные ворота" для наноматериалов определены, культуры клеток соответствующих тканей можно изучать в отношении повреждения протеинов и ДНК. Следует отдавать предпочтение культурам клеток человека.
Среди методов in vitro, применимых для изучения генотоксичности/мутагенности наноматериалов: тест Эймса, тест на хромосомные аберрации, тест на внеплановый синтез ДНК, тест на сестринский хроматидный обмен.
Каждый из тестов может быть частичной или полной заменой для методов in vivo. Отрицательные результаты теста не требуют проведения дополнительных исследований in vivo. Кроме того, генотоксичность можно оценивать, используя другие доступные, надежные методы, например, Cоmet тест.
Таким образом, достижения в области высоких технологий, аналитических методов позволяют проводить адекватное тестирование токсичности без использования животных. Электронная микроскопия и клеточные культуры, диагностические наборы предоставляют исследователям возможность оценивать клетки/органеллы/ДНК в ходе токсикологических исследований и регистрировать химические изменения в этих структурах, вызванные наноматериалами.
С точки зрения безопасности для здоровья
человека и окружающей среды необходимо, чтобы нанотоксикология строилась на
фундаменте надежных, адекватных тестов in vitro, позволяющих прогнозировать
эффект наноматериалов.
2. Обьекты,
методы исследований, приборы, оборудование
2.1 Наночастицы,
используемые в экспериментах in vitro
.1.1 Характеристика наночастиц серебра
Для проведения исследований использованы
наночастицы серебра производства фирмы Aldrich, содержание наночастиц серебра
99,5% (следовые количества металлов), размер частиц <100 нм. Частицы имеют
органическое покрытие для дисперсии в полярном растворителе.
2.2 Культуры
клеток, используемые для изучения токсичности in vitro
2.2.1 Культура клеток карциномы легкого человека (А549)
Клетки культивируют в среде ДМЕМ с добавлением
10%-ой инактивированной телячьей эмбриональной сыворотки (FBS), 45 ЕД/мл
пенициллина и 45 мг/мл стрептомицина в 5%-ой CO2
среде
при 37 °C в CO2-инкубаторе
(рисунок 2).
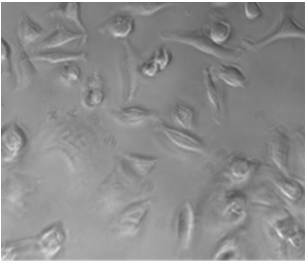
Рисунок 4 - Культура клеток А549
2.2.2 Культура клеток амниона человека, сублиния FL
Морфология: эпителиоподобная. Способ
культивирования: монослойный. Условия культивирования: среда - 199 или ЕМЕМ,
сыворотка - КРС 10% (199); эмбриональная бычья10% (ЕМЕМ). Процедура пересева -
cнятие клеток, используя версен 0,02% c химопсином 0,1 мг/мл, кратность рассева
1:4 - 1:10, оптимальная плотность 0,5-1,0х105 клеток/мл. Кариология: 2n=46,
пределы изменчивости по числу хромосом 47-66, модальное число хромосом 60,
количество маркеров 9, из которых 3 - специфичны для клеток НеLa (N 1,2,3, G
диски). Изоэнзимы Г6ФДГ, А.16. Чувствительность к интерферону человека. Область
применения: вирусология, канцерогенез, клеточная биология.
.2.3 Культура лимфоцитов человека
Культура лимфоцитов человека является одной из обязательных тест-систем при оценке влияния мутагенных факторов окружающей среды. Одним из достоинств этой тест-системы является то, что по наблюдаемым типам аберраций можно достаточно определенно идентифицировать тип мутагенного воздействия.
Культивирование лимфоцитов. Кровь отбирают из локтевой вены, помещают в стерильную пробирку, содержащую раствор гепарина (200 ЕД/мл крови). В стерильных условиях образцы крови переливают по 0,8 мл в приготовленные для культивирования флаконы Карреля с культуральной средой. Состав культуральной среды: 6,16 мл среды МЕМ; 1,6 мл инактивированной телячьей сыворотки; 0,08 мл L-глютамина; 0,08 мл р-ра антибиотика; 0,15 мл фитогемагглютинина. Флаконы помещают в термостат при 37°С для инкубации клеток в течение 48 ч. Для блокирования митоза на стадии метафазы за 2 ч до окончания инкубации во флаконы добавляют раствор демеколцина в концентрации 0,2 мкг/мл среды.
Гипотонизация клеток. После окончания культивирования культуру клеток переливают в центрифужные пробирки и центрифугируют при 10007 об./мин в течение 15 мин для осаждения клеток. Надосадочную жидкость удаляют с помощью водоструйного насоса, добавляют предварительно подогретый до 37°С гипотонический раствор (0,75 М KCl) и ресуспендируют в нем осадок. Далее пробирки с культурой клеток выдерживают на водяной бане (37°С) 10-12 мин. По окончании гипотонизации вновь центрифугируют при тех же условиях с последующим удалением надосадочной жидкости.
Фиксация клеток. Для фиксации клеток осадок
ресуспендируют в 1-1,5 мл свежеприготовленного фиксатора (смесь метилового
спирта и ледяной уксусной кислоты в пропорции 3:1) на шейкере и доводят его
объем до 10 мл. Смену фиксатора с последующим центрифугированием производят
трижды.
.2.4 Культура кардиомиоцитов крыс линии SHR
Исходный материал для первичной культуры
кардиомиоцитов крыс получают путем дезагрегации 0,25%-ным раствором трипсина
при 37ºС
в течение 30 мин сердечной ткани 12-14-суточных эмбрионов крысы. После удаления
трипсина осадок суспендируют в ростовой среде (90% среды Игла, 10%
эмбриональной сыворотки телят с добавлением антибиотиков). Суспензию пропускают
через капроновый фильтр (ячейка 0,3 х 0,3 мм). После подсчета в камере Горяева
клетки высевают в 96-луночные планшеты и культивируют в ростовой среде DMEM.