Материал: Обзор методов определения содержания витаминов А и Е в продуктах питания
Антиоксидантная активность витамина Е.
Витамин Е (токоферола ацетат, Tocopheroli acetas). Токоферола ацетат является синтетическим препаратом витамина Е. Наибольшей биологической активностью обладает а-токоферол. Под названием «витамин Е» известны и другие токоферолы, они близки по химической природе и биологическому действию. Витамин Е обладает выраженным антиоксидантным свойством. Он захватывает неспаренные электроны активных форм кислорода, блокирует перекисное окисление липидов (а именно тормозит перекисное окисление ненасыщенных жирных кислот), стабилизируя состояние клеточных мембран. Это свойство - предотвращение окисления ненасыщенных жирных кислот - используется в косметических средствах, дает возможность избежать прогоркания жиров.
Кроме того, витамин Е участвует в биосинтезе гемоглобина крови и белков, в делении клеток, в тканевом дыхании и других сложных и важных процессах. Витамин Е восстанавливает витамин А и кофермент Q10 (убихинон). Кроме того, действие витамина Е связано с действием микроэлементов (в частности, селена, который входит в состав фосфолипидглутатионпероксидазы и глутатионпероксидазы, активность которых зависит от витамина С) [20].
Токоферолы в природе содержатся в зеленых частях растений, особенно в молодых ростках злаков, некоторое количество их содержится в жире, мясе животных, яйцах, молоке, креветках, кальмарах и др.
В медицине и косметологии используют экстракты из злаков, пророщенных зерен, растительные масла, полученные холодным отжимом. Богаты токоферолом следующие растительные масла:
· соевое (1140 мг/кг);
· хлопковое (990 мг/кг);
· кукурузное (930 мг/кг);
· оливковое (130 мг/кг)
и другие (арахисовое, облепиховое, пальмовое, миндальное, масло лесного ореха).
.4
Неферментативная антиоксидантная система
В качестве компонентов неферментативной АОС могут выступать низкомолекулярные вещества, имеющие высокую константу скорости взаимодействия с АФК.
Неферментативная АОС включает различные по химическому строению и свойствам соединения: водорастворимые - глутатион, аскорбат, цистеин, эрготионеин, и гидрофобные - - токоферол, витамин А, каротиноиды, убихиноны, витамины группы К, которые снижают скорость образования свободных радикалов и уменьшают концентрацию продуктов реакций, протекающих с участием радикалов [21].
Основная направленность действия низкомолекулярных АО связана с защитой белков, нуклеиновых кислот, полисахаридов, а также биомембран от окислительного разрушения при свободнорадикальной процессах. Важное значение низкомолекулярные АО приобретают в условиях окислительного стресса, когда ферментативная АОС оказывается менее эффективной в сравнении с их протекторным действием. Причины этого - быстрая инактивация конститутивного пула ферментов свободными радикалами и значительное время, необходимое для индукции их синтеза [22].
В липидах содержатся природные антиоксиданты (АО), существенно влияющие на скорость реакции обрыва цепей окисления. К гидрофобным АО фенольного типа относятся три группы веществ: токоферолы, убихиноны и витамины группы К. Каждое из этих веществ образует группу структурно-родственных соединений, включающую хиноны, хинолы, хроманолы и хроменолы. В липидном бислое мембран эти формы могут переходить одна в другую. Каждая группа природных АО присутствует в липидах преимущественно в одной, наиболее стабильной для данных соединений форме: витамины группы К находятся в виде хинонов, токоферолы находятся в липидах, в основном, в циклической форме 6-оксихроманов как в виде свободного токоферола, так и в виде его эфиров, для убихинонов наиболее устойчивой является хинонная форма. Гидрохинонная форма убихинонов довольна нестабильна и окисляется кислородом воздуха, однако в клетках до 70% убихинона может находится в восстановленной форме. Более стабильными являются циклические формы - убихроменолы, не участвующие в процессе переноса электрона по дыхательной цепи. Предполагают, что эта форма выполняет в липидах роль АО [23].
Характерной особенностью вышеназванных соединений является наличие в их структуре боковых алифатических заместителей, состоящих из нескольких изопреноидных звеньев, различающихся степенью ненасыщенности.
Хиноны легко реагируют с алкильными радикалами липидов (R), доля которых в общем количестве свободных радикалов при ПОЛ велика, по механизму:+ Q RQ; RQ + R RQR и могут эффективно тормозить окисление.
Хиноны и их производные способны
реагировать с АФК, в частности, хиноны способны связывать радикалы
супероксид-аниона, участвующие в инициировании цепей свободнорадикального
окисления липидов, с образование семихинонов. Вместе с тем предполагают, что
убисемихиноны и убихиноны могут, подобно менасемихинону и менадиолу,
реагировать с молекулярным кислородом с образованием супероксидных
анион-радикалов.
2. Материалы и методы исследования
.1 Общий обзор методов
определения содержания витаминов А и Е
В области изучения витаминов накоплен громадный и разнообразный материал и он свидетельствует о том, что витамины являются органическими соединениями разной химической природы, необходимыми для обеспечения обмена веществ, лежащего в основе всех жизненных процессов. В связи с этим интерес к витаминам со временем не ослабевает, а возрастает еще больше. Особенно важной является разработка методов определения витаминов в различных объектах с целью контроля за их содержанием в продуктах питания, косметических средствах, лекарственных препаратах.
Методы определения содержания витамина А в продуктах.
При количественном определении витамина А в пищевых продуктах используют различные методы: колориметрический, флуоресцентный, способ прямой спектроскопии и ВЭЖХ. Выбор метода определяется наличием той или иной аппаратуры, целью исследования, свойствами анализируемого материала, предполагаемым содержанием витамина А и характером сопутствующих примесей.
Выделение витамина осуществляют кипячением со спиртовым раствором КОН в среде азота; и последующей экстракцией петролейным эфиром.
. Для количественного определения веществ, обладающих А-витаминной активностью, может быть использован метод прямой спектрофотометрии, основанный на способности этих соединений к избирательному светопоглощению на разных длинах волн в УФ области спектра. Поглощение пропорционально концентрации вещества при измерении на тех длинах волн, где наблюдается свойственный данному соединению максимум абсорбции в используемом растворителе. Метод - наиболее простой, быстрый, достаточно специфичный. Дает надежные результаты при определении витамина А в объектах, не содержащих примесей, обладающих поглощением в той же области спектра. При наличии таких примесей метод может быть использован в сочетании со стадией хроматографического разделения.
. Перспективным является флуоресцентный метод, основанный на способности ретинола флуоресцировать под действием УФ лучей (длина волны возбуждающего света 330-360 нм). Максимум флуоресценции наблюдается в области 480 нм. Определению витамина А этим методом мешают каротиноиды и витамин D. Для устранения мешающего влияния используют хроматографию на оксиде алюминия. Недостаток флуоресцентного метода - дорогостоящая аппаратура.
. Ранее наиболее
распространенным являлся колориметрический метод определения витамина А по
реакции с хлоридом сурьмы. Используют раствор хлорида сурьмы в хлороформе
(реактив Карр-Прайса). Механизм реакции точно не установлен и предполагают, что
в реакцию вступает примесь SbCL5 в SbCl3. Образующееся в реакции соединение
окрашено в синий цвет. Измерение оптической плотности проводят при длине волны
620 нм в течение 3-5 секунд. Существенным недостатком метода является
неустойчивость развивающейся окраски, а также высокая гидролизуемость SbCl3.
Предполагается, что реакция протекает следующим образом:
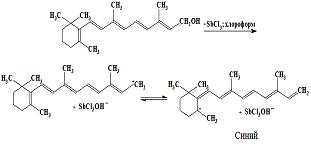
Эта реакция для витамина А не специфична, аналогичное окрашивание дают каратиноиды, но хроматографическое разделение этих соединений позволяет устранить их мешающее влияние.
Определению витамина А перечисленными методами, как правило, предшествует подготовительная стадия, включающая щелочной гидролиз жироподобных веществ и экстракцию неомыляемого остатка органическим растворителем. Часто приходится проводить хроматографическое разделение экстракта.
. В последнее время вместо колоночной хроматографии находит все более широкое применение ВЭЖХ, которая позволяет разделить жирорастворимые витамины (A, D, E, K), обычно присутствующие одновременно в пищевых продуктах, и количественно их определить с большой точностью. ВЭЖХ облегчает определение различных форм витаминов (витамин А-спирт, его изомеры, эфиры ретинола), что особо необходимо при контроле за внесением витаминов в пищевые продукты.
Методы определения содержания витамина Е в продуктах.
К группе веществ, объединяемых общим названием «витамин Е» относятся производные токола и триенола, обладающие биологической активностью a-токоферолла. Кроме a-токоферолла, известно еще семь родственных ему соединений, обладающих биологической активностью. Все они могут встречаться в продуктах. Следовательно, главная трудность при анализе витамина Е состоит в том, что во многих случаях приходится рассматривать группу соединений, имеющих большое химическое сходство, но одновременно различающихся по биологической активности, оценить которую можно только биологическим методом. Это трудно и дорого, поэтому физико-химические методы почти полностью вытеснили биологические.
Основные стадии определения витамина Е: подготовка образца, щелочной гидролиз (омыление), экстракция неомыляемого остатка органическим растворителем, отделение витамина Е от мешающих анализу веществ и разделение токоферолов с помощью различных видов хроматографии, количественное определение. Токоферолы очень чувствительны к окислению в щелочной среде, поэтому омыление и эктсракцию проводят в атмосфере азота и в присутствии антиоксиданта (аскорбиновой кислоты). При омылении могут разрушаться ненасыщенные формы (токотриенолы). Поэтому при необходимости определения всех форм витамина Е, содержащихся в продукте, омыление заменяют другими видами обработки, например, кристаллизацией при низких температурах.
. Большинство физико-химических методов определения витамина Е основано на использовании окислительно-восстановительных свойств токоферолов. Для определения суммы токоферолов в пищевых продуктах наиболее часто используют реакцию восстановления трехвалентного железа в двухвалентное токоферолами с образованием окрашенного комплекса Fe(2+) с органическими реагентами. Наиболее часто используют 2,2’ - дипиридил, с которым Fe(2+) дает комплекс, окрашенный в красный цвет (лmax = 500 нм). Реакция не специфична. В нее также вступают каротины, стиролы, витамин А и др. Кроме того, интенсивность окраски существенно зависит от времени, температуры, освещения. Поэтому для повышения точности анализа токофероллы предварительно отделяют от соединений, мешающих определению, методом колоночной, газожидкостной хроматографии, ВЭЖХ. При определении Е-витаминной ценности продуктов, в которых a-токоферол составляет более 80% общего содержания токоферолов (мясо, молочные продукты, рыба и др.), часто ограничиваются определением суммы токоферолов. Когда в значительных количествах присутствуют другие токоферолы (растительные масла, зерно, хлебобулочные изделия, орехи), для их разделения используют колоночную хроматографию.
. Для определения суммы токоферолов может быть использован также флуоресцентный метод. Гексановые экстракты имеют максимум флуоресценции в области 325 нм при длине волны возбуждающего света 292 нм.
. Для определения индивидуальных
токоферолов несомненный интерес представляет метод ВЭЖХ, обеспечивающий в одном
процессе как разделение, так и количественный анализ. Метод также
характеризуется высокой чувствительностью и точностью. Детектирование проводят
по поглощению или по флуоресценции.
2.2 Определение
количественного содержания витаминов А и Е в морепродуктах
Определение количественного содержания витаминов А и Е проводилось на образцах четырех видов замороженных морепродуктов (креветка, осьминог, кальмар, мидия) и трех видах замороженной морской рыбы (минтай, путассу, камбала). Исследовали по пять параллельных образцов каждого объекта, в которых определяли содержание витаминов А и Е.
Методика определения количественного содержания витаминов А и Е.
В центрифужные пробирки помещается растертое мясо морепродукта (навеска 1 г), 1 мл спирта и 1 мл дистиллированной воды. Пробирки закрывают крышками и перемешивают содержимое осторожными встряхиваниями. Затем добавляют по 5 мл гексана и еще раз производят встряхивание. Затем центрифугируют в течении 10 минут при 1500 об/мин.
Четко отделившийся гексановый слой используют для проведения измерений.
Определение содержания витаминов А и Е проводили на анализаторе «Флюорат».
Градуировку прибора «Флюорат» осуществляли путем измерения сигналов флуоресценции, приготовленных растворов. Контроль стабильности градуировочной характеристики состоит в проведении измерений концентрации витаминов в нескольких смесях. Градуировка признается стабильной, если полученное значение концентрации витаминов в смеси отличается от известного не более, чем на 10% в диапазоне 0,5 -2,0 мг/дм3 и 20% при более низких концентрациях. При несоответствии полученных результатов указанным нормативам процесс градуировки необходимо повторить.
В основу работы прибора положен флуориметрический метод измерения содержания органических и неорганических веществ в области спектра 250-900 нм (например, витамин Е диапазон 300-320 нм). Для анализа использовались кюветы 10х20 мм. Во время работы на «Флюорате» необходимо выбрать из меню необходимую методику, затем измерить фоновый сигнал, после установить кювету с пробой и запустить процесс измерения.
В качестве светофильтров при измерения витамина Е применяют светофильтр возбуждения Е-1 (292 нм) и светофильтр регистрации Е-2 (320 нм). В качестве светофильтров при анализе витамина А используют светофильтр возбуждения А-1 (335) нм) и светофильтр регистрации А-2 (460 нм).
Этот метод определения содержания
витаминов был выбран в связи с наличием необходимого оборудования и простотой
использования.
2.3 Определение
содержания диеновых конъюгатов в морепродуктах
Помимо того что о антиоксидантной активности морепродуктов можно судить по содержанию витаминов А и Е так и по содержанию диеновых конъюгатов.
К первичным продуктам перекисного окисления липидов относятся циклические эндоперекиси и алифатические моно- и гидроперекиси, так называемые липопероксиды и диеновые конъюгаты [25].
Определение диеновых конъюгатов имеет значительное преимущество для оценки ПОЛ, поскольку отражает раннюю стадию окисления. Обычным субстратом для определения диеновых конъюгатов выступает любое вещество, содержащее полиненасыщенные жирные кислоты.
Свободнорадикальное, или перекисное, окисление липидов (ПОЛ) представляет собой самоподдерживающуюся цепную реакцию, продукты которой в умеренных количествах необходимы для осуществления таких функций организма, как обновление биологических мембран, фагоцитоз, регуляция артериального давления и т.д., но в больших - вредны, поскольку нарушают структуру клеточных мембран [26].
При свободнорадикальном окислении арахидоновой кислоты происходит отрыв водорода в б-положении по отношению к двойной связи, что приводит к перемещению этой двойной связи с образованием ДК [27].
Диеновые конъюгаты относятся к токсическим метаболитам, которые оказывают повреждающее действие на липопротеиды, белки, ферменты и нуклеиновые кислоты [28].
Определение диеновых конъюгатов имеет значительное преимущество для оценки ПОЛ, поскольку отражает раннюю стадию окисления. Обычным субстратом для определения диеновых конъюгатов выступает любое вещество, содержащее полиненасыщенные жирные кислоты.
Диеновые конъюгаты обладают поглощением в УФ-области (л = 232 нм), коэффициент молярной экстинкции 2,2∙105 см-1 ∙М -1. Пробоподготовка для анализа диеновых конъюгатов обязательно включает в себя экстрагирование липидов органическими растворителями.
а) Экстракция диеновых конъюгатов из сыворотки крови или ткани гептан-изопропанольной смесью, с последующим измерением оптической плотности в гептановой или изопропанольной фазе (л= 232-234 нм).
б) При анализе с использованием ВЭЖХ, установлено, что диеновые конъюгаты, образующиеся в организме человека, в основном представлены изомерами линолевой кислоты, октодека-9 цис -, транс - диеновой кислоты.