Материал: микра от 104 группы
23. Бактерии рода Clostridium. Брожения, вызываемые этими бактериями. Ход и конечные продукты. Значение этих процессов для сельского хозяйства
Анаэробные бактерии рода Clostridiumбыли открыты Л. Пастером в 1861 г. Сейчас среди представителей Clostridiumнасчитывается более 80 видов бактерий. Они имеют палочковидные клетки, обычно подвижны, передвигаются при помощи перитрихальных жгутиков. У видов рода образуются споры, имеющие овальную или сферическую форму; они терморезистентны. Как правило, споры раздувают клетку (рис. 38). Грамположительные. Облигатные анаэробы.
Род включает психрофильные, мезофильные и термофильные виды. Температурный оптимум для роста большинства мезофиль- ных видов лежит в диапазоне 30—40 °С. Для термофильных видов температурный оптимум составляет 60—75 °С. Оптимальная реакция среды для клосгридий — нейтральная или слабощелочная. Хемоорганогетеротрофы. Клостридии сбраживают сахара, многоатомные спирты, аминокислоты, органические кислоты, пурины и пи- римидины, другие органические соединения. Ряд видов способен к фиксации молекулярного азота атмосферы. Места обитания кло- сгридий — почва, водоемы, а также пищеварительный тракт человека и животных.
Все виды рода объединены в группы в зависимости от способности сбраживать те или иные органические соединения.
Первая группа — сахаролитическиевиды Clostridium,сбраживающие растворимые углеводы, крахмал или пектин с образованием бутирата, ацетата, С02 и Н2. Брожение при участии некоторых микроорганизмов группы приводит к образованию из сахаров дополнительных нейтральных соединений (бутанола, пропанола, ацетона, небольших количеств этанола). В группу входят бактерии, вызывающие маслянокислое и ацетонобутиловое брожения: С. butyri- сит, С. pasteurianum, С. tyrobutyricum, С. butylicum, С. acetobutylicum и др. Возможно, к ней можно отнести и ряд видов Clostridium —вы- сокоспециализированных агентов анаэробного разрушения целлюлозы, причем главные конечные продукты брожения — этанол, ацетат и сукцинат, СО, и Н2.
Вторая группа — протеолитическиевилы Clostridium,сбраживающие аминокислоты. Обладают сильными протеолитическими свойствами и способны к интенсивному гидролизу белков с последующим сбраживанием аминокислот. Рост микроорганизмов в средах с белком сопровождается образованием аммиака, С02, Н2, жирных кислот и большого количества летучих соединений с неприятным запахом. К группе относятся виды: С. sporogenes,С. per- fringens,С. histolyticum, С. botulinumи др. Многие представители рода Clostridium, сбраживающие аминокислоты, способны также к сбраживанию углеводов.
Третья группа — виды Clostridium, сбраживающие азотсодержащие циклические соединения —пурины и пиримидины. Пурины (гуанин, гипоксантин, ксангин и др.) под влиянием С. acidi-urici и С. cylindrosporumпревращаются в аммиак, ацетат и С02. С. и racili- сити С. oroticumсбраживают пиримидины, при этом урацил распадается до (i-аланина, С02 и NH3, а оротовая кислота — до уксусной кислоты, С02 и NHV
Четвертая группа включает всего один вид — С. kluyveri, сбраживающий смесь этанола с ацетатомдо бутирата и капроновой кислоты, а также небольшого количества водорода.
Маслянокислое брожение
Маслянокислое брожение — метаболический путь превращения органических веществ облигатно анаэробных бактерий, конечными продуктами которого являются АТФ, а также масляная кислота, бутанол, ацетон, изопропанол, этанол, уксусная кислота, углекислый газ и водород.
Маслянокислое брожение начинается с трансформации сахаров в пируват по пути Эмбдсна— Мейергофа— Парнаса. Конечные продукты из пирувата образуются в цепи последовательных реакций, катал изуемых несколькими ферментными системами. Остановимся на кратком описании данного процесса.
Пируват превращается в ацетил-СоА, С02 и Н, при участии ферментной системы: пируват + ферредоксиноксидоредуктаза. Из ацетил-КоА через а цетил фосфат синтезируется ацетат. Синтез бугирата начинается с конденсации двух молекул ацетил-КоА, возникших в результате декарбоксил ирования пиру вата, что приводит к образованию ацетоацетил-КоА. Последний восстанавливается в (3-оксибу- тирил-КоА. С отщеплением от молекулы Р-оксибутирил-КоА молекулы воды возникает кротонил-КоА, ферментативно восстанавливающийся в бутирил-КоА. Наконец, после гидролиза бутирил-КоА и переноса КоА на ацетат образуется бутират.
Превращение ацетил-КоА в ацетилфосфат, а затем в ацетат сопровождается синтезом АТФ. Таким образом, в процессе субстратного фосфорилирования при маслянокислом брожении синтезируется третья молекула АТФ (две другие образовались в процессе гликолитического расщепления глюкозы). Суммарное уравнение маслянокислого брожения:
4C6H12O6 = 3CH3CH2CH2COOH + 2CH3COOH + 8CO2 + 8H2
Мслянокислое брожение — не всегда желательный процесс. Например, при его развитии в заквашиваемых кормах белковая часть корма разлагается, а накопившаяся масляная кислота придает продукту неприятный запах. Вместе с тем для некоторых промышленных целей требуется чистая масляная кислота. Ее получают на заводах, специально сбраживая подготовленные среды чистой культурой маслянокислых бактерий. Образовавшуюся кислоту отделяют и очищают химическим методом.
Ацетонобутиловое брожение.
Возбудитель ацетонобутилового брожения — С. acetobutylicum, он широко распространен в почвах, имеет палочковидные клетки (0,6—0,9 х 2,4—4,7 мкм) с пери- трихальным жгутикованием. Характерно образование овальных спор, которые располагаются в клетке субтсрминально. Бактерии сбраживают моно-, ди- и полисахариды, а также глицерин, маннит, глюконат, пируват и ряд других соединений, фиксируют молекулярный азот. Оптимальная температура для их роста 37—38 °С, оптимальное значение pH среды — 5,1—6,9. Ацетонобутиловые бактерии способны разлагать белки.
Сбраживание углеводов при помощи данных бактерий происходит по пути Эмбдена— Мейергофа—Парнаса. Образовавшийся в результате декарбоксил ирования пирувата ацетил-КоА восстанавливается в этанол, идет на синтез ацетата или конденсируется в ацетоацетил-КоА. Последний декарбоксилируется, что приводит к образованию ацетона, или восстанавливается в бутирил-КоА, который может трансформироваться в бутират или восстанавливаться через бутиральдегид до бутанола. Суммарная схема ацетонобутилового брожения:
C6H12O6 -> CH3CH2CH2CH2OH + CH3COCH3 + CH3CHOHCH3 + H2 + CO2
Основные конечные продукты брожения, как видно, — бутанол, этанол, ацетон, 2-пропанол, а также ацетат и бутират. Однако характер конечных продуктов определяется как видовой принадлежностью используемого для брожения микроорганизма, так и условиями, в которых идет процесс. Установлено, что ацетонобутиловое брожение имеет двухфазный характер. В течение первой фазы наблюдается активный рост бактерий, в среде идет накопление преимущественно органических кислот. Во второй фазе брожения снижается значение pH среды, рост бактерий замедляется, преобладает синтез нейтральных продуктов — ацетона, бутанола и этанола.
Двухфазность ацетонобутилового брожения связана с pH среды. Если кислотность среды в результате накопления органических кислот возрастает до pH 4,5 и более, происходит интенсивное образование нейтральных продуктов, что предупреждает дальнейшее подкисление среды, неблагоприятное для бактерий.
Ацетонобутиловые бактерии значительно более требовательны к среде, чем маслянокислые. Эти микроорганизмы нуждаются в готовых аминокислотах и витаминах (биотин и //-аминобензойная кислота).
Описанный вид брожения широко используют в промышленном производстве ацетона и бутанола из кукурузной муки и другого крахмалистого сырья. Ацетон применяют для производства искусственного шелка и кожи, фотографических пленок, искусственного цемента и других продуктов, бутанол — при производстве лаков. Газы, образующиеся при ацетонобутиловом брожении, идут на синтез метанола.
Смешанное брожение.
Некоторые бактерии, главным образом представители кишечной микрофлоры, относящиеся к семейству Enterobacteriaceae, называемые энтеробактериями, могут осуществлять смешанное кислое и бутандиоловое брожение, при котором образуются ряд органических кислот, спирты, С02 и Н2. Энтеробактерии — факультативные анаэробы, они представляют собой грамот- рицательные подвижные, неспорообразующие палочки.
К энтеробактериям относятся:
• Escherichia coli (кишечная палочка) — обитает в кишечнике человека и животных; бактерия может существовать в почве и воде, обнаружение ее в питьевой воде, молоке или другом субстрате служит показателем их загрязнения фекалиями;
• Salmonella — представители кишечной микрофлоры, патогенные микроорганизмы, возбудители кишечных инфекций и нишевых отравлений, обитают в почве и воде;
• Shigella — возбудители кишечных инфекций;
• Yersinia — возбудители чумы человека и животных;
• Enterobacter, Serratia и Proteus, представители которых в основном обитают в почве и воде, а также
• фитопатогенный род Erwinia.
Превращение углеводов у энтеробактерий идет по пути Эмб- дена—Мейергофа—Парнаса. Основные продукты брожения — ацетат, сукцинат, лактат, этанол, глинерол, ацетон, 2,3-бутандиол, С02 и Н2. Продукты брожения, вызываемого представителями энтеробактерий, различаются в качественном и количественном отношении. Виды родов Escherichia. Salmonella и Shigella сбраживают сахара до лактата, ацетата, сукцината и муравьиной кислоты. Кроме того, образуются С02, Н2 и этанол. Представители родов Enterobacter, Serratia и Erwinia продуцируют меньше кислот, но больше С02, этанола и особенно большое количество 2,3-бутандиола (2,3-бугиленгликоля).
24. Нитрификация. Возбудители, их особенности, химизм процесса, значение для почвы и при хранении навоза.
Нитрификация – аммиак, образующийся в почве, навозе и воде при разложении органических веществ, довольно быстро окисляется до азотистой, а затем азотной кислоты. Нитрификаторы оказались хемолитоавтотрофами, т. е. бактериями, использующими энергию окисления аммиака или азотистой кислоты для синтеза органических веществ из СО2 (хемосинтез). Поэтому их клетки очень чувствительны к присутствию в среде органических соединений. Нитрифицирующие бактерии удалось выделить на минеральных питательных средах.
С. Н. Виноградский установил, что существуют две группы нитрификаторов:
окисление аммиака до азотистой кислоты (NH+4 > NO-2)
окисление азотистой кислоты до азотной (NO-2 > NO-3).
Представителей обеих групп относят к семейству Nitrobacteriaceae – это одноклеточные грамотрицательные бактерии. Среди нитрифицирующих бактерий есть палочковидные клетки, эллиптические, сферические, извитые и дольчатые, плеоморфные. Существуют подвижные и неподвижные формы с полярным, субполярным и перитрихальным жгутикованием. Размножаются бактерии-нитрификаторы в основном делением. Почти у всех нитрификаторов хорошо развита система внутри цитоплазматических мембран, значительно различающихся по форме и расположению в клетках отдельных видов. Мембраны цитоплазмы подобны мембранам фотосинтезирующих пурпурных бактерий.
Первая фаза:
Род: Nitrosomonas, Nitrosococcus, Nitrosospira, Nitrosolobus и Nitrosovibrio. Наиболее детально к настоящему времени изучен Nitrosomonaseuropaea. Он представляет собой короткие овальные палочки. В жидкой культуре клетки Nitrosomonas проходят ряд стадий развития. Две основные из них представлены подвижной формой и неподвижными зооглеями. Подвижная форма обладает субполярным жгутиком или пучком жгутиков. Описаны представители и других родов бактерий, вызывающих первую фазу нитрификации.
Вторая фаза:
Род: Nitrobacter, Nitrospira и Nitrococcus. Наибольшее число исследований проведено с Nitrobacter winogradskyi, однако описаны и другие виды (например, Nitrobacter agilis). Клетки нитробактepa имеют удлиненную, клиновидную или грушевидную форму, более узкий конец часто загнут в клювик. При почковании дочерняя клетка обычно подвижна, так как имеет один полярный жгутик. Известно чередование в цикле развития подвижной и неподвижной стадий.
Нитрифицирующие бактерии культивируют на простых минеральных средах, содержащих аммиак или нитриты (окисляемые субстраты) и диоксид углерода (основной источник углерода). Источником азота для этих организмов служат аммиак, гидроксиламин и нитриты.
Нитрифицирующие бактерии развиваются при рН 6,0—8,6, оптимум реакции среды составляет рН 7,5—8,0. При значениях ниже рН 6 и выше рН 9,2 бактерии не развиваются. Оптимальная температура для развития нитрификаторов 25—30 °С.
Нитрификаторы — облигатные аэробы. Используя кислород воздуха, они окисляют аммиак до азотистой кислоты (первая фаза нитрификации), а затем азотистую кислоту до азотной (вторая фаза нитрификации).
С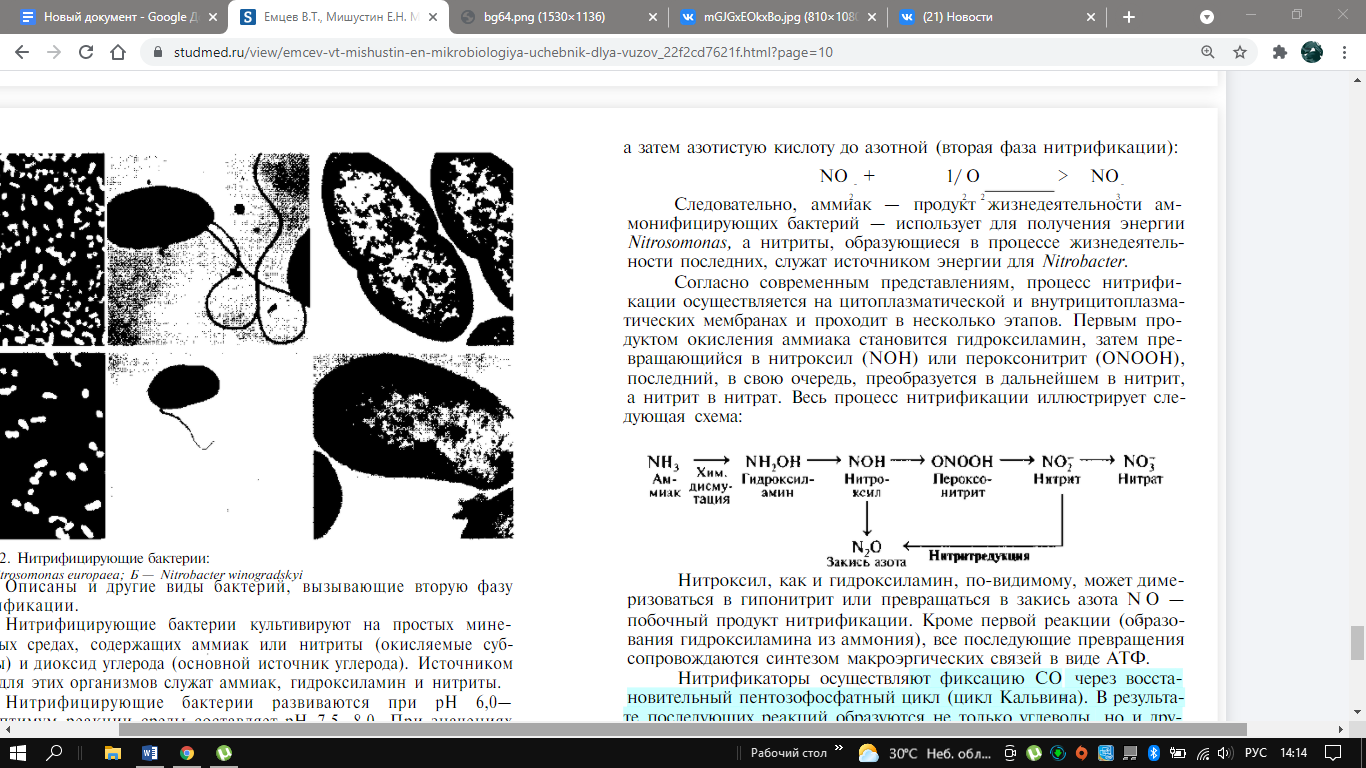 ледовательно,
аммиак — продукт жизнедеятельности
аммонифицирующих бактерий — использует
для получения энергии Nitrosomonas, а
нитриты, образующиеся в процессе
жизнедеятельности последних, служат
источником энергии для Nitrobacter.
ледовательно,
аммиак — продукт жизнедеятельности
аммонифицирующих бактерий — использует
для получения энергии Nitrosomonas, а
нитриты, образующиеся в процессе
жизнедеятельности последних, служат
источником энергии для Nitrobacter.
Накопление нитратов происходит с неодинаковой интенсивностью на разных почвах. Чем богаче почва, тем больше соединений азотной кислоты она может накапливать. Существует метод определения доступного растениям азота в почве по показаниям ее нитрификационной способности. Следовательно, интенсивность нитрификации можно использовать для характеристики агрономических свойств почвы. Вместе с тем при нитрификации происходит лишь перевод одного питательного для растений вещества — аммиака в другую форму — азотную кислоту. Нитраты, однако, обладают некоторыми нежелательными свойствами. В то время как ион аммония поглощается почвой, соли азотной кислоты легко вымываются из нее. Кроме того, нитраты восстанавливаются в результате денитрификации до N2, что также обедняет азотный запас почвы. Все перечисленное существенно снижает коэффициент использования нитратов растениями.
Нитрификации и денитрификации азота в навозе не происходит, так как бактерии-нитрификаторы в аэробных условиях погибают при высокой температуры, а в анаэробных условиях не могут существовать. Также на них губительно действуют высокие концентрации аммиака и повышенное содержание растворимых органических соединений.