Материал: мфт 3 семинар-1
Мфт. Семинар №3
Вопрос 1. Качество медицинских товаров. Понятие. Определение.
Качество товаров – совокупность потребительских свойств товаров,
обусловливающих их способности удовлетворять определенные потребности в соответствии с их назначением.
Качество имеет 2 стороны: техническую и экономическую
Под свойством продукции понимают ее объективную особенность,
проявляющуюся при производстве, эксплуатации или потреблении.
Качество лекарственного средства – совокупность свойств, которые придают ЛС
способность удовлетворять потребителей соответственно своему назначению и отвечают требованиям, установленным законодательством и НД
Вопрос 2. Показатели качества. Характеристика, виды показателей.
Квалиметрия – область практической и научной деятельности, связанная с
разработкой теоретических основ и методов измерения и количеств. оценки качества.
Показатель качества товаров – это количественная характеристика
применительно к конкретным условиям производства и потребления, регламентируемая нормативной документацией (имеет наименование и значение)
В товароведении показатели качества классифицируют по следующим признакам:
1. Количеству характеризуемых свойств (единичные и комплексные);
Единичные показатели характеризуют одно свойство продукции (например,
шероховатость металлической поверхности, водоустойчивость стекла и др.)
Комплексные показатели характеризуют совокупность нескольких свойств
продукции (например, надёжность, безопасность и др.).
2. Назначению (определяющие и интегральные);
Определяющие показатели – показатели, по которым принимают решение
оценивать качество продукции (ГОСТ 15467-79)
Интегральные показатели качества выражают через соответствующую сумму
экономических или технических показателей (например, общий полезный эффект от использования медицинского изделия, общие затраты на его создание и эксплуатацию)
3. Способу выражения (в натуральных единицах и баллах);
4. Методу определения (органолептические, инструментальные,
социологические, экспертные)
5. Области применения (единицы продукции, совокупности единиц однородной
продукции, совокупности единиц разнородной продукции);
6. Стадии определения (на стадии проектирования, на стадии производства,
на стадии потребления).
Вопрос 3. Основные критерии качества лекарственных средств.
Безопасность лекарственных средств – характеристика ЛС, основанная на
сравнительном анализе их эффективности и оценке риска причинения вреда здоровью.
Биодоступность лекарственных веществ отражает содержание свободного
вещества в плазме крови через определенный промежуток времени после его приема относительно исходной дозы препарата.
Эффективность лекарственных средств – характеристика степени
положительного влияния лекарственных средств на течение болезни.
Аутентичность (подлинность)
Вопрос 4. Понятие "единичный", "комплексный", "интегральный" показатели. Характеристика.
Единичные показатели характеризуют одно свойство продукции (например,
шероховатость металлической поверхности, водоустойчивость стекла и др.)
Комплексные показатели характеризуют совокупность нескольких свойств
продукции (например, надёжность, безопасность и др.).
Интегральные показатели качества выражают через соответствующую сумму
экономических или технических показателей (например, общий полезный эффект от использования медицинского изделия, общие затраты на его создание и эксплуатацию)
Вопрос 5. Обеспечение качества в сфере обращения лекарственных средств.
Фармацевтическая продукция, как и другие группы товаров, проходит
различные этапы жизненного цикла (петли качества). Качество продукции планируется и формируется в производственной сфере (в процессе проектирования или планирования, а также в процессе производства или осуществления) и подвергается изменениям в потребительской (в течение эксплуатации).
Требования каждого этапа отражены в соответствующих руководствах
по надлежащим практикам.
В большинстве стран стандарты надлежащих практик – это требования,
предъявляемые организациями здравоохранения на этапе разработки, исследований, производства и реализации лекарственных средств.
Руководства по надлежащим практикам устанавливают стандарты
качества на различных этапах жизненного цикла лекарственных средств. Все надлежащие практики представляют собой звенья одной цепи, так как каждая практика занимает свой сегмент жизненного цикла продукции.
Надлежащие практики
Надлежащая лабораторная практика (Good Laboratory Practice - GLP) –
совокупность правил по планированию, выполнению, контролю, оценке и документированию лабораторных исследований, которые являются частью доклинического изучения лекарственных средств и обеспечивают качество, точность и полноту полученных данных.
Надлежащая клиническая практика (Good Clinical Practice - GCP) –
совокупность правил по планированию, выполнению, оценке и документированию клинических испытаний лекарственных средств, соблюдение которых обеспечивает точность полученных данных, защиту прав лиц, которые принимают участие в испытаниях, конфиденциальность данных об этих лицах.
Надлежащая производственная практика (Good Manufacturing Practice –
GMP) – комплекс правил по организации производства и контроля качества, которые являются элементом системы обеспечения качества. Соблюдение требований надлежащей производственной практики обеспечивает стабильное производство лекарственных средств согласно требованиям нормативно-технической документации и проведения контроля качества в соответствии с аналитической нормативной документацией.
Надлежащая практика хранения фармацевтической продукции (Guide to
Good Storage Practice for Pharmaceuticals - GSP) – специальные меры, необходимые для правильного хранения и транспортирования фармацевтической продукции. Эти меры при необходимости можно адаптировать к конкретной ситуации при условии соблюдения всех стандартов качества.
Надлежащая практика дистрибуции (Good Distribution Practice - GDP) –
комплекс правил и требований к дистрибуции, соблюдение которых обеспечивает качество лекарственных средств в процессе управления и организации их оптовой реализации на всех ее этапах.
Надлежащая аптечная практика (Good Pharmaceutical Practice - GPP) –
деятельность, связанная с поставками, хранением и применением лекарственных средств и изделий медицинского назначения, осуществляемая в аптеках, лечебных учреждениях и домашних условиях.
Надлежащая практика для национальных лабораторий контроля
лекарственных средств (Good Practices for National Pharmaceitical Control Laboratories - GPCL/WHO) – это совокупность критериев работы лаборатории контроля лекарственных средств, обеспечивающих основу для правильной оценки результатов и выводов о соответствии качества лекарственных средств требованиям спецификаций.
Вопрос 6. Показатели качества медицинских товаров.
Показатель качества товаров – это количественная хар-ка применительно к
конкретным условиям производства и потребления, регламентируемая НД
Вопрос 7.Стандарты. Виды стандартов.
Качество товара регламентируется стандартом.
Стандарт – официальный государственный или нормативный документ отрасли,
предприятия, фирмы, устанавливающий необходимые качественные характеристики, требования, которым должен удовлетворять данный вид продукции, товара.
В зависимости от региона и сферы действия различают стандарты:
1. Международные – принятые исо (iso – International Organization for
Standardization) или другими уполномоченными международными организациями по стандартизации отдельных видов продукции, например ЕКН и ЕКЭН; имеют рекомендательный статус. В нашей стране такой стандарт может быть применен с заимствованием отдельных положений, при этом дается ссылка в ГОСТ на первоисточник.
2. Межгосударственные – принятые Россией и рядом стран Содружества
независимых государств (СНГ). Их применяют на основании постановления национального комитета по стандартизации без переоформления.
3. Национальные (принятые национальным органом РФ). Их разрабатывают на
продукцию и услуги, имеющие межотраслевое значение.
К национальным относятся следующие категории стандартов РФ:
Государственный стандарт Российской Федерации (ГОСТ Р или ГОСТ) –
принимается Федеральным агентством по техническому регулированию и метрологии. Он составляется на организационно-методические и общетехнические объекты, продукцию, работы и услуги, имеющие межотраслевое и общенародное значение, поэтому является обязательным для всех предприятий, организаций и учреждений российского, республиканского и местного подчинения во всех отраслях народного хозяйства России;
Отраслевой стандарт (ОСТ) – принимается государственным органом управления
в пределах его компетенции. Он обязателен для всех предприятий и организаций других отраслей, применяющих или потребляющих продукцию этой отрасли. Такие стандарты устанавливаются на сырье, полуфабрикаты, используемые в данной отрасли, а также на отдельные виды товаров народного потребления. Утверждаются отраслевые стандарты министерством (ведомством), являющимся ведущим в производстве данной продукции.
Стандарт предприятия (СТП) – принимается предприятием. Он отражает
присущие каждому предприятию особенности технологического процесса получения товара и содержит перечень показателей качества, которые должны быть не ниже требований ГОСТа или ОСТа на аналогичную продукцию.
Стандарт научно-технического объединения (СТО) – принимается научно-
техническим, инженерным обществом или другим общественным объединением.
Стандарты административно-территориальной единицы. Создание таких
стандартов особенно важно для России, где разграничены обязанности и компетенция федерального и административно-территориального уровня по оказанию медицинской помощи. Поскольку здравоохранение финансируется главным образом за счет средств субъектов Российской Федерации, их роль важна в развитии системы стандартизации и обеспечения качества оказания медицинской помощи.
На некоторые виды товаров, в том числе и медицинские, разрабатывают
технические условия.
Вопрос 8. Определение понятий: нормативная документация, технические условия. Разделы ту.
Нормативный документ – документ, устанавливающий правила, общие принципы
или характеристики, касающиеся различных видов деятельности или их результатов (ГОСТ Р 1.0). Термин "нормативный документ" является родовым, охватывающим такие понятия, как стандарты и иные нормативные документы по стандартизации - правила, рекомендации, регламенты, общероссийские классификаторы.
Стандарт на продукцию – это нормативно-технический документ,
устанавливающий требования, которым должна удовлетворять продукция или группа продукции с тем, чтобы обеспечить ее соответствие своему назначению.
Основные виды стандартов:
Государственный стандарт России (ГОСТ Р или ГОСТ) – это тип
стандарта, который разрабатывается на продукцию, работы и услуги, потребности в которых носят межотраслевой характер.
Его обозначение:
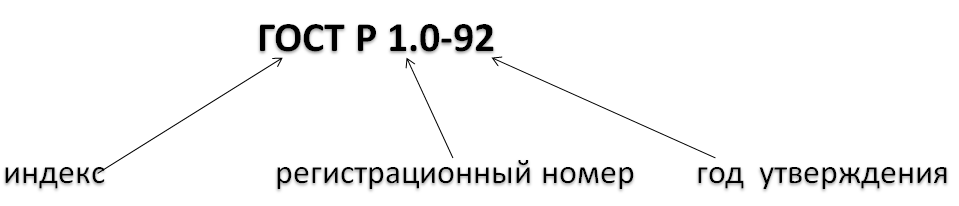
Отраслевой стандарт (ОСТ) - тип стандарта, разрабатываемый в случае
отсутствия ГОСТ Р или при необходимости установления требований, расширяющих установленных ГОСТом Р.
Устанавливается на дополнительные технические требования и групповые
характеристики, необходимые для изготовления и поставки ЛС (термины, обозначения, правила приемки, маркировка, упаковка, хранение, транспортирование и др.);
Утверждаются МЗ РФ и медицинской промышленности.
Его обозначение:
ОСТ 42-0002-16
ОСТ - индекс
42 - условное обозначение министерства или ведомства,
0002 – регистрационный номер в управлении по внедрению новых ЛС
16 - год утверждения.
Стандарт предприятия (СТП) - разрабатывается в случае отсутствия ГОСТ Р или
ОСТ на объект стандартизации.
Его обозначение:
СТП 424-11,
где
СТП - индекс,
424 - регистрационный номер,
11 - год утверждения.
Технические условия (ТУ) - это нормативно-технический документ,
устанавливающий технические требования, которым должна удовлетворять продукция,
процесс или услуга.
ТУ 64-1 323-19,
ТУ – индекс
64 - номер министерства и ведомства
323 - регистрационный номер
19- год утверждения.
Они могут быть стандартом или частью стандарта.
ТУ разрабатывают на одно конкретное изделие, материал или вещество либо
на несколько конкретных изделий, материалов, веществ и т.п. (групповые ТУ).
Требования, установленные ТУ, не должны противоречить обязательным
требованиям государственных (межгосударственных) стандартов, распространяющихся на данную продукцию.
Контроль качества готовых медицинских товаров и БАДов осуществляется
в соответствии с ТУ.
Стандарт качества ЛС – это НД, содержащий перечень нормируемых показателей
и методов контроля качества ЛС, утверждаемый МЗ РФ
Виды НД на ЛС:
Общая фармакопейная статья (ОФС) – гос. стандарт качества ЛС. Включает в себя
перечень нормируемых показателей или методов испытания для конкретной лекарственной формы, описание физических, физико-химических, химических, биохимических, биологических, микробиологических методов анализа ЛС, требования к используемым реактивам, титрованным растворам, индикаторам.
Его обозначение:
ОФС-42-0007-19
ОФС - индекс,
42 - условное обозначение министерства или ведомства,
0007 - регистрационный номер,
19 - год утверждения
Фармакопейная статья (ФС) – гос. стандарт качества ЛС под международным
непатентованным наименованием (МНН), содержит обязательный перечень показателей и методов контроля качества с учетом его лекарственной формы.
ФС утверждаются на ЛС, имеющие наибольшую терапевтическую ценность,
широко вошедшие в медицинскую практику и имеющие высокие качественные показатели. ФС включаются в государственную фармакопею (серийное производство).
Её обозначение:
ФС-42-00018-17
ФС -индекс,
42 - условное обозначение министерства или ведомства,
00018 – регистрационный номер,
17- год утверждения
Фармакопейная статья предприятия (ФСП) – стандарт качества на ЛС под
торговым наименованием, содержащий перечень показателей и методов контроля качества ЛС, произведенного конкретным предприятием, учитывающий конкретную технологию данного предприятия и прошедший экспертизу, и регистрацию в установленном порядке.
Его обозначение:
ФСП-42-0208-00046-12
ФСП - индекс,
42 - условное обозначение министерства или ведомства,
0208 - код предприятия,
00046 – регистрационный номер стандарта,
12 - год утверждения.