Материал: Методи вирощування кристалів
При температурі плавлення руйнується кристалічна структура, розпадається правильний лад частинок.
Для всіх кристалів однокової речовини, при постійних умовах
температура плавлення однакова, а для різних речовин вона різна. Кристал
кам'яної солі починає плавитися точно при 804° С, кристал кварцу при 1470° С.
Всі кристали під час плавлення зберігають постійну температуру. Саме на ці
властивості кристалів заснований пристрій термометра. Нуль градусів за шкалою
термометра - це температура, при якій в звичайних умовах тануть, тобто плавляться,
кристали льоду. Температура плавлення кристала залежить від тиску, під яким цей
кристал перебуває (рис. 2).
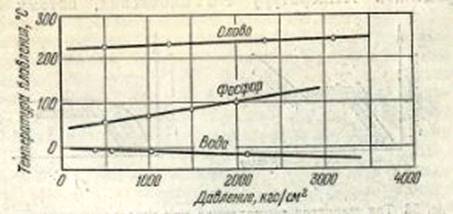
Рис. 1.4 Залежність температури плавлення кристалів від тиску
У дослідах з колосальними тисками аж до десятків тисяч атмосфер вдалося міняти температури плавлення кристалів навіть на сотні градусів. Наприклад, якщо підвищити тиск до 12 тисяч атмосфер, то температура плавлення кристалів калію підвищиться з 62 до 179° С, а у кристалів аніліну вона зросте ще сильніше: щоб розплавити під таким тиском кристал аніліну, його доведеться нагрівати до 199° С, тоді як при атмосферному тиску він плавиться вже при - 6° С. А ось у кристалів вісмуту при такому ж підвищення тиску температура плавлення не збільшиться, а зменшиться: для плавлення достатньо буде нагріти кристал вісмуту до 218° С, тоді як в нормальних умовах він плавиться при 271° С Тиск впливає на температуру плавлення всіх кристалів, але вплив для різних речовин особливий: в одних він сильніший, в інших слабший; у деяких речовин при підвищенні тиску температура плавлення зростає, а в декого, навпаки, знижується. Це особливо позначається в глибині Землі, де діють тиску в мільйони разів більші, ніж на її поверхні. Тому в надрах Землі кристали плавляться при інших температурах, ніж в лабораторіях. Але й там кристали починають плавитися обов'язково при певній температурі, тільки температура ця особлива для кожної області тиску.
На температуру плавлення впливають, крім тиску ще й інші причини, наприклад домішки інших речовин в розплаві. Так, температури плавлення чистого заліза і чистого кремнію дуже високі, а суміш оксидів цих елементів з вапном плавиться при набагато нижчій температурі. На цьому заснований спосіб виплавки заліза з руд, що містять кремнезем. У рудну суміш додають вапняк, кремнезем, вапно і невелика частка заліза легкоплавкий шлак, який спливає і виділяється від більш тугоплавкого чистого заліза.
1.3 Як кристали ростуть з розчинів
Візьміть склянку гарячої води і всипте в нього синій порошок мідного купоросу. Цей досвід можна виконати з будь-яким іншим кристалічним розством, розчинним у воді гіпосульфітом, содою, борною кислотою, галуном, англійською сіллю. Якщо ви дістанете не порошок, а крупні кристали, то спочатку потовчіть їх в порошок. У склянку гарячої води всипте стільки порошку, скільки зможе розчинитися. Помішуйте воду, так порошок буде розчинятися швидше. Коли порошок зовсім перестане розчинятися і почне осідати на дно, злийте утворився розчин в іншій стакан так, щоб на дно склянки з розчином не потрапило жодної крупинки порошку. Для цього профільтрувати розчин через фільтрувальний папір або через чисту ганчірочку. В отриманому розчині кількість речовини як раз відповідає його розчинності при даній температурі. Розчин "наситився" і більше він не може поглинути ні крупинки речовини. Такий розчин називається насиченим. Тепер залиште склянку з розчином і дайте йому охолонути. При охолодженні розчинність майже всіх речовин зменшується. Поки розчин був гарячим, у склянці води було розчинено, скажімо, 12 ложок речовини, тоді як при вже не може зберігатися пересиченим. Почнеться зростання кристалів, який буде йти до тих пір, поки все зайве речовина не випаде у вигляді кристалів і розчин знову не стане насиченим. У природних умовах, у кімнатній температурі в ньому могло б розчинитися лише 10 ложок Цієї речовини. Таким чином, тепер в розчині виявилася зайва речовина. Інакше кажучи, при високій температурі розчин був насиченим, а охолонувши, він став пересиченим. Такий пересичений розчин не може довго існувати, тому зайве речовина виділяється з розчину і осідає на дно склянки. Розгляньте в лупу, і ви побачите, що цей осад складається з кристалів. Розчинена речовина кристалізується з пересичених розчинів тому, що його виявляється в розчині занадто багато - більше, ніж розчин може утримати в собі. Якщо у вас вдома є тільки велика сіль, ви можете перекристалізовувати її в дрібну столову сіль. Розчиніть сіль у воді, профільтруйте розчин через фільтрувальний папір або чисту ганчірку і випарте цей розчин на повільному вогні. З розчину осядуть дуже дрібні кристалики. Явище пересичення розчинів відкрив в 1803 р. член Російської Академії наук Товій Єгорович Ловіц (1757-1804). Ловіц вказав, що якщо розчин охолоджується в чистій закритій посудині і якщо при цьому немає тряски, поштовхів, то розчин може деякий час, залишатися пересиченим, не кристалізуючись. Але лише тільки в рідині виникає хоча б мікроскопічно маленький кристалик, розчин відкритих водоймах, пересичений розчин не може зберігатися без кристалізації.
1.4 Як кристали ростуть з розплавів
Якщо нагріти кристал до температури плавлення, то він почне плавитися. Охолодити до температури плавлення, рідкий розплав почне кристалізуватися. Нагрійте чистий лід при атмосферному тиску до 0° С - він розтане, тобто розплавиться і перетвориться у воду. Навпаки, охолодіть чисту воду до 0° С - вона замерзне, перетвориться на кристали льоду. При нагріванні до нуля градусів розсипається лад часток, руйнується кристалічна структура льоду. А при охолодженні до нуля градусів безпосередньо частинки починають збиратися правильним строєм: серед хаосу виникають зародки кристалічної структури. Значить, температура плавлення кристалів даної речовини є в той же час і температурою кристалізації його розплаву.
У масі застигаючого розплаву утворюється відразу багато кристалічних зародків. Всі вони одночасно виростають в маленькі кристали. Поки ці кристалики зовсім малі, вони ростуть вільно, кожен - правильним багатогранником. Але, збільшуючись, кристали зустрічаються і починають заважати один одному. Як тільки два зростаючих кристала зустрінуться один з одним, зростання обох кристалів в цьому місці припиняється, адже жоден з них не може відсунутися. З інших же сторін - там, де кристали ще не зіткнулися з сусідами - вони продовжують рости. Так виходить, що кристал виростає в одну сторону більше, ніж в іншу: утворюються не правильні багатогранники. Або ж, врешті-решт, після запеклої "боротьби" виживають окремі кристалики.
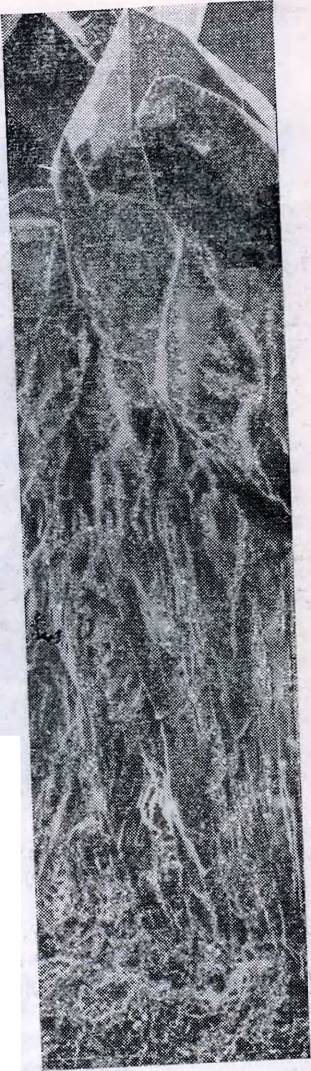
Назва самої розповсюдженою, всім відомої гірської породи, граніту, проходить від латинського слова "Гранум", тобто "Зерно". У граніті легко розрізнити простим оком зерна димчастого або безбарвного кварцу, рожевого, сірого, бузкового польового шпату, блискучі лусочки слюди.
Так само застигає розплавлений метал. Заводський метал теж є полікристал, тобто складається з багатьох монокристалічних зерен. Серед цих зерен не зерен металу зазвичай абсолютно неправильні. Зустрічається правильних, симетричних багатогранників форми всіх кристалічних Характерною властивістю кристалів є їх багатогранна форма, тому, що якби це ж саме кристалічне зерно росло не в тісноті, а так, щоб йому ніщо не заважало, то воно неодмінно набуло б форму правильного багатогранника. Крива, не багатогранна форма - це не звичайна, а вимушена форма кристала, йому довелося прийняти її тому, що не було ні місця, ні матеріалу для утворення цієї вільно форми, властивої всім кристалам, зростаючим без перешкоди. Дайте цьому кристалу рости вільної перед вами знову виникне правильний симетричний багатогранник.
1.5 Не тільки багатогранники
У природі кристали неправильної форми зустрічаються частіше,
ніж правильні багатогранники. У руслах річок через тертя кристалів про пісок і
камені кути кристалів стираються, багатогранні кристали перетворюються на
заокруглені камінчики - гальку. Від дії води, вітру, морозів кристали
розтріскуються, розсипаються в гірських породах кристалічні зерна заважають
один одному рости і набувають неправильні форми різні розчини і розплави
розчиняють, роз'їдають кристали, у результаті чого утворюються окатанниє,
"обсмоктавні", "поїдені" кристали. І все-таки властивості
всіх цих виродків і властивості чудових красенів багатогранників
однакові.
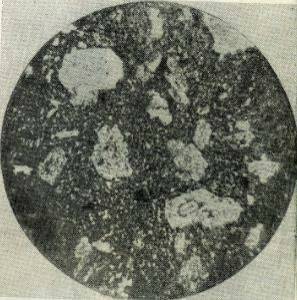

Рис. 1.4 Великі кристалічні зерна в мілко
кристалічній гірській породі. Збільшено в 60 разів.
Розділ 2. Вирощування кристалів
2.1 Вирощування монокристалів з розплавів
Кристалізація відбувається при охолодженні нижче точки
насичення. Основними достоїнствами методу є те, що кристалізацію можна
проводити значно нижче температури плавлення одержуваного матеріалу. Недоліки:
забруднення елементами флюсу, необхідність у дуже точному регулюванні
температури, використання дорогих платинових і ін матеріалів тиглів.
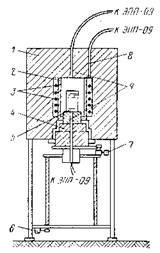
Рис. 2.5. Принципова схема установки для вирощування кристалів з розплаву в розчині
- кристалізаційна піч,
- Циліндричний карборундовий екран,
- нагрівальні світові стрижні,
- під печі,
- тигель,
- пристрій для вертикального переміщення,
- пристрій для реверсивного обертання,
- термопередатчик,
- контрольні термопари.
До флюсів пред'являються такі вимоги: вони не повинні бути летючими та токсичними, по можливості мінімально входити до складу монокристалів (якщо не є їх компонентами), повинна бути помірна в'язкість розплавів.
Наприклад, для вирощування кристалів феррограната (ЖИГ) беруть шихту, що містить в мольна. %: 10 Y2O3, 20,4 Fe2O3, 36,8 PbO 27,1 PbF2, 5,5 B2O3. Склад кристалізується цільового продукту Y3Fe5O12 не відповідає за співвідношенням концентрації основних компонентів складу розплаву, як і у випадку кристалізації феритових кристалів з розчину, який був розглянутий нами вище. Процеси росту монокристалів при реалізації їх технології підкоряються, власне кажучи, тим же основним термодинамічним і кінетичним закономірностям, що і синтез порошкових і плівкових матеріалів. Так найважливішим фактором є високотемпературна фазова діаграма компонентів шихти в області ліквідусу і солідусу. Зростання кристалів протікає через виникнення зародків, які можуть в залежності від температури і хімічних потенціалів компонентів розчинятися або рости далі, тобто можуть мати критичними розмірами і т.д.
За цим варіантом температура витримки розплаву 1250-1300оС (15 годин), швидкість охолодження після цього до кристалізації 0,3-0,5 град / год. Кристалізацію припиняють при 950-1000оС і видаляють залишився розплав, отримані кристали очищають кип'ятінням в азотній кислоті. Швидкість обертання тигля при вирощуванні 20 об / хв, обертання здійснюють 15 с в один бік і 15 с в іншу з 5-секундною паузою.
2.2 Метод Вернейля
Метод Вернейля реалізується шляхом просипкі маленьких порцій
порошкової шихти в трубчасту піч, та розплавляється підчас падіння в
киснево-водневому полум'я і живить краплю розплаву на поверхні затравки. Запал
при цьому витягується поступово вниз, а крапля перебуває на одному і тому ж
рівні по висоті печі. Переваги цього методу: відсутність флюсів і дорогих
матеріалів тиглів; відсутність необхідності точного контролю температури;
можливість контролю за зростанням монокристала. Недоліки: через високу
температуру росту кристали мають внутрішні напруги; стехіометрії складу може
порушуватися внаслідок відновлення компонентів воднем і випаровування летючих
речовин. Швидкість вирощування - кілька мм / год.
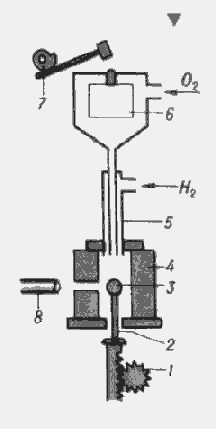
- механізм опускання кристала,
- кристалотримач,
- зростаючий кристал
- муфель, 5 - пальник, 6 - бункер,
- механізм струшування,
- Катетометри.
Рис.2.6. Схема установки для вирощування монокристалів по
методу Вернейля
2.3 Метод Бріджмена
Метод Бріджмена - зароджуються в нижній частині тигля з
розплавом монокристали служать затравкою. Тигель опускається в більш холодну
зону печі. Нижня частина тигля - конічна. Швидкість вирощування - також кілька
мм / год.
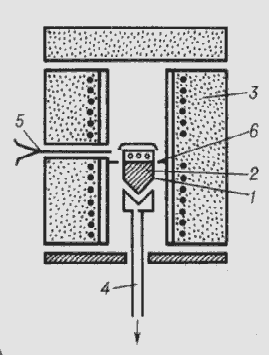
- тигель з розплавом,
- кристал,
- піч,
- холодильник,
- термопара,
- тепловий екран.
Рис. 2.7. Схема установки для вирощування монокристалівза
методом Стокаберга-Бріджмена
2.4 Метод Чохральського
За методом Чохральського виробляють витягування вгору на
затравку монокристала з ванни з розплавом. Нагрівання зазвичай здійснюють за
допомогою НВЧ випромінювання. Для зняття виникаючих напруг використовують
додаткову піч, через яку проходить вирощуваний кристал і відпалювати.
- тигель з розплавом,
- кристал,
- піч,
- холодильник,
,6 - механізм витягування.
Рис. 2.8 Схема установки для вирощування монокристалів за
методом Чохральського.
2.5 Метод зонної плавки
Зонна плавка полягає в прогоні зони розплаву по довжині
заготовки монокристала, одночасно в зоні розплаву концентруються домішки і
відбувається очищення кристала, кінцеву частину якого потім видаляють.
Нагрівання здійснюється індукційним, радіаційно-оптичних чи іншим методом.
Швидкість вирощування за методами 4 і 5 близька до такої для 2 і 3 методів. При
реалізації трьох останніх способів необхідно регулювання газового середовища
вирощування.
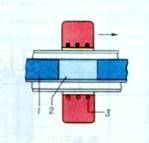
- тверда фаза,
- розплав,
- нагрівач, (стрілкою показаний напрям руху нагрівача)
Рис. 2.9. Схема пристрою для зонної плавки:
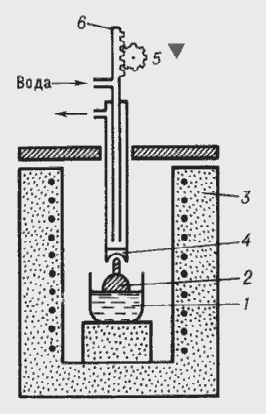
2.6 Гідротермальне вирощування
Вихідні оксиди або готовий складний оксид розчиняють у водних
розчинах кислот або лугів для реалізації гідротермального методу. Вирощування
проводять в автоклавах із захисними корозійностійкими вкладишами, наприклад,
для феритів при 375-725оС і тиску 1800-2000 атм. Через різницю температур у
верхній і нижній зонах автоклава вгорі виділяється кристал. Швидкість
вирощування - від часток мм до декількох мм на добу. Вирощувані монокристали
зазвичай мають високу якість і характерну кристалографічну огранювання, тобто
ростуть в умовах більш-менш близьких до рівноважних.
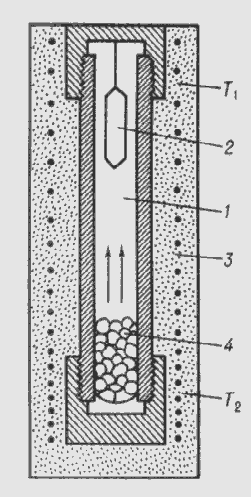
Рис. 2.10. Схема автоклава для гідротермального синтезу
- розчин,
- криcтал,
- піч,
(T1<T2).
2.7 Метод твердофазної рекристалізації
Для вирощування кристалів шляхом твердофазної рекристалізації
призводять до зіткнення керамічну заготівлю та монокристалічний затравки, між
ними іноді поміщають речовина, що ініціює процес рекристалізації, зокрема, при
отриманні феритових кристалів - оксид заліза (тонкий шар). Якщо швидкість
рекристалізації перевищує швидкість виходу пір на поверхню, що отримується
кристал може бути досить пористим. Після отримання монокристалів їх точно
орієнтують в просторі і піддають механічній обробці: різанню, шліфуванню,
поліровці. Наприклад, монокристали ІЧ-оптики типу ВРХ (галогеніди талію)
обробляють через їх невеликий твердості на токарних верстатах в спеціальних
захисних боксах. На монокристали наносять захисні покриття і при необхідності
шари матеріалів різного функціонального призначення.
Висновки
В даній роботі була розказана мала доля того, що відомо про кристали в наш час, але і ця інформація показала наскільки неординарні і загадкові кристали по своїй сутності.
В ході даної роботи я спостерігала якими методами можна вирощувати кристали.
В даний час відомі штучні способи вирощування кристалів. Їх навіть можна вирощувати у звичайному стакані. Для цього потрібний лиш спеціальний розчин та акуратність з якою потрібно слідкувати за кристалом, що росте.
У небі, надрах Землі, на вершинах гір, у піщаних пустелях, в морях та океанах, у наукових лабораторіях, у клітинах живих і мертвих організмах - усюди ми зустрінемо кристали. Ми також знаємо,що і на інших планетах і на далеких зірках весь час неперервно виникають, ростуть і руйнуються кристали. Метеорити також складаються з кристалів, навіть інколи в їхній склад входять такі кристалічні речовини, які на Землі ще не зустрічалися кристали повсюди.
Люди звикли використовувати кристали, робити з них прикраси, любуватися ними. Кристали за їх міцності використовують в різноманітних ріжучих апаратах. Людина використовує кристали майже у всіх областях мінеральної сфери, їхня вартість і значення надзвичайно великі.
Тепер, коли вивченні методи штучного вирощування кристалів,
їхня область застосування розширилась, і, можливо, майбутнє нових технологій
належить кристалам і кристалічним агрегатам.
Перелік посилань
1. Шаскольская М.П. - Кристаллография. М.: Высшая школа, 2006. - 400 с.
. Сиротин Ю.И., Шаскольская М.П. - Основы кристаллофизики М.: Наука, 2009. - 635 с.
. Гончаренко С.У. - Фізика. К.: Освіта, 2012. - 319 с.
. Шаскольская М.П. - Кристаллы. М.: Наука, 2008. - 208 с.
. Трофимова Е.И. - Курс физики. М.: Академия, 2010. - 560 с.
. Блудов М.І. - Бесіди з фізики. К.: Радянська школа, 2009. - 351 с.