Материал: Методи вирощування кристалів
Методи вирощування кристалів
МЕТОДИ ВИРОЩУВАННЯ КРИСТАЛІВ
Курсова робота
Зміст
Вступ
Розділ 1. Основні відомості про кристали
1.1 Структура кристалів
1.1.1 Сполучення елементів симетрії структур. Грати Браве
1.1.2 Кристалографічні категорії, системи та сингонії
1.2 Як утворюються розплави
1.3 Як кристали ростуть з розчинів
1.4 Як кристали ростуть з розплавів
1.5 Не тільки багатогранники
Розділ 2. Вирощування кристалів
2.1 Вирощування монокристалів з розплавів
2.2 Метод Вернейля
2.3 Метод Бріджмена
2.4 Метод Чохральського
2.5 Метод зонної плавки
2.6 Гідротермальне вирощування
2.7 Метод твердофазної рекристалізації
Висновки
Перелік посилань
Вступ
Повсюди нас оточують кристали. Ми ходимо по кристалах, будуємо із кристалів, обробляємо кристали на заводах, створюємо прилади й вироби із кристалів; проникаємо в таємниці будови кристалів. Ми дуже багато говоримо про кристали, але що ж це таке? Кристали - це речовини, в яких складові їх частки (атоми, іони, молекули) розташовані строго періодично, утворюючи геометрично закономірну кристалічну структуру. Але кожну кристалічну речовину можна відрізнити від інших кристалічних речовин за атомною структурою.
За розмірами кристали бувають різними. Багато з них можна побачити тільки в мікроскоп, а буває,що зустрічаються гігантські кристали масою в кілька тонн.
Кристалічну структуру ми можемо зустрічати повсюди. Люди навіть не задумуються про це.
Учені все глибше проникають у таємниці будови кристалів і знаходять їм нові застосування. Особи, що присвячують своє життя вивченню кристалів, часто сприймають їх живими. Мається на увазі, що вони говорять про них, як про живі істоти. Металознавці говорять про утому металевого кристала, про його старіння, здатність відпочивати, видавати звуки. Геологи говорять про пам´ять мінералу, про його здатність розумно пристосовуватись до зовнішніх умов. Учені не помиляються з приводу вміння кристалу розповідати свою біографію або виявляти емоції, але атмосфера особистого відношення із природою надає пошуку необхідне для них романтичне фарбування.
Правильна многогранна форма - перше, що впадає в око спостерігача, але не вона є головною особливістю кристалічного тіла. Кристал можна розбити на дрібні частинки, так що не залишиться й сліду від його краси, і все ж таки кожний кусочок буде, як і раніше, кристалом.
вирощування кристал монокристал гідротермальний
Найголовніше в кристалі не зовнішня його форма, а своєрідність його внутрішніх властивостей. Але спочатку звернемо увагу на правильність форми кристала - на симетрію. За висловом кристалографа Є.С. Федорова, " Кристали виблискують симетрією"
Залежно від геометричної симетрії, форми росту і від симетрії фізичних властивостей кристали поділяються на категорії, системи та сингонії. Кристали мають також фізичні властивості: електропровідність, теплопровідність, діелектричну проникливість та інші.
Для всіх кристалів однокової речовини, при постійних умовах температура плавлення однакова, а для різних речовин вона різна. Всі кристали під час плавлення зберігають постійну температуру. Саме на ці властивості кристалів заснований пристрій термометра. Нуль градусів за шкалою термометра - це температура, при якій в звичайних умовах тануть, тобто плавляться, кристали льоду. Температура плавлення кристала залежить від тиску, під яким цей кристал перебуває.
Робота складається із вступу, з двох розділів, висновку та
переліку посилань. Перший розділ називається: основні відомості про кристали,
він складається з таких підпунктів: структура кристалів, сполучення елементів
симетрії структур. Грати Браве, кристалографічні категорії, системи та
сингонії, як утворюються розплави, як кристали ростуть з розчинів, як кристали
ростуть з розплавів, не тільки багатогранники. Другий розділ називається:
вирощування кристалів, він складається з таких підпунктів: вирощування
монокристалів розплавів, метод Вернейля, метод Бріджмена, метод Чохральського,
метод зонної плавки, гідротермальне вирощування, метод твердофазної
рекристалізації. До роботи також водять висновки та перелік посилань.
Розділ 1. Основні відомості про кристали
1.1 Структура кристалів
В усьому світі ми не знайдемо жодного атома або молекули,що знаходилися б у спокої: всі вони рухаються, але ці рухи зовсім різноманітні.
Ось наприклад якщо взяти кристали, то форма їх абсолютно правильна. Їх атоми, молекули, іони також не знаходяться у спокої, але частинки не взаємодіють одна з одною, тому всі вони розташуванні правильним порядком і кожна може коливатися біля певного положення.
Якби ми розглянули б кристал ззовні, то помітили, що
тягнуться безкінечні рівні ряди частинок. (див. рис. 1.1).
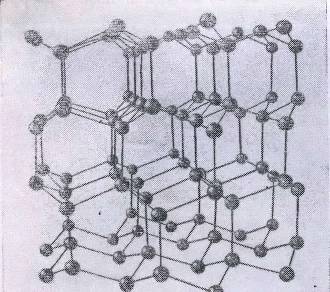
Рис. 1.1 Модель атомної решітки кристалу діаманта.
Ці правильні ряди частинок в просторі, трьохмірні решітки з атомів утворюють кристалічну структуру. Також ми помітили б, що структура всіх кристалічних речовин періодична і закономірна. У всіх кристалів частини порядкуються симетричними правильними рядками, плоскими сітками, трьохмірними решітками.
У твердій кристалічній речовині кожна частинка рухається "вільно", коливається, але тільки на своєму місті у рядку. Вийти зі свого положення частинки твердого тіла можуть, тільки тоді, коли наприклад кристал нагріти, щоб він почав плавитися.
Характеристики твердого тіла: порядок, закономірність, періодичність, симетрія роз положення атомів.
У всіх кристалах, твердих речовинах частинки розположенні правильним, чітким порядком, побудовані симетричними, правильними, узорами, які повторюються. Доки є цей порядок існує тверде тіло, кристал. Порушено порядок, розсипався лад часток це означає, що кристал розплавився, перетворившись в рідину, або випарувався, перейшовши в пар.
Порядок, лад атомів в різних тілах, різні строї атомів заліза зовсім не схожий на будівництво кристала льоду. У кожному речовині є саме свій, характерний візерунок і порядок розташування атомів. І від того, який цей порядок, залежать властивості речовини. Одні і ті ж атоми, частинки одного сорту, розташовуючись по-різному, утворюють речовини із зовсім різними властивостями. Подивимося, наприклад, на атоми вуглецю.
Сажа, або кіптява - м'який чорний порошок, на дні каструлі або в комині, що викидається чорними клубами диму з труб, - це вуглець.
Графіт, м'який стерженек олівця, залишаючий слід на папері. У техніці графіт служить не тільки для олівців: цей матеріал витримує дуже високі температури, і тому з нього роблять вогнетривкий посуд. Графіт - кристал, складений з атомів вуглецю.
Є й інша форма кристалів вуглецю - алмаз. Алмаз дуже твердий, він твердіше всіх каменів на Землі. Алмазом можна різати, шліфувати, свердлити будь-які тверді камені і метали. Важко повірити, що алмаз і графіт складені з одних і тих самих атомів вуглецю. Графіт м'який, непрозорий, чорний. Алмаз - твердий, прозорий, іскристий всіма кольорами веселки. Графіт-вогнетривкий, алмаз легко горить. У полум'ї кисню коштовний діамант згорає повністю, залишається лише купка сажі або графіт. Алмаз, графіт і сажа складаються з одних і тих самих атомів вуглецю, а різниця лише в тому, який порядок розташування цих атомів. Розставлені вони одним строєм - і виникає м'який чорний графіт. Перебудуються по - іншому і вийде твердий прозорий алмаз. Структура кристала визначає властивості речовини і його форму. А правильна багатогранна форма - це наслідок атомної структури. Плоскі грані кристала відповідають плоским сіткам кристалічної решітки, гострі прямі ребра - рядам атомів в решітці.
Кожна кристалічна речовина відрізняється від інших кристалічних речовин за своєю атомною структурою. У різних речовинах різні відстані між частинками в решітці. Але всі ці відстані дуже малі, це - стомільйонний ні частки сантиметра (ангстрема). У всіх кристалічних речовинах атоми, іони, молекули утворюють симетричні ряди, сітки і грати. Правильно повторюється симетричне розташування частинок обов'язково для кристалів та є їхньою характерною особливістю, відрізняючою їх від некристалів. Кристали - це речовини, в яких складові їх частки (атоми, іони, молекули) розташовані строго періодично, утворюючи геометрично закономірну кристалічну структуру.
Кристалічна структура виявлена не тільки в природних многогранниках каменів, в кристалічних гірських породах і в металах, але і в багатьох інших тілах, про яких нікому і в голову не приходило подумати, що вони теж складаються з червоних металів. Глина не схожа на кристали, але й вона складається з найдрібніших кристалічних частинок. Навіть у таких речовинах, як звичайна сажа, людські кістки, волосся, волокна вовни, шовк, целюлоза і т.п., виявлено кристалічну будову.
1.1.1 Сполучення елементів симетрії структур. Грати Браве
Основне симетрична перетворення кристалічних структур - це
нескінченне повторення. Жодна точка не залишається на місці, всі вони
нескінченно повторюються з допомогою трансляцій. Кристалічна структура
складається з частинок або груп частинок, пов'язаних один з одним різними
перетвореннями симетрії. Поєднання трансляцій з кожним з елементів симетрії
генерує нові елементи симетрії, що нескінченно повторюються в просторі. Для
кожної структури характерний її набір елементарних трансляцій або трансляційна
група, яка визначає просторову решітку. Залежно від ставлення величин та взаємної
орієнтації трьох основних трансляцій відрізняються одна від одної по своїй
симетрії. Симетрія обмежує число можливих решіток. Всі кристалічні структури
описуються 14 трансляційними групами, відповідає 14 гратам Браве. Гратами
Браве називається нескінченна систематочок, яка утворюється
трансляційний повторенням однієї точки. 14 решіток Браве відрізняються один від
одного за формою елементарних комірок і по симетрії і поділяються на 6
сингоній. Підрозділ на сингоній було введено ще на початку XIX століття тільки
на підставі вивчення зовнішньої форми мінералів вирішуючи задачу про
симетричному розташуванні сферичних частинок (матеріальних точок) в просторі,
Браве в 1848 р. прийшов до такого ж поділу на сингоній. Симетрія кристалічного
простору обмежує число можливих решіток. Решітка повинна бути інваріантною
відношенню до всіх перетворень симетрії, можливим для даного кристалічного
простору.
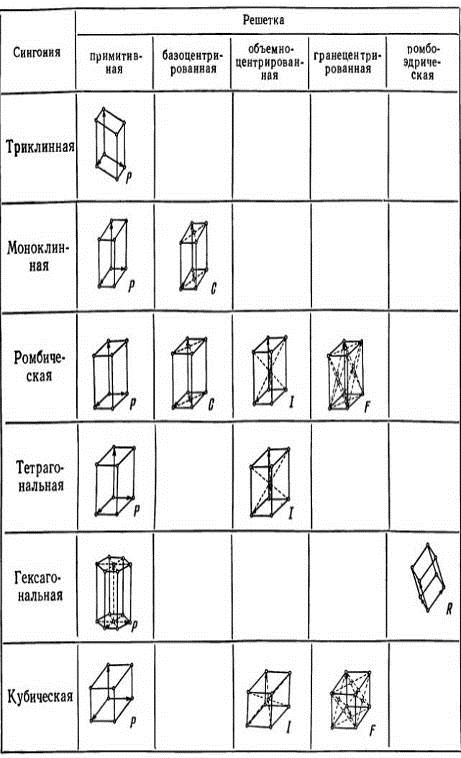
Рис. 1.2 Чотирнадцять решіток Браве
1.1.2 Кристалографічні категорії, системи та сингонії
Залежно від геометричної симетрії, форми росту і від симетрії фізичних властивостей кристали поділяються на категорії, системи та сингонії. Залежно від числа особливих (одиничних) напрямів і від наявних осей симетрії кристали поділяються на три категорії:
вища категорія - немає особливих напрямів, є кілька осей симетрії порядку вище ніж 2 (приклад - куб);
середня категорія - особливий напрям, збігається з єдиною віссю симетрії порядку 3, 4 або 6, тобто вище ніж 2 (наприклад - три-, чотири-і шестигранна призма);
нижча категорія - кілька особливих напрямків, немає осей порядку вище ніж 2 (приклад - так звана ромбічна призма (цеглинка), що має три осі 2).
До вищої категорії відносяться кристали, у яких є кілька осей симетрії порядку вище ніж 2; зокрема, обов'язково є чотири осі 3 і, крім того, можуть бути по три осі и. Це високосиметричні кристали. У них немає особливих напрямів. Будь-якому напрямку в кристалі вищої категорії відповідають інші симетрично еквівалентні напряму. Властивості кристала в симетрично еквівалентних напрямках повинні бути однаковими, тому анізотропія властивостей у кристалів вищої категорії виражена найменш різко. Фізичні властивості кристалів, описувані тензором другого рангу, тобто електропровідність, теплопровідність, діелектрична проникність та інші, в цих кристалах ізотропні, ізометричні.
До середньої категорії відносяться кристали, у яких є одне особливий напрямок, а саме, одна вісь симетрії 3, 4 або 6 (проста або інверсійна). Анізотропія фізичних властивостей у цих кристалів виражена значно різкіше, ніж у кристалів вищої категорії.
До нижчої категорії відносяться кристали, у яких немає осей симетрії порядку вище ніж 2 і є кілька особливих напрямів. Це найменш симетричні кристали з найбільшою анізотропією властивостей.
У свою чергу, три категорії поділяються на сім систем за ознакою їх характерною симетрії і по сполученням осей симетрії нижча категорія ділиться на три системи:
тріклінную ("тричі похила") система - немає ні осей, ні площин симетрії; моноклінна ("однонаклонная") - є лише одна вісь симетрії другого порядку, або одна площина симетрії, або і вісь, і площина;
ромбічна - у кристала є більше однієї осі другого порядку або більше однієї площини симетрії.
Середня категорія поділяється також на три системи:
трігональная - одна основна вісь симетрії 3 або 3;
тетрагональная - " " " " 4 або 3;
гексагональна - " " " " 6 або 6.
Вища категорія складається з єдиної системи -
кубічної, яка характеризується наявністю чотирьох осей симетрії третього порядку.
Замість підрозділів на сім систем можна поділяти категорії на шість сингоній. Поняття сингоній збігається з поняттям системи для всіх систем, крім тригональної і гексагональної. Поділ на сингоній визначає вибір кристалографічної системи координат і характеризує її трійки базисних векторів а'а2, a3 i або, інакше кажучи, метрики a, ft, с, а, р, у.
Кристалографічні осі координат завжди вибираються за осях
симетрії або по нормалі до площин симетрії. Якщо немає відповідних елементів
симетрії, як у моноклінної і триклинной сингоніях, осі координат вибираються по
ребрах кристалографічного багатогранника або по рядах кристалічної решітки.
Примітивні елементарні комірки, що відповідають кожній сингоній, показані в
першому стовпці табл. 9.1 і в табл. 1.3.

Рис. 1.3 Розділ кристалів на категорії сингонії та системи
Застигання магми - це процес росту кристалів з розплавів. При нагріванні тверді речовини розплавляються. Але виявляється, що кристали і аморфні речовини (скло) плавляться зовсім по-різному. Кожне кристалічна речовина починає плавитися при зовсім різній температурі. Нагріємо, наприклад, кристал олова і будемо при цьому вимірювати температуру: 100, 200, 225° С - кристал не змінюється. Раптом при 231,9° С кристал відразу починає плавитися. Скільки б разів ми не повторювали цей дослід, нам не вдасться розплавити кристал олова при 231° С або більш низькій температурі і навпаки, нам не вдасться зберегти його при 232° С або більш високій температурі: він обов'язково почне плавитися при 231, 9° С, якщо тільки дослід робити при атмосферному тиску, якщо в олові немає домішок і якщо немає явища переохолодження. Будемо продовжувати нагрівати плавлячий кристал олова. Незважаючи на нагрівання, температура олова більше не підвищується: у весь час плавлення вона залишається рівною 231,9° С. І тільки коли плавлення закінчиться, температура олова - тепер вже не кристала, а рідкого розплаву - почне збільшуватися - якщо, звичайно, продовжувати нагрівання.