Материал: Методи спектрофотометрії
3. Методика спектрофотометричних вимірювань
Існує два типи спектрофотометрів: однопроменеві
і двопроменеві. У однопроменевий приладі промінь світла, що виходить з
монохроматора, проходить через одну кювету і потім потрапляє в детектор.
Визначення поглинання роблять у такий спосіб. Спочатку прилад встановлюють на
нуль проникання(нескінченна величина поглинання) з детектором в темряві, що
робиться для компенсації слабкого струму, який є навіть за відсутності
випромінювання і виникає внаслідок емісії теплових електронів. Потім в промінь
поміщають кювету, що містить розчинник, і прилад встановлюється для вимірювання
в одиницях проникнення (нуль поглинання) при певній довжині хвилі. Після чого,
кювету з розчинником замінюють кюветою з розчином досліджуваної речовини і
виробляють вимір.За цією методикою вимірюють два фотоструми - один пропорційний
інтенсивності променя, що пройшов через розчинник, і другий - пропорційний
інтенсивності променя, що пройшов через розчин речовини. Щоб співвідношення цих
струмів були еквівалентні проникності, треба джерело випромінювання і детектор
залишати постійними в межах, коли проникність встановлена на одиницю і коли
проникність зменшується при вимірюванні поглинання речовини. Отже, особливу
увагу необхідно звертати на постійну напругу, що подається на лампу.У
двохпроменевій спектрофотометрії ця проблема вирішена наступним чином.
Випромінювання, що виходить з монохроматора, розділяється на два промені, що
мають однакові інтенсивності і спектральні розподіли. Один з променів проходить
через кювету з розчинником, інший - через кювету з досліджуваним речовиною. На
відношення випромінювань, що виходять з обох кювет, величина джерела світла не
робить ніякого впливу. Ставлення випромінювань може бути виміряна двома
способами.Промені, що вийшли з кювет, спрямовуються на катоди двох
фотоемісійних ламп або фотопомножувач. Виходи цих детекторів пов'язані серією
опорів, посилюють різницю між двома фотоструму і реєструють величину
поглинання. Зручністю двопроменевих приладів є можливість реєстрації показань.У
приладах з одним детектором промені, що виходять з двох кювет, спрямовуються на
ту ж частина катода однієї лампи. За допомогою обертового непрозорого диска
промені розбиваються на окремі порції. Таким чином, на детектор падає
випромінювання, інтенсивність якого змінюється в межах I і I0, і його вихід
змінюється з тією ж швидкістю, що і швидкість обертання диска. Це створює
напругу, амплітуда якого буде пропорційна різниці в інтенсивності двох
променів. Подальше вимір напруги, відповідного інтенсивності променів, залежить
від конструкції приладу.Зазвичай для отримання спектрів потрібно від 0, 1 до
100 мг речовини в залежності від молярного коефіцієнта поглинання. Розчини, що
застосовуються в спектрофотометрії, є дуже розведеними, що обумовлює
необхідність точного зважування зразка і точного відмірювання розчину при наступних
розведеннях. Підходящої для вимірювань концентрацією є та, яка забезпечує
показання поглинання між 0, 2 і 0, 7, що відповідає проникнення від 65 до
20%.Певне підвищення точності спектрофотометричного аналізу досягається шляхом,
так званої диференціальної фотометрії. Цей метод заснований на порівнянні
поглинання невідомого розчину і поглинання стандартного розчину, останній
підібраний таким чином, що різниця в поглинаннях буде знаходитися в межах, в
яких вимір може бути виконано з достатньою точністю. Диференціальний спосіб
прийнятий Скандинавської фармакопеєю в якості основного методу для
спектрофотометричних визначень.Відповідно до одного з варіантів
диференціального методу, званого іноді ДЕ або Δε методом,
вимірювання проводиться шляхом порівняння. Невідомої речовини при певній
величині рН до тієї ж концентрації речовини, але при іншій, відмінній від
першої, величиною рН. Наприклад, для визначення фенолів розводять частина
розчину лужним, буфером, а іншу частину кислотним буфером. Вимірюють поглинання
лужного розчину, використовуючи для порівняння кислотний розчин. Розраховують
вміст фенолів, застосовуючи ДЕ значення, знайдене для чистої речовини в тій же
парі буферних розчинів.Таким чином визначається зміст гексахлорофен в рідкому
милі по Фармакопеї США XVII. Так як ряд речовин не показує змін до спектральних
характеристиках при зміні рН, диференційний метод для фенолів можна вважати
більш специфічним, ніж хімічний метод.
4.Фактори, що впливають на абсорбціонні
властивості хромофора
Спектр поглинання хромофора визначається в першу чергу хімічною структурою молекули. Однак λ макс. і E зазнають помітних змін і під впливом оточення . Мається на увазі вплив рН, полярності розчинника або сусідніх молекул і відносна орієнтація сусідніх хромофорів. Саме ці фактори лежать в основі використання абсорбційної спектроскопії для характеристики макромолекул.
Вплив оточення полягає в наступному:
.1 Ефект рН
рН розчину визначає іонну форму іонізуючих
хромофорів. На рис. 4-1 показаний приклад, зображений вплив рН на спектр
тирозину.
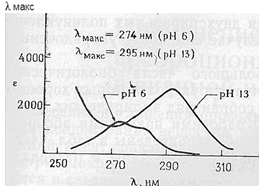
Рис.4-1.
Спектр поглинання тирозина при рН 6 і
13.Відмітим що, як λ Макс, так і Е збільшується при
дисоціації ОН-групи фенольного залишку
.2 Ефект
полярності
У разі полярних хромофорів часто справедливо
(особливо якщо молекула містить О, N або S), що λ макс
спостерігається при більш коротких довжинах хвиль у полярних розчинниках, що
містять гідроксил (Н2О, спиртах), ніж у неполярних.
Приклад наведено на рис. 4-2.
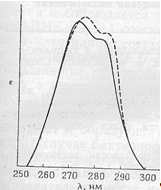
Рис 4-2.
Вплив полярності розчинника на спектр поглинання
тирозина .
.3 Ефекти
орієнтації
Величини λ макс. і Е істотно залежать від геометричних особливостей молекул. Найбільш відома гіпохромія нуклеїнових кислот, тобто зниження коефіцієнта погашеня нуклеотиду, за умови, що нуклеотид входить до складу одноланцюгового полінуклеотіду, в якому нуклеїнові основи зближені і розташовані один над одним . Подальше пониження Е спостерігається для двох спіральних полінуклеотидів, так як основи в цьому випадку ще більш впорядковані.
Це показано на рис. 4-3.В результаті досліджень
великої кількості біологічно важливих з’єднань і макромолекул, структура яких
добре
відома
для різних умов, зібраний ряд емпіричних фактів, які можуть бути названі
робочими правилами абсорбціонної спектроскопії в біохімії. Вони наведені в
табл. 1
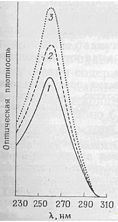
Рис 4-3.
Спектри поглинання ДНК фага Т7 в двоколірній(1) і одноколірній(2) формах, а також після гідролізу до вільних нуклеотидів (3), що показує пониження оптичної щільності .
ТАБЛИЦЯ 1. Емпіричні правила інтерпретації спектрів поглинання біологічних макромолекул
. Якщо амінокислоти; триптофан, тирозин, фенілаланін і гістидін - переміщуються в менш полярне оточення, λ макс І Е зростають.
а. Якщо в знятому в полярному розчиннику спектрі амінокислоти, знаходяться у складі білка, спостерігаються великі λ макс і Е, чим ті ж величини для вільної амінокислоти в тому ж розчиннику, то ця амінокислота знаходиться у внутрішній області білка ("схована ") і оточена неполярними амінокислотами.
б. Якщо спектр білка чутливий до зміни полярності розчинника, амінокислота, для якої спостерігаються зміни λ макс і Е, повинна розташовуватися на поверхні білка.
. У разі амінокислот λ макс і Е завжди зростають, коли титруєма група (наприклад, ОН тирозину і SH цистеїну) заряджена. Отже:
а. Якщо не спостерігається змін в спектрі однієї з цих амінокислот,
а рН таке, що мала б відбуватися іонізація вільної амінокислоти, то вона повинна бути захована в неполярній області молекули білка.
б. Якщо значення рК іонізуючої групи амінокислоти, визначене за зміни спектра при зміні рН, таке ж, як для вільної амінокислоти в розчині, то ця амінокислота знаходиться на поверхні білка.
в. Якщо значення рК, визначене за зміни спектра при зміні рН, істотно інше, то ця амінокислота, ймовірно, знаходиться в дуже полярному оточенні (наприклад, тирозин, оточений карбоксильними групами).
. Величина Е пуринів і піримідинів знижується у
міру того, як плоскості їх кілець стають паралельними і кільця зближуються один
з другим . Величина Е знижується в наступному ряді : вільна основа > основа
в складі одноланцюгового полінуклеотида, що не має сгекінга > основу в
складі одноланцюгового полінуклеотиду зі стекінгом > основа у складі
двохланцюгового полінуклеотида.
5. Застосування
абсорбційної спектроскопії у видимій і УФ-областях спектра
Вимірювання поглинання проводиться для багатьох
цілей: визначення концентрації речовини, аналізу деяких хімічних реакцій,
ідентифікації речовин та визначення структурних параметрів макромолекул. Всі ці
галузі застосування розглядаються в наступних прикладах.
.1 Приклад 1.
Вимірювання концентрації
Найбільш часто через вимірювання поглинання проводять для визначення концентрації .Це можна робити, якщо відомий молярний коефіцієнт погашення і дотримується закон Бера. Наприклад, для двохланцюгового ДНК D260 = 1 відповідає 50 мкг / мл (ця величина залежить від нуклеотидного складу) . Оскільки закон Бера дотримується принаймні до D = 2 (яка наближається до межі для більшості спектрофотометрів), легко підрахувати концентрацію, а саме: D, рівна 0, 5, відповідає 25 мкг / мл, D, равная 0, 1, відповідає 5 мкг / мл і т. д.
Іноді досліджуваний матеріал складається з частинок, поглинаючого світла і утворюють швидше суспензію, ніж розчин; наприклад: у разі бактеріофагів, поглинання майже цілком визначається вмістом у них ДНК.
Бактеріофаги не тільки поглинають, але також й розсіюють світло (релляївське розсіювання) і, отже, можуть мати штучно завищене поглинання.
Однак, вимірюючи поглинання при ряді довжин
хвиль, далеких
від
λ
макс,
можна зробити поправку на розсіювання. Так як розсіяння змінюється пропорційно λ
-4,
можна побудувати залежність вимірюваного поглинання від λ -4 і,
екстраполюючи лінійну частину цієї кривої (де все спостережуване поглинання обумовлене
розсіюванням) до λ
макс,
внести поправку в вимірюване поглинання, що дорівнює величині, обумовленої
розсіюванням. Приклад такої поправки зображений на рис. 5.
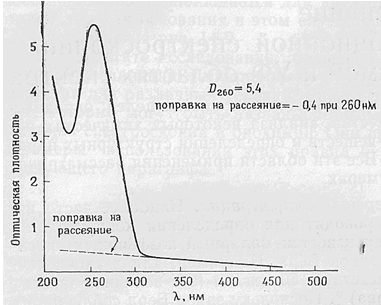
Рис. 5.
Це зручний метод визначення вмісту нуклеїнової кислоти в бактеріофага; враховується також те, що D260 (з поправкою на розсіювання) = 1 відповідає концентрації ДНК 50 мкг / мл.
Концентрацію бактерій також часто визначають
спектрофотометричним методом, хоча при використовуваних довжинах хвиль все поглинання
обумовлено розсіюванням. У цьому випадку замість поправки на розсіювання
проводиться співставлення спостережуваної оптичної щільності з кількістю
життєздатних клітин і будується калібрувальна крива.
Таким шляхом, як показано на рис. 5-1, вдається точно визначити концентрацію
клітин або сухої маси на одиницю об'єму.
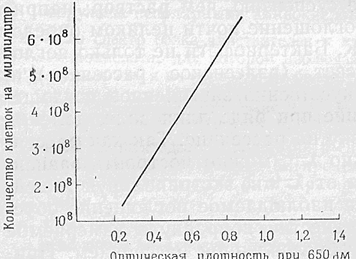
Рис .5-1.Концентрація бактерій, визначена шляхом
вимірювання оптичної щільності .
.2 Приклад 2.
Дослідження хімічних реакцій
В ході реакції має змінюватися поглинання одного
із реагентів. Розглянемо вимір активності ферменту-галактозидази. Ця методика
широко використовується в молекулярній біології при вивченні функціонування
лактозного оперону. Цей фермент розщеплює 0-нітрофенілгалактозид (ОНФГ) з
утворенням о-нітробензолу, який можна визначити за його поглинання при 420 нм.
Так як, в деякому інтервалі, швидкість реакції пропорційна концентрації
ферменту, з нахилу кривої залежності D від часу гідролізу (рис. 5-2) можна
визначити кількість ферменту.
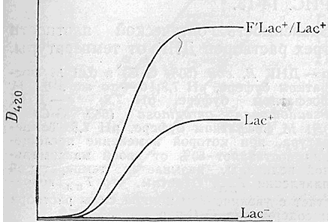
Рис. 5-2 .Час після додавання стимулятора.
Вивчення синтезу -галактозидази шляхом
вимірювання D420 продукту гідролізу о-нітрофенілгалактозида (ОНФГ). Три
культури : Lac-, Lac+ і диплоїд, містить дві копії генів lас, вирощувалися в
гліцерин-сольовому середовищі.При t = O був доданий стимулятор синтезу
-галактозидази. Через відмінні проміжки часу брали проби і обробляли толуолом
для того, щоб вбити клітини і відокремити фермент, потім був доданий ОНФГ.
Через тридцять хвилин була виміряна D420. У результаті цього досвіду показано,
що клітини Lac-не продукують фермент, а диплоїд продукує приблизно в два рази
більше, ніж гаплоїди.
5.3 Приклад 3.
Спектрофотометричне титрування білків
При багатьох дослідженнях структури білків
виникає необхідність визначення величини рК дисоціації протонів іонізуючих
бічних груп амінокислот, оскільки ці величини вказують на локалізаuію
амінокислоти у білку (правило 2 в табл. 14-2). Це часто можна зробити
спектрофотометрично, так як при дисоціації часто змінюється спектр одного з
хромофорів (наприклад, у випадку тирозину).Розглянемо гіпотетичний
тирозиновмістимий білок і для визначеня числа зовнішніх тирозинових залишків
скористаємося правилом 2 (табл. 14-2). Припустимо, що в цьому білку міститься
п'ять тирозинових залишків. Якщо всі вони розташовані на поверхні
і іонізуются при збільшенні рН, спектр, відповідаючим залишками тирозину, буде
наближатися до спектру вільного тирозину при високих значеннях рН, (правило 2
б). Іншими словами, залежність D295 (λ макс
для іонізованої форми) від рН буде виглядати, як крива
А на рис.5-3. Коли ж, навпаки, три тирозинових залишки розташовані всередині в
неполярному оточенні, отримана крива аналогічна кривій Б (правило 2а);
відношення величини першого плата до кінцевої величини, що дорівнює 2 / 5.
Зазначимо, що при дуже високих рН на кривій видно велике зростання D295. Це
вказує на те, що внутрішні тирозинові залишки стали доступні розчиннику, тобто
білок денатурувував.
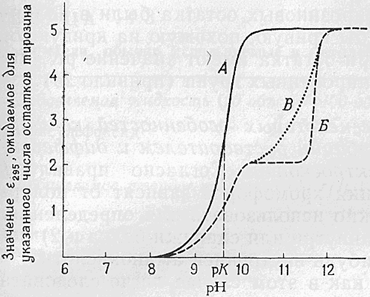
А-всі 5 залишків находяться на поверхні ; Б-2 залишки на поверхні, а 3 в середині, в неполярному оточенні ;В-3 внутрішніх залишки знаходяться в полярному оточенні і доступні розчиннику.Якби три внутрішніх тирозинових залишки були в полярному оточенні, то отримали б криву, схожу на криву В, яка вказує, що ці три залишки мають значення рК (правило 2в).
5.4 Приклад 4.
Асоціація білка
Зміна спектрів в процесі асоціації білка можуть
бути викликані тим, що хромофори розташовані на поверхності попали в площину
зєднання і стали недоступні розчиннику .По спектральним випромінюванням можна
контролювати наявність взаємозв’язку молекул білка і визначати умови, кінетику
цього процесу.
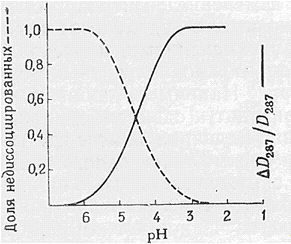
Рис .5-4.
Цей процес можна вивчати з допомогою
диференціальної спектроскопії; в цьому випадку для отримання диференціального
спектра використовують два розчини, які ідентичні у всьому, крім концентрації.
.5 Приклад 5. Пертурбація
розчинником нуклеїнових кислот
Заміна води на 50%-ну D2Oпризводить до
характерних змін в спектрах мононуклеотидів, та не впливає на спектри пар
оснований .Таким чином, зміни в спектрі НК в 50%-ній D2O можна використати для
оприділення долі основаній, які не беруть участі в утворенні пар .Це важливо
при вивченні таких молекул, як транспортна РНК (тРНК).В тРНК послідовність
основаній така що не всі вони утворюють вуглецеві зв’язки ; можна побудувати
просторові моделі, в яких реалізується частина вуглецевих зв’язків
(рис.5-5).Згідно різним моделям потрібно щоб різне число основаній було
зв’язане вуглецевими зв’язками ;спектральні дані дозволяють виключити деякі
можливі моделі .
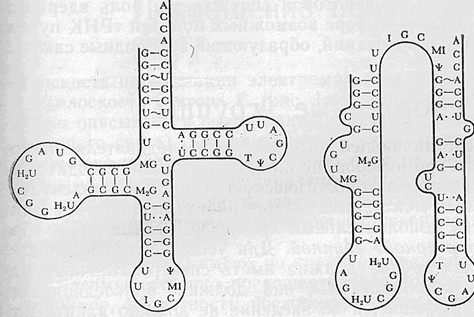
Рис.5-5.
Дві із декількох можливих структур алланінової
тРНК, збудованих таким чином, що більша частина основ бере участь в утворенні
вуглецевих зв’язків .Вуглецеві зв’язки пари G*C позначена суцільною лінією,
пари А*U - точками, більш слабшими ніж вуглецеві зв’язки, другі пари позначенні
хвилеподібною лінією .
6. Поглинання
поляризованого світла
Площина поляризації електромагнітної хвилі
визначається як площина вектора Е (мал. 14-1, див. також гл. 16, де більше
повно описується поляризація і виникнення плоскополяризованого світла).
Звичайний промінь світла не поляризований, тому що його можна представити як
набір хвиль з випадково орієнтованими площинами поляризації. Однак
плоскополяризоване світло можна отримати, або пропускаючи світло через різні речовини,
або шляхом відображення від поверхні під критичним кутом. Всі хромофори мають
принаймні одну вісь, вздовж якої переважно поглинається плоскополяризоване
світло. Наприклад, ймовірність поглинання світла гексаметилбензолом, являючи
собою симетричне плоске кільце максимальне, коли вектор Е знаходиться в площині
кільця, і дорівнює нулю, коли він перпендикулярний цій площині. Якщо в молекулі
є осі симетрії різної довжини, як у випадку плоскої молекули нафталіну, то
поглинання відбувається тільки тоді, коли вектор Е лежить в площині кільця. Цей
ефект називається дихроїзмом ; він визначає різні значення величини Е для
окремих напрямів. Його зручно використовувати, визначаючи орієнтацію молекул в
біологічних системах. При дослідженнях макромолекул він найбільш часто
використовується в інфрачервоній спектроскопії для визначення орієнтації
окремих зв'язків по відношенню до осі молекули.