Материал: метаболизм аминокислот
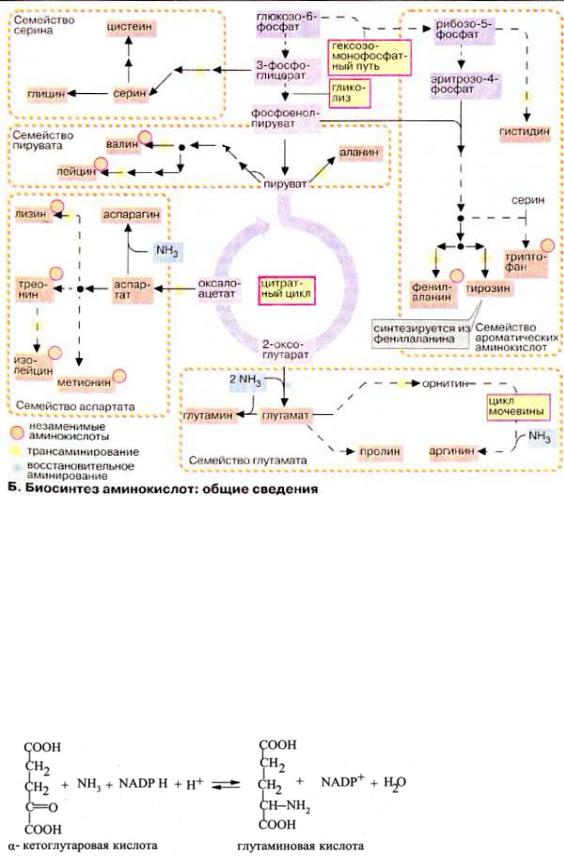
Пятьсоединений: 3вместе-фосфоглицератсдвумямоносахаридами, фосфоенолпируватпентозофосфатного,пируват, оксалоацетатпутислужат предшественникамиα-кетоглутарат всехаминокислотвбактерияхи растениях.
Пути биосинтезазаменимыхам нокислот |
|
|
|||
Фундаментальное значение длябиосинтезавсехаминокислотво всехорганизмах |
|||||
имеетреакцияобразования |
|
(глутамата)изаммиакаи α- |
|||
кетоглутаровойкислоты(α-кетоглутарата) поддействиемфермента |
|
||||
|
: |
|
глутаминовой кислоты |
|
|
|
|
|
|
|
глутамат- |
дегидрогеназы |
|
NH4++ α-кетоглутарат + NADPH→L-глутамат + NADP+ + H2O |
|||
(глутамат)
Биосинтетический путьглутамата,глутаминаи пролинаодинаковы увсех форм живыхорганизмов.
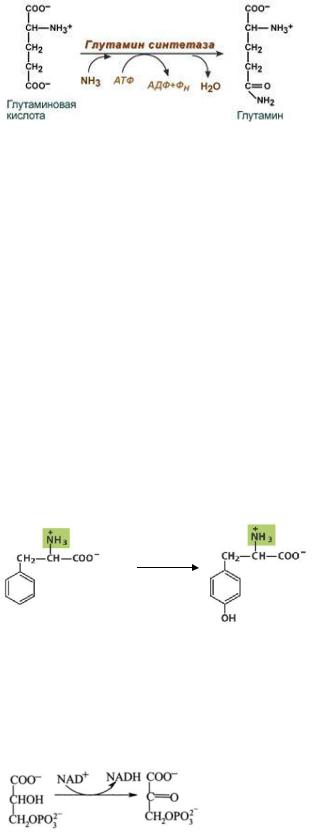
Глутамин образуется изглутаматавреакции,катализируемойглутаминсинтетазой
Глутамат +NH4++ АТФ→ глутамин+ АДФ + Р+Н+
Пролин |
|
|
|
|
|
|
|
|
Аргининобразуетсяизглутаматапосредствомегоциклизации, |
|
|||||||
|
синтезируетсяизглутаматавцикле мочевины. |
|
||||||
Трансаминирование α -кетокислотсиспользованиемглутаминовойкислотыв |
||||||||
качестве донорааминогруппы представляетсобойосновной путь введения α - |
||||||||
аминогруппы прибиосинтезе большинствадругихаминокислот. |
|
|||||||
Аланин |
|
пирувата |
|
|
оксалоацетата |
|
||
|
оваяк слота |
|
|
|
|
|||
Аспарагобразуетсяиз |
|
|
|
в реакциитрансаминирования, |
вреакции |
|||
трансаминирования |
|
|
(аспартат) образуется из |
|
||||
|
Аспараг |
н |
изаспарагиновойкислотыаспарагинсинтетазой |
|||||
Бактериисинтезируют |
|
|
|
|||||
который используют ионаммония для включениядобавочнойаминнойгруппы, (каквслучае глутамина). Увысших животных донором аммиакадлясинтеза аспарагина служитглутамин.
уживотных образуетсяизнезаменимойаминокислоты –фенилаланина путемТирозингидроксилированияфенильнойгруппы, ферментом фенилаланин-4-
монооксигеназа, который обеспечивает превращение фенилаланина в тирозин. Фермент имеется только в печени, почках, поджелудочной железе. Снижение активности фермента вызывает заболевание фенилкетонурию.
фенилаланин |
тирозин |
Изтирозинасинтезируютсякатехоламины-адреналин, норадреналин, дофамин. А также гормонщитовиднойжелезы –Тироксин.
синтезируется втри стадииизпромежуточного продуктагликолиза -3- фосфоглицератаСерин ,который сначала вкетокислоту - 3- фосфогидроксипируват: окисляется

Затемэтакетокислотаподвергается |
|
глутаминовойкислотой |
ипревращаетсяв 3-фосфосерин,который далее |
досерина: |
|
|
транс минированию |
|
гидролизуется
Аминокислота цистеин образуетсяиз незаменимойаминокислотыметионинаи |
||||
заменимойаминокислотысерина.Метионин поставляет длясинтезацистеинаатом |
||||
серы,асерин – углеродныйскелет (ОН-группасериназамещаетсяна SН-группу |
||||
метионина).. |
|
|
|
|
д ления-простейшая аминокислота,синтезкоторойосуществляетсяпутем |
||||
Глицин |
|
|
|
.Реакцияпротекаетс |
участиемкофермента -тетрагидро-фолиевойкислоты (FH4),—которыйслужит |
||||
концевойгидрокс метиленов группы серина |
|
|||
переносчиком одноуглеродныхгрупп.Такогорода переносиграетважную рольв |
||||
синтезе нуклеотидов. |
|
|
|
|
Суммарнореакцию биосинтезаглицинаизегопредшественника - серина -можно |
||||
записатьследующим образом: |
5 |
10 |
|
|
Серин+FH4 |
глицин + N ,N |
-метилен -FH4 |
|
|
какправилосложнее идлиннее путей синтезазаменимыхаминокислот. Организмвысшихорганизмов не способен
синтезироватьПути нтезанезаменимыхаминокислот
ароматические аминокислоты de novo(тирозинне является незаменимойаминокислотойтолько потому,что можетобразоватьсяиз фенилаланина).Кнезаменимымаминокислотампринадлежат аминокислотыс разветвленнойбоковойцепью: валиниизолейцин,атакже лейцин,треонин, метионинилизин.Неспособностьвысших животныхсинтезироватьнезаменимые аминокислотыобъясняется у ниходногоили двух ферментов, необходимыхдляэтогосинтезаотсутствием.Наибольшейсложностью отличаютсяпути, ведущие ксинтезу фенилаланина,триптофанаигистидина,молекулыкоторых содержатбензольные кольцаилигетероциклы.
Питательнаяценностьбелков решающим образомзависитотсодержания незаменимыхаминокислот.
Заболеванияпринарушении обменааминокислот.В сыворотке крови(в норме)
содержание свободных аминокислот составляет 2,7- 4,6 ммоль/л. Аминокислотный состав сывороткисоответствует составусвободных аминокислот в органах и
тканях заисключением более низкогосодержания аспартата иглутамата и повышенногосодержания аспарагинаи глутамина(25 %). Изменение содержания общего аминного азотав сыворотке имочеможет служить одним из показателей нарушения соотношения катаболических илианаболических процессовв организме, сопровождающих ряд патологий.
Увеличение содержания аминокислот в крови (гипераминоацидемия) наблюдается при заболеваниях печени, что связано с пониженным синтезом мочевины, а также при различных тяжелых инфекционных заболеваниях, опухолях, тяжелых оперативных вмешательствах, приводящих к усиленному распаду белков тканей.
Повышениесодержания аминокислот в моче (гипераминоацидурия) наблюдается при заболеваниях паренхимы печени. Это связано с нарушением процессов дезаминирования итрансминирования в печени, атакже в связи с усиленным распадом клеток при тяжелых инфекционных заболеваниях, злокачественных новообразованиях, тяжелых травмах, миопатии, коматозныхсостояниях,
гипертиреозе, прилечениикортизоном иАКТГ.
,онислужат предшественниками многихспециализированныхбиомолекулбел : пуриновыхи
Аминокислоты –этонетолькостроительныеблокивитаминов пиримидиновыхнуклеотидов,различныхгормонов, , коферментов, порфиринов,антибиотиков, пигментов,нейромедиаторов ит.д.