Материал: магістерський іспит з хімії 1
77. Будова і властивості твердих тіл
Твердими називають такі тіла, які зберігають об’єм і форму навіть під час дії на них інших тіл (сил). При зближенні ізольованих атомів і утворення з них кристалу, що складається з N атомів, кожний окремий атом взаємодіє з своїми сусідам, що приводить до появи в кристалі N близько розміщених один від одного підрівнів, які утворюють енергетичну зону. Найвища зона, яка цілком заповнена електронами при T=0 K, називається валентною зоною (ВЗ).Зона, яка заповнена електронами частково або вільна від електронів при T=0 K, називається зоною провідності (ЗП).
Органічні провідники повинні володіти невеликою вагою, невисокою вартістю, високою технологічністю, високою корозійною і хімічною стійкістю. Органічні провідники отримують або вводячи електропровідний наповнювач в полімери - термопласти або реактопласти, або вони являють собою по хімічній будові часто молекули полімерів, наприклад, поліацетилен - СН = СН - СН = СН - СН = СН -.
Парамагнетики -
речовини
з невеликою позитивною магнітною
сприйнятливістю, які у зовнішньому
магнітному полі намагнічуються вздовж
поля і дещо підсилюють
його.Парамагнетизм спостерігається
в речовинах, молекули яких
мають власний магнітний
момент. Закон
Кюрі:
намагніченість газоподібних парамагнітних
речовин прямо пропорційна напруженості
магнітного поля й обернено пропорційна
абсолютній температурі
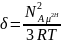 ,
де
μ – магнітний момент однієї молекули,
Т – абсолютна температура,
,
де
μ – магнітний момент однієї молекули,
Т – абсолютна температура,
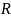 – абсолютна газова стала, δ – намагніченість
речовини.Феромагнітними
наз.
речовини з дуже високою магнітною
сприйнятливістю ( Fe,
Ni,
Co).
Антиферомагнетики —
магнітновпорядковані кристалічні речовини,
які при низьких температурах мають дві
повністю намагнічені спінові ґратки,
які повністю компенсують одна одну.
– абсолютна газова стала, δ – намагніченість
речовини.Феромагнітними
наз.
речовини з дуже високою магнітною
сприйнятливістю ( Fe,
Ni,
Co).
Антиферомагнетики —
магнітновпорядковані кристалічні речовини,
які при низьких температурах мають дві
повністю намагнічені спінові ґратки,
які повністю компенсують одна одну.
Фазовий перехід газ – рідина, газ – тверде тіло називають конденсацією. Тому рідкий і твердий стани речовини називають її конденсованим станом.Всякий матеріальний об'єкт, всяке тіло, що складається з великого числа частинок, називається макроскопічною системою.
Молекулярні кристали кристалічні твердотільні речовини, молекули яких зберігають цілісність в твердій фазі. Йонні кристали в структурному відношенні являють собою позитивні й негативні йони, що правильно чергуються. Сили притягання і відштовхування між йонами визначають стан рівноваги і характерні для кожного кристалу міжйонні відстані.Ковалентні кристали представлені сполуками, хімічні зв’язки у яких обумовлюють спарені електрони. Диполь-дипольна взаємодія - взаємодія між диполями молекул або полярними групами молекул. Існує три типи диполь-дипольних взаємодій:1. Орієнтаційні взаємодії.2. Індукційні взаємодії.3. Дисперсійні (Ван-дер-Ваальсівські) взаємодії.
Індукційна взаємодія викликана тим, що сталий диполь однієї молекули індукує в іншій молекулі чи групі молекул дипольний момент. Орієнтаціна взаємодія - полярні молекули, у яких центри тяжіння позитивного і негативного зарядів не збігаються, наприклад HCl, H2O, NH3, орієнтуються таким чином, щоб поруч знаходилися кінці з протилежними зарядами. Дисперсійна взаємодія - між неполярними молекулами також може виникнути тяжіння. Електрони, які знаходяться в постійному русі, на мить можуть виявитися зосередженими з одного боку молекули, тобто неполярна частина стане полярною. Внутрішньомолекулярний водневий зв'язок - це водневий зв'язок, в якому атом H є зв'язаним з двома (найчастіше) гетероатомами однієї молекули. Мiжмолекуляpний водневий зв'язок– це водневий зв'язок, в якому атом H зв'язаний з двома (найчастiше) гетероатомами рiзних молекул.
76. Двохатомні молекули. Багатоатомні молекули
При квантовомеханічному описі твердих тіл доводиться розглядати системи, що складаються з великого числа електронів і атомних ядер. Оскільки маси ядер в декілька тисяч разів більші маси електрона, то в середньому вони рухаються значно повільніше, ніж електрони. У зв’язку з цим існує можливість наближеного опису твердих тіл, де в нульовому наближенні ядра вважаються нерухомими, а в наступних наближеннях рух ядер враховується методами теорії збурень. Такий наближений опис називається адіабатичним наближенням.
Терми двоатомних молекул - внесок електронів у загальний енергетичний спектр молекул, що складаються із двох атомів. Електронні терми розраховуються при фіксованому положенні ядер атомів і є функціями віддалі між цими ядрами. Терми двоатомних молекул мають особливу класифікацію завдяки симетрії, що виділяє їх в особливий підклас електронних молекулярних термів.
Теорема Вігнера-Неймана стверджує, що рівні енергії станів однакової симетрії не перетинаються ні при якому значенні параметра. До станів однакової симетрії відносять стан з однаковими квантовими числами, власні функції які зі зміною параметра зберігаються.
Коливальний спектр багатоатомних молекули складається з великої кількості смуг (ліній), наявність яких пов'язана з властивостями окремих груп молекули.Із загальної теорії коливальних спектрів багатоатомних молекул відомо, що зміщення атомів при коливанняхможна вважати обернено пропорційними величинам мас атомів. У свою чергу, так звані кінематичні зв'язки між окремими частинами молекули, які проявляються в тому, що при зсувах атомів однієї частини молекули збуджуються коливання і іншій її частині, внаслідок чого в коливання втягується вся структура молекули або комплексу, залежать від величини зміщень атомів, спільних для двох частин молекул. Обертальні спектри двохатомних молекул в самому простому випадку являють собою смуги поглинання (абсорбції) випромінювання, вони, втім, характерні тільки для таких молекул, у яких є дипольниймомент.
Нормальне коливання − це незалежне зміщення атомів в молекулі, при якому положення центру маси не змінюється. Нормальне коливання − це одночасний рух усіх атомних ядер молекули, що відбувається з однаковою частотою і узгоджено за фазою.
Поверхня потенціальної енергії — теоретична модель, яка часто використовується у квантовій механиці у рамках наближення Борна-Оппенгеймера для моделювання простих хімічних перетворень (реакцій).
Ефект Я́на — Теллера — зниження симетрії розташування оточення іонів у кристалах та молекулах за рахунок зняття виродження основного електронного стану.
Ефект Яна—Теллера виникає тоді, коли в симетричній конфігурації основний електронний стан вироджений. Здебільшого це буває в октаедральній конфігурації, зокрема він часто зустрічається в комплексах шестикоординованої міді. Видовження або скорочення однієї з пар міжатомних відстаней призводить до зняття виродження, при цьому енергія одного зі станів — понижується. Як наслідок симетрична конфігурація стає нестійкою. Здебільшого ефект проявляється як видовження, хоча можливе також скорочення.
Явище розщеплення енергетичних рівнів і спектральних ліній під дією на речовину зовнішнього електричного поля називають ефектом Штарка.
Однією
із простих систем точкових зарядів
є електричний
диполь –
сукупність двох однакових за абсолютним
значенням і протилежним за знаком
точкових зарядів +q і –q, розміщеній на
деякій відстані ![]() .
Величину
називають плечем
диполя.
Якщо відстань між зарядами не змінюється,
то такий диполь називають жорстким.
Якщо довжина плеча диполя
мала
порівняно з відстанню
.
Величину
називають плечем
диполя.
Якщо відстань між зарядами не змінюється,
то такий диполь називають жорстким.
Якщо довжина плеча диполя
мала
порівняно з відстанню ![]() від
диполя до точки спостереження, то такий
диполя називають точковим.
Потенціал взаємодії між нейтральними
атомами на великих відстанях між ними
завжди має характер притягання,
спричинений вандервальсовими
силами — взаємодією наведених
дипольних моментів. Притягання відповідає
негативному значенню енергії взаємодії.
Чим далі атоми один від іншого — тим
ближча енергія взаємодії до нуля..
від
диполя до точки спостереження, то такий
диполя називають точковим.
Потенціал взаємодії між нейтральними
атомами на великих відстанях між ними
завжди має характер притягання,
спричинений вандервальсовими
силами — взаємодією наведених
дипольних моментів. Притягання відповідає
негативному значенню енергії взаємодії.
Чим далі атоми один від іншого — тим
ближча енергія взаємодії до нуля..
Орієнтаційна поляризація. За відсутності зовнішнього поля в рідинах та газах з полярними молекулами вектор поляризації Р = 0. Зовнішнє поле намагається зорієнтувати полярні молекули вздовж силових ліній. Внаслідок спільної дії двох факторів (зовнішнього поля і хаотичного теплового руху) у діелектрику з'являється переважаюча орієнтація молекулярних диполів у напрямку поля.
Деформаційна (електронна) поляризація обумовлена зміщенням електричних зарядів в атомах і молекулах під дією зовнішнього електричного поля, що призводить до появи дипольного моменту у цих частинок.
Між молекулами може відбуватися як електростатична, так і донорно-акцепторна взаємодія. Сили електростатичної молекулярної взаємодії, виникнення яких не супроводиться передачею атомами електронів, називаються силами Ван-дер-Ваальса. Їх поділяють на орієнтаційну, індукційну і дисперсійну взаємодії.
Орієнтаційна взаємодія виявляється між полярними молекулами. При зближенні вони орієнтуються таким чином, що різнойменно заряджені кінці їх диполів притягаються і молекули орієнтуються по прямій. Індукційна взаємодія. Якщо зустрічаються полярні й неполярні молекули, то полярні молекули поляризують неполярні, внаслідок чого останні стають індуковано полярними. Дисперсійна взаємодія. Всередині неполярних молекул постійно відбувається перерозподіл електронної густини внаслідок руху електронів в атомах і коливання ядер. Це приводить до синхронної появи і зникнення миттєвих мікро диполів, за рахунок яких молекули притягуються одна до одної.
Надтонке розщеплення – це розщеплення спектральних ліній завдяки взаємодії електронної підсистеми атомів зі спіном ядра.
Ефект Пашена-Бака, полягає в тому, що в сильних магнітних полях складне зєємановських розщеплення спектральних ліній переходить в просте.
Функціями живої речовини в біосфері є:
газова – вплив живих організмів на газовий склад атмосфери (утворення кисню, виділення вуглекислого газу, фіксація Нітрогену тощо);
концентраційна – поглинання живими організмами певних хімічних елементів і їх накопичення (накопичення молюсками в черепашках Кальцію, діатомовими водоростями, хвощами, злаками – сполук Силіцію, морськими водоростями – Йоду);
окиснювально-відновна – живі організми окиснюють та відновлюють певні сполуки (залізо-, сіркобактерії);
біохімічна – синтез і розщеплення органічних сполук, що обумовлює біологічний колообіг та біогенну міграцію атомів.
83.Газова функція живої речовини та біогенний кугооіг води
Газові функції пов'язані з поглинанням і виділенням живими організмами кисню, вуглекислого газу, аміаку, пари води. Газові функції розділяють на види:
-киснево-вуглекислотна функція, завдяки якій створюється основна маса вільного кисню на планеті. Носіями цієї функції є хлорофільні зелені організми. Виділення кисню йде тільки при освітленні зеленої речовини сонячним промінням. Вночі зелені рослини утворюють вуглекислий газ, відбувається процес утворення вугільної кислоти. Тому ця функція і називається киснево- вуглекислотна
6СО2 + 6Н2О → С6Н12О6 + 6О2↑;
-вуглекислотна функція, при якій утворюється біогенна вугільна (H2CO3) кислота за результатом дихання тварин, життєдіяльності грибів, бактерій;
-озонна та перекисьводородна функція, в результаті якої кисень, переходячи в озон, зберігає життя від пагубної дії ультрафіолетового випромінювання. Озон і перекис водню – це продукти життя на Землі;
-азотна функція, завдяки якій вільний азот утворюється живою речовиною ґрунту океану;
-вуглеводнева функція, при якій біогенні гази – вуглеводні, що утворюються в сонячні дні в повітрі хвойних лісів, зменшують теплове випромінювання нашої планети і охороняють рослини від нічного тепловипромінювання;
-водна функція, яка забезпечує біогенний кругообіг води в біосфері живою речовиною. Наприклад, рослини висмоктують воду з ґрунту і підґрунтя, чим знижують рівень ґрунтових вод;
-сірчановоднева або сульфідна функція, яка складається з двох стадій: у перетворенні органічної сірки тваринами і бактеріями на кінцевий продукт – сірководень і відновлення мінеральної сірки бактеріями в сірководень. Наприклад, у присутності органічної речовини і при недоліку кисню система сульфати-сульфіди за участю мікроорганізмів різко зрушується у бік утворення сульфідів
Na2SO4 + 2C → Na2S + 2CO2↑.
Під дією вуглекислоти сірчисті метали розкладаються з утворенням бікарбонатів і карбонатів
Na2S + Н2CO3→ Na2СO3 + Н2S↑.
Сірководень, що утворюється, йде до атмосфери і у вигляді опадів випадає на землю, викликаючи процеси десульфатації ґрунтів (солончаки, торф'яні болота, застояні водоймища).
84. Концентраційна функція живої речовини
Концентраційні функції виявляються в здатності живих організмів накопичувати хімічні елементи. У рослинних тканин знаходиться велика кількість хімічних елементів, що вибірково поглинаються живою речовиною. Всі концентраційні функції живої речовини можна розділити на дві великі групи: концентраційні функції I роду і концентраційні функції II роду.
Функції I роду полягають у здатності живої речовини захоплювати з навколишнього середовища ті хімічні елементи, сполуки яких зустрічаються в тілі всіх без виключення живих організмів. До таких елементів, які входять до складу всіх живих організмів належать H, C, N, O, Na, Mg, Al, Si, P, S, Cl, K, Ca, Fe.
Функції ІІ роду забезпечують концентрацію певних хімічних елементів, які можуть в інших живих організмах не зустрічатися або знаходитися в низьких межах. Організми, які вибірково накопичують один або декілька хімічних елементів, називають організмами- концентраторами. До найбільш відомих організмів-концентраторів відносяться: картопля і соняшник, які накопичують у великих кількостях калій; бобові рослини накопичують кальцій; чай – алюміній; мохи – залізо; раки і павуки – мідь; молюски і корали – кальцій та ін.