Материал: магістерський іспит з хімії 1
66. Визначення фізичних констант
Кожна органічна сполука характеризується фізичними константами за певних умов: для твердих речовин – температура плавлення (ТПЛ), для рідких – температура кипіння (ТКИП), показник заломлення (n) та густина (питома маса) (d).
Найпростішим способом ідентифікації невідомої речовини, а також перевірки її чистоти є визначення її фізичних констант та порівняння їх з літературними даними.
Температурою плавлення (ТПЛ) речовини називається така температура, за якої тверда речовина знаходиться у рівновазі зі своїм розплавом. Чиста речовина має чітко виражену температуру плавлення, яка завжди вища, ніж у забрудненої. Для визначення температури плавлення використовують прилад, Капіляр – тонка скляна трубочка з внутрішнім діаметром 0,6…1 мм завдовжки 30…40 мм. Заповнюють капіляр так: відкритим кінцем його занурюють у речовину, а потім запаяним кінцем донизу кидають у довгу скляну трубку. Повторюють цю операцію багаторазово, доки висота ущільненого шару речовини у капілярі не сягне5…10 мм. Заповнений капіляр закріплюють за допомогою гумового кільця на термометрі так, щоб стовпчик речовини знаходився саме навпроти кульки термометра. Після цього термометр закріплюють гумовою пробкою(з вирізом навпроти шкали) у колбі.Зовнішній вигляд речовини перед плавленням дещо змінюється. Вона ущільнюється, в окремих місцях з’являються бульбашки пари. Потім вона “змочується” – цей момент і є початком плавлення. Коли вся речовина перетворюється на прозору рідину, настає кінець плавлення. Інтервал між початком та кінцем плавлення для чистої речовини – не більше 1…2 °С. З двох визначень розраховується середня температура плавлення.
Температура, при якій тиск пари рідини дорівнює зовнішньому тиску, називається температурою кипіння (ТКИП)Дані про температуру кипіння завжди супроводжуються даними про тиск, при якому її визначали. ТКИП можна визначити як у паровій. так і в рідкій фазі. У першому випадку одержують точніші результати, оскільки температура пари практично не залежить від коливань температури всередині рідини, які неминучі при її безпосередньому нагріванні. На практиці температуру кипіння визначають під час перегонки. Температурою кипіння вважається та температура, яка не змінюється протягом 2…3 хв.
Питомою вагоюназивається фізична величина, що чисельно дорівнює відношенню ваги Р тіла до його об’єму V.Ареометр з постійним об'ємом являє собою циліндр що має додатну плавучість у воді. До ареометра прикріплені чашки (верхня і нижня), в яких розміщують досліджуване тіло і рівноваги. На ареометрі нанесена риска m, до якої ареометр потрібно занурити у воду. При виконані цієї умови об'єм зануреної у воду частини приладу залишається постійним. Звідси і назва приладу "ареометр з постійним об'ємом".
Розчинність речовини в певному розчиннику характеризують її максимальною масою, яка може розчинитися за даних умов (температури, тиску) у 100 г розчинника.Рідини за їх розчинністю у воді поділяють на добре розчинні, малорозчинн і і практично нерозчинні. Деякі рідини, як спирт і гліцерин, змішуються з водою у будь-яких відношеннях, не утворюючи насичених розчинів. За приклад малорозчинних рідин може служити ефір, який уже при невеликих кількостях утворює з водою насичений розчин. Вода в ефірі розчиняється теж дуже мало. Тому при змішуванні ефіру з водою утворюються два шари насичених розчинів: нижній шар — ефіру у воді і верхній — води в ефірі підвищенням температури взаємна розчинність рідин звичайно збільшується. До нерозчинних у воді рідин належать бензин, гас, олія та ін. Вода в цих речовинах теж не розчиняється
70. Кількісний функціональний аналіз
Функціональний аналіз – встановлення наявності функціональних груп в молекулах органічних сполук, наприклад: аміно- (NН2), нітро- (-NО2), гідрокси- (-ОН), карбоксильних (-СООН) та ін. груп. У відповідності із задачами встановлення хімічного складу розрізняють два види аналізу – якісний і кількісний. Ціль кількісного аналізу – знайти кількісні співвідношення між компонентами, знайденими при якісному дослідженні. Часто визначають кількість тільки одного або декількох (не всіх) компонентів проби. Результати аналізу дають можливість встановити хімічні формули синтетичних і природних сполук, оцінити відповідність різних матеріалів потребам виробництва.
Досліджуючи нову або невідому речовину, насамперед, з'ясовують, з яких елементів або іонів вона складається, а потім уже визначають, у яких кількісних співвідношеннях вони складаються. Проте на практиці дуже часто якісний склад аналізованого матеріалу достатньо добре відомий, і це дозволяє відразу приступити до кількісного аналізу, обравши найбільш прийнятний метод. Методи якісного і кількісного аналізу, що дозволяють визначити в аналізованій речовині вміст окремих елементів або іонів, називають елементним аналізом.
Для кількісного аналізу речовини береться точно зважена кількість речовини і непрямим шляхом визначається маса елементів, зв’язаних у речовині.
Якщо речовина складається тільки з Карбону, Гідрогену й Оксигену, то вона повністю окиснюється повітрям або киснем і купрум оксидом до СО2 і Н2О. Вода абсорбується в ємкості, заповненій сухим кальцій хлоридом, а СО2 — в ємкості, заповненій NaOH і скловатою. Збільшення маси в посудинах відповідає масам сполук, що утворюються при згоранні. Завдяки цьому можна розрахувати вміст Карбону і Гідрогену в речовині. Прилад для кількісного визначення Карбону, Гідрогену й Оксигену у складі органічної речовини (апарат Лібіха)
71. Основи класичної теорії хімічної будови
Класична теорія будови речовини була створена у другій половині ХІХ ст. Мікрочасткою в цій теорії є атом, який вважався неподільним. Хімічною часткою є молекула, сукупність яких формує макротіла. Тому предметом вивчення класичної теорії є вивчення будови окремих хімічних часток – молекул. Велике значення у створенні класичної теорії будови речовини відіграв закон кратних відношень. Ця найменша кількість елемента називається атомом, а найменша масова кількість вважається атомною масою.Дальший розвиток вчення про будову речовини був пов’язаний з обгрунтуванням поняття про молекулу, визначенням молекулярних мас і формул речовин.
Структурна формула – цехімічна формула, яка схематично показує порядок сполучення атомів у молекулі.
Молекулярний граф – цеграф з по-різному позначеними (кольорами) вершинами, які представляють атоми різних типів, та по-різному позначеними (кольорами) ребрами, що співвідносяться з різними типами зв'язків, котрий відображає усю сітку зв'язків для даної конфігурації ядер у молекулярній частинці.
Величини, які визначають геометричну конфігурацію молекули: тип гібридизації, число гібридних орбіталей, число неподільних електронних пар, координаційне число, валентний кут, довжина хімічних зв’язків. Види геометричних конфігурацій молекул: лінійна, кутова, трикутна, тетраедрична, тригональна, октаедрична.
Конформація молекули – просторове розташування атомів в молекулі певної конфігурації, обумовлене поворотом навколо однієї або декількох одинарних сигма-зв'язків. Характерна для циклічних сполук.
Види конформацій
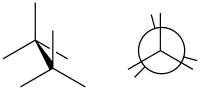 Заслоненная
конформація
Заслоненная
конформація
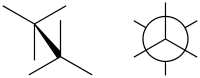 Загальмована конформація
Загальмована конформація
а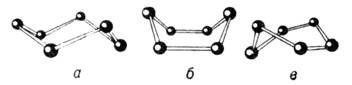 )
конформація
«крісло» - має найменший запас енергії;
)
конформація
«крісло» - має найменший запас енергії;
б) «ванна» - найменш вигідна конформація, найбільше енергії;
в) «твіст» форма
Механічна модель молекули – модель представлена не як електронно-ядерна система, а як система взаємодіючих атомів.
Молекулярна механіка — метод розрахунку геометрії та енергетичних характеристик молекулярних частинок з використанням емпіричних потенціальних функцій, вид яких взято з класичної механіки і в яких враховуються вандерваальсові сили та електростатична взаємодія.
Розглянемо рух вільної частинки, тобто частинки, що рухається у відсутність зовнішніх полів вздовж осі х. Оскільки зовнішні сили на частинку не діють, то її потенційна енергіяі Е = const її можна прирівняти нулю. В такому випадку рівняння Шредінгера для стаціонарних станів матиме вигляд:
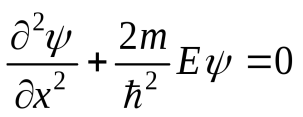 де
m
– маса
електрона, ψ – функція, h
–
стала Планка, Е - енергія
де
m
– маса
електрона, ψ – функція, h
–
стала Планка, Е - енергія
Структурна ізомерія: ізомерія карбонового скелету, ізомерія пов’язана з розміщенням гетероатомів, замісників, кратних зв’язків.
Оптичні ізомери – це просторові ізомери, молекули яких відносяться між собою як предмет і несумісне з ним дзеркальне відображення.
72. Фундаментальні складові матеріальних об’єктів
Елементарними називають частинки, які у взаємодіях поводять себе як єдине ціле. Першою елементарною частинкою, яку відкрив Дж. Томсон у 1897 p., був електрон. У 1919 p. E.Резерфорд виявив частинку, яка входить до складу ядер атомів – протон. У 1932 р. Д.Чедвік відкрив другу складову частинку ядра – нейтрон. У 1905 р. А.Ейнштейн увів у науковий обіг поняття про складову частинку світла – фотон.
Відомо 4 типи фундаментальних взаємодій: сильна (ядерна)відбувається між ядерними частинками (нуклонами) з участю π- мезонів; електромагнітна забезпечує зв'язки між зарядженими частинками; вони реалізуються за допомогою електромагнітного поля;слабка;гравітаційна з усіх інших типів фундаментальних взаємодій найслабша.
В останні роки дуже великого успіху досягла класифікація адронів (елементарні частинки, що беруть участь в сильній взаємодії) на основі кваркової моделі. Кварки були придумані в 1964 р. американськими фізиками Гелл-Маном і незалежно від нього Цвейг. Відповідно до цієї моделі, будь-який адрон складається з трьох кварків з досить незвичайними властивостями. Передбачається, що існує шість ароматів кварків взаємодія між якими здійснюється глюонами. Кварки і глюони мають специфічний заряд, який називається кольором.
Стандартна модель елементарних частинок — теоретична конструкція, що описує електромагнітну, слабку і сильну взаємодію всіх елементарних частинок. Стандартна модель не єтеорією всього, так як не описує темну матерію, темну енергію і не включає в себе гравітацію.
Атомне ядро — позитивно заряджена центральна частина атома, в якій зосереджена майже вся його маса. Ядра складаються з протонів і нейтронів, які є різними станами однієї частинки — нуклона.Вид ядер і атомів з даним числом протонів і нейтронів називають нуклідом.Нуклони пов'язані в ядра завдяки ядерним силам, які значно перевершують сили електростатичного відштовхування, що діють між протонами. Для розщеплення ядра необхідно подолати ці сили, тобто витратити енергію. З'єднання нуклонів з утворенням ядра, навпаки, супроводжується вивільненням енергії, яку називають енергією зв'язку ядра.
Оболонковамодельядра – модель ядраатома, в якій нуклони:протони і нейтрони розглядаються як квантові частинки, що рухаються в самоузгодженому центральному потенціалі й мають дискретний енергетичний спектр, подібний до спектру електронів у атомі.
Ефектом Мессбауера є резонансне поглинання γ-квантів на ядрах речовин, яке виникає тоді коли енергія γ-квантів співпадає з рівнем збудженого ядра.
Нейтронографія - метод вивчення будови молекул, кристалів і рідин за допомогою розсіяння нейтронів. Мезонна хімія – розділ хімії, що вивчає системи в яких або ядро замінене на іншу позитивну частинку або електрон замінений на іншу негативну частинку.
Векторна модель атома. Вихідним її положенням є те, що енергія електрона в складному атомі визначається електронною конфігурацією - розподілом електронів між наявними орбіталями і комбінацією можливих спінових і орбітальних внесків, що призводять до повного кутового моменту атома. Спін-орбітальна взаємодія зв'язує спінову підсистему квантової системи з її координатною підсистемою. Фактично це означає, що завдяки спін-орбітальній взаємодії вектор спіну має орієнтацію в звичайному координатному просторі.Лембів зсув - незначна за величиною зміна енергії квантовихстанів завдяки взаємодії з нульовими коливаннями електромагнітного поля у вакуумі.
73. Симетрія молекулярних систем
Симетрія в хімії виявляється в геометричній конфігурації молекул, що позначається на специфіці фізичних і хімічних властивостей молекул в ізольованому стані, в зовнішньому полі і при взаємодії з іншими атомами і молекулами.
Елементи симетрії – це уявні геометричні образи, за допомогою яких встановлюється симетрія молекул. Для опису симетрії молекул використовують п’ять типів елементів симетрії:центр симетрії;вісь власного обертання;зеркальна площина;інверсійні осі, або зеркально-поворотні осі;елемент тотожності.Операція симетрії - це дія над молекулою із метою встановлення її симетрії. Існують операції: обертання, інверсії, відбиття.
Хвильова функція, яка при перестановці місцями двох частинок системи не змінює свого знаку ― називається симетричною. В тих випадках, коли при аналогічній перестановці частинок системи хвильова функція змінює знак, вона є антисиметричною.Симетрія хвильової функції системи однакових частинок зберігається з часом. Системи однакових частинок із нульовими, або цілочисловими спінами описуються лише симетричними хвильовими функціями і називаються бозонами.Системи однакових частинок із напівцілими спінами описуються лише антисиметричними хвильовими функціями і називаються ферміонами.
Атомною орбіталлю (АО) називають ділянку простору, усередині якої імовірність знаходження електрона максимальна. Атомні орбіталі s-типу мають сферичну симетрію. Існують три однакові за енергією р-АО гантелеподібної форми, які відрізняються одна від одної орієнтацією в просторі: рх, р , рz. Молекулярна орбіталь — наближена хвильова функція електронів молекули, утворена суперпозицією атомних орбіталей різних атомів.
Симетрія рівноважної конфігурації ядер в молекулі спричиняє за собою певну симетрію хвилевих функцій різних станів цієї молекули, що дозволяє проводити класифікацію станів за типами симетрії.
Дипольного моменту μ, є добутком абсолютного значення заряду електрона на відстань між центрами позитивного і негативного зарядів у молекулі μ = ql.
Момент
інерції - скалярна
фізична величина,
міра інертності при обертальному русі
навколо осі, подібно до того, як маса
тіла є мірою його інертності в поступальному
русі. Характеризується розподілом мас
у тілі: дорівнює
сумі добутків мас частинок тіла на
квадрати їхніх відстаней від осі
обертання.
![]()
Нормальні коливання– це незалежні коливанняядер у молекулі, що здійснюються за законом гармонічного осцилятора. Сукупність усіх амплітуд коливань атомів і траєкторій їх руху при даному нормальному коливанні називають формою нормального коливання.Форми нормальних коливань для простих молекул часто зображують у графічному вигляді. Стрілками при цьому вказують траєкторії руху атомів при даному коливанні.
Орбiтальна симетрiя — властивість атомної чи локалізованої молекулярної орбіталі, що характеризує її поведінку під дією операції молекулярної симетрії. Основою для використання орбітальної симетрії в трактуванні хімічних реакцій є розгляд хімічних змін, які включають збереження орбітальної симетрії. Якщо якийсь елемент симетрії зберігається впродовж усього шляху реакції, цей шлях є дозволеним за принципом збереження орбітальної симетрії, коли кожна із зайнятих молекулярних орбіталей молекули реактанту має такий же тип симетрії, як подібні зайняті молекулярні орбіталі молекули продукту