Материал: Л12 Экология гидросферы
ГИДРОСФЕРА
Гидросфера - водная оболочка Земли, представляющая собой совокупность океанов, морей, озер, рек, прудов, болот, подземных ввод. Общая площадь океанов и морей в 2,5 раза больше площади суши. На 75% площади преобладают глубины от 3 до 6 тыс. м.
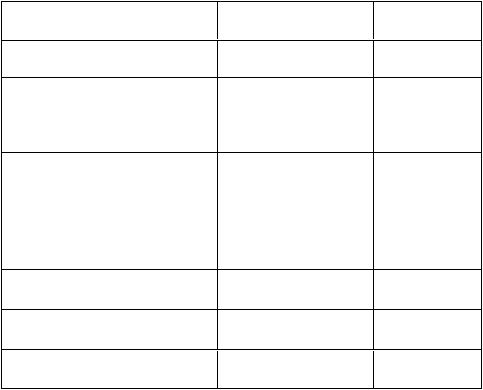
Классификация природных вод и характеристика их примесей. Таблица 5. Распределение водных масс в гидросфере
Форма нахождения |
Объем, 103 км3 |
% |
Мировой океан |
1 370 000 |
94,0 |
Подземные воды |
60 000 |
4,0 |
активного водообмена |
4 000 |
0,3 |
Ледники |
24 000 |
1,7 |
Озера |
280 |
~0,02 |
Почвенная влага |
80 |
~0,01 |
Пары атмосферы |
14 |
~0,001 |
Речные воды |
1,2 |
~0,0001 |
Всего |
1 454 000 |
100,00 |
Растворенные вещества определяют соленость - массу растворенного вещества, в граммах, в 1000 г морской воды.
Различают соленые воды Мирового океана и внутренних морей; пресные воды суши, сосредоточенные в горных льдах, реках, озерах, болотах. Соленые воды Мирового океана и внутренних морей содержат 3,5% солей. Пресные воды суши (горные льды, реки, озера, болота) содержат менее 0,1% солей.
Соленость воды определяется катионами: Na+, Mg2+, Ca2+ и анионами Cl-, SO42-, HCO3-. Соотношения концентрации ионов достаточно постоянны.
В морской воде:
Na+> Mg2+> Ca2+, Cl- > SO42- > HCO3-
1
В материковых водах:
Ca2+ > Na+ > Mg2+, HCO3- > SO42- > Cl-
Пресные воды, содержащие значительное количество солей, называются жесткими. Различают:
1.Временная (карбонатная) жесткость, которую можно удалить при кипячении, т.к. она обусловлена присутствием Ca(HCO3)2 и
Mg(HCO3)2:
Ca(HCO3)2®CaCO3 + CO2 + H2 O
Образуется, в основном, при прохождении воды, насыщенной CO2, через известковые породы:
CaCO3 + CO2 + H2 O® Ca(HCO3)2
CO2 + H2 O « H2CO3
H2CO3 « Н+ + НCO3-
2.Постоянная (некарбонатная) жесткость обусловлена присутствием солей металлов: SO42-,Cl-, NO3-, и др., которые не удаляются при
кипячении.
Если суммарная концентрация ионов Mg2+ и Ca2+ меньше 4 ммоль/л, то вода мягкая; 4÷8 ммоль/л вода - средней жесткости; 8÷12 ммоль/л вода - жесткая
иболее 12 ммоль/л вода - очень жесткая. Наиболее мягкая вода - из атмосферных осадков (дожди, снег), содержит менее 0,1 ммоль/л ионов Mg2+
иCa2+.
р.Амур Москва-река Урал Океан Жесткость, ммоль/л 1,45 4,5 8,2 130
Еще одна характеристика природных вод - общая минерализация воды, определяется суммарной концентрацией (г/л) всех молекул, ионов, различных соединений, содержащихся в воде. Хорошая питьевая вода содержит менее 0,5 г/л растворенных веществ; пресная вода содержит 0÷1 г/л; минеральная вода - 1÷30 г/л, а соленая вода более 30 г/л.
2
Газообмен между атмосферой и гидросферой
Все газы, содержащиеся в атмосфере, частично присутствуют в растворенном состоянии в гидросфере. Между атмосферой и поверхностными слоями воды через поверхностную пленку осуществляется газообмен, причем благодаря диффузии и перемешиванию, газы равномерно распределяются в объеме воды.
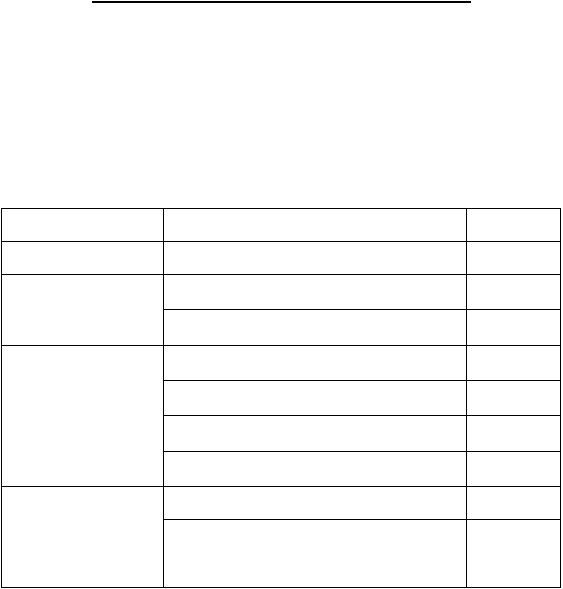
Таблица 6. Диапазон значений рН для различных видов природных вод
Класс, рН |
Природные воды |
рН |
||||
Сильнокислые, <3 Воды вулканических извержений |
>3 |
|||||
Слабокислые, |
Рудничные воды |
3 |
- |
4 |
||
|
|
|
|
|
||
3 |
- |
6,5 |
Болота, грунтовые воды лесной зоны |
4 |
- |
6 |
|
|
|
||||
Нейтральные и |
Подземные воды |
5 |
- |
7 |
||
|
|
|
|
|
||
слабощелочные, |
Реки |
6,8 |
- |
7,8 |
||
|
|
|
|
|
||
3 |
- |
6,5 |
Пресные озера |
7,3 |
- |
9,2 |
|
|
|
||||
|
|
|
Мировой океан |
7,8 |
- |
8,3 |
|
|
|
|
|
||
Сильнощелочные, |
Соляные (содовые) озера |
До 10 |
||||
>8,5 |
Термальные воды (подземные воды, воды |
До 11,5 |
||||
|
|
|
источников с t=37-42°C) |
|
|
|
При нормальных условиях поверхностный слой воды насыщен газом в соответствии с его содержании в атмосфере и давлением, и в большинстве случаев вода содержит максимально допустимое количество газа.
Эта величина определяется законом Генри, который связывает между собой массу газа в единице объема растворителя с парциальным давлением газа, находящимся в равновесии с растворителем:
m=kP,
где k - коэффициент Генри; P- парциальное давление газа; m - масса газа в единице объема растворителя.
Общее содержание кислорода в гидросфере меняется в пределах 6÷12
ppm. Растворимость кислорода понижается с увеличением температуры и
3

солености воды, поэтому холодные пресные воды содержат больше растворенного кислорода, чем теплые соленые.
Карбонатное равновесие
Система "CO2-CO3-2" является одной из наиболее сложных и важных для гидросферы. Она участвует в обмене "воздух-поверхностные слои воды", влияет на химию водной системы, биологическую структуру организмов и отложение осадков, содержащих углерод. От этой системы зависит величина рН среды, что непосредственно влияет на некоторые химические равновесия в данной локальной системе, особенно в отношении ионов тяжелых металлов. Величина рН непосредственно влияет на биологический цикл организмов, в котором углерод используется в процессах развития, гибели и разложения.
Распределение CO2 неравномерно и частично зависит от биологической активности в данном районе. Подобно кислороду, содержание CO2 в поверхностных слоях воды является функцией его содержания в атмосфере, т.е. парциального давления. Однако схемы распределения CO2 и O2 сильно отличаются друг от друга. Так, поверхностные воды Индийского океана вблизи экватора перенасыщены CO2. Это указывает на аномалию равновесной растворимости CO2, т.е. содержание растворимого CO2 в водах Индийского океана повышается при увеличении температуры.
Распределение же общего углерода в зависимости от глубины более единообразно: наблюдается единая тенденция к повышению содержания углерода по мере увеличения глубины вследствие оседания продуктов распада погибших организмов из биологически более богатого поверхностного слоя воды.
Усваиваемый углерод является существенной частью питательных веществ и имеет первостепенное значение во всей экологической структуре гидросферы. CO2 играет основную роль в фотосинтезе.
4

Растворимость CO2 |
явление, чем |
растворимость кислорода, т.к. CO2 |
подчиняется |
закону Генри: |
|
CO2 + H2 |
|
Которая |
|
H2CO3 « Н+ + Н |
|
НCO3- « Н+ + |
|
Процесс растворения CO2 |
чем |
диссоциация по 1-ой ступени, поэтому |
объединяют: |
CO2 + H2 O « |
|
НCO3- « Н |
|
|
|
|
[Н+ ][НСО-] |
|
|
|
|
|
|
К1 = |
[СО ] |
3 |
|
|
|
|
|
||
|
|
|
|
|
|||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
[Н+ ][СО3- 2] |
|
|
|
|
|
|
КД 2 |
= |
[НСО3-] |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Из приведенных уравнений можно |
|
|
|
|
CO2, |
||||
НCO3- и CO3-2 в растворе зависит |
|
|
|
может быть |
|||||
изображено в виде графика (рис. 13). |
|
|
|
|
|
|
|||
1,0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Конц., |
|
|
|
|
|
|
|
|
|
мол.доля |
|
CO2 |
НCO3- |
|
CO3-2 |
||||
|
|
|
|
||||||
0,5
|
0 |
4 |
6 |
8 |
10 |
12 |
14 |
рН |
5 |
2 |
|||||||
|
|
|
|
|
|
|
|