Материал: Курсовая медхим
5.1.4 Ноук (β-нафтоксиуксусная кислота)
Обладает ауксиновой активностью и может применяться в качестве средства стимуляции плодообразования на томатах и землянике. [1]
5.2 Гиббереллины
Гиббереллины — стимуляторы роста растений, выделенные из продуктов жизнедеятельности некоторых грибов и высших растений. Стимулируют цветение, увеличивают число завязей, нарушают период покоя семян, клубней, повышают урожай, ускоряют созревание плодов и т.д. [7]
Гиббереллины представляют
собой группу близких по строению
тетрациклических карбоновых кислот,
относящихся к классу дитерпенов. Наиболее
распространен и преимущественно
применяется гиббереллин
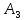 (гибберелловая кислота, ГК).
(гибберелловая кислота, ГК).
У большинства гиббереллинов тетрациклическое ядро несет ряд постоянных заместителей: в положении С-7 — карбоксильная группа, С-17 — обычно экзометиленовая двойная связь, С-18 — чаще всего метильная группа, С-19 — ν- или 19->10-δ лактон или карбоксильная группа. [1]
Наиболее типичное действие гиббереллинов — это стимуляция роста междоузлий стебля у карликовых сортов гороха, кукурузы с нарушенным биосинтезом гиббереллинов или розеточных растений, что используют для биотестов. После обработки гормоном такие растения достигают высоты нормальных сортов. ГК действуют прежде всего на интеркалярные меристемы. После обработки гиббереллином у злаков вытягиваются как стебли, так и листья; у широколиственных растений резко усиливается рост стеблей; растение капусты может достичь двухметровой высоты, а кустовая форма фасоли — превратиться во вьющуюся. Рост стеблей вызван только растяжением клеток. Гиббереллин действует и на эмбриональную фазу роста клетки. Он также стимулирует рост столонов и задерживает образование клубней.
Гиббереллины ингибируют образование и рост корней, но стимулируют разрастание завязей, что приводит к образованию партенокарпических плодов, причем гиббереллины активнее ауксинов. Например, гиббереллин способен вызвать партенокарпию у косточковых, которые не чувствительны в данном случае к ауксину.
Обработка этим гормоном может нарушить состояние покоя. Перед выходом из состояния покоя гиббереллины накапливаются в семенах, луковицах, почках, клубнях. Они активизируют гидролитические ферменты (например, амилазы) и их синтез в зерновках злаков, что вызывает более быстрые превращения запасных веществ и прорастание семян. Возможно, способствуя размягчению семенной кожуры, они облегчают прорастание семян. Выводя семена из состояния покоя, они индуцируют образование плодов и стимулируют их рост. Гиббереллины ускоряют прорастание и свежесобранных клубней картофеля. Нанесение экзогенного гиббереллина индуцирует формирование ювенильных листьев у плюща.
Гиббереллины — один из регуляторов цветения. Под их влиянием у растений с разнополыми цветками увеличивается количество тычиночных цветков. При индукции цветения или стимуляции закладки органов цветка добавление экзогенного гиббереллина может заменить влияние пониженных температур или фотопериода. Эти внешние факторы оказывают влияние через повышение концентрации эндогенного гиббереллина.
У кукурузы закладка женского соцветия происходит при более высокой концентрации эндогенного гиббереллина, чем индукция заложения мужских цветков. Гиббереллин активирует гены, которые блокируют развитие андроцея. У риса и кукурузы не образуется фертильная пыльца.
Гиббереллины усиливают нециклическое фотосинтетическое фосфорилирование, стимулируют работу нижнего концевого двигателя водного тока, что подтверждается увеличением количества выделяемой пасоки у растений, обработанных гиббереллинами.[8]
Препараты гиббереллина, в основном состоящие из гибберелловой кислоты, получают путем микробиологического синтеза, наподобие антибиотиков. Продуцент гиббереллинов — фитопатогенный гриб Fusarium moniliforme Sheld. [1]
5.3 Цитокинины
В 1955 было выделено новое химическое вещество, являющееся по составу 6-фурфуриламинопурином, который образуется из дезоксиаденозина при определенных условиях деградации ДНК. Поскольку его добавление к питательной среде, содержащей сахарозу, элементы минерального питания, витамины и ауксин, вызывало переход клеток изолированной сердцевины стебля табака к делению, это вещество получило название кинетин (от слова кинез — деление).
Вскоре оно было синтезировано. Последовал синтез большого числа его химических аналогов, обладающих такой же или даже более высокой биологической активностью. Все эти вещества были объединены под общим названием цитокинины.
Первый из цитокининов — зеатин — 6-(4'-окси-3'-метил-транс-2'-бутенил-амино)пурин был выделен из семян кукурузы в стадии молочной спелости и идентифицирован Литамом в 1964 г. Это вещество содержится в растениях в очень малых количествах. Для получения 1 мг зеатина потребовалось переработать 70 кг семян кукурузы. При этом нужно иметь в виду, что развивающиеся семена отличаются наиболее высоким содержанием цитокининов.
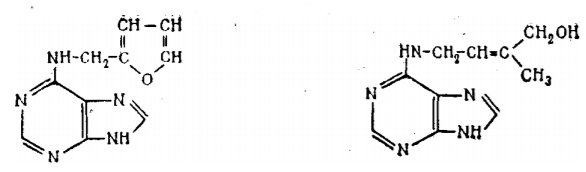
Рис. 6 — Кинетин (слева) и зеатин (справа)
Обязательным для физиологической активности этих соединений является присутствие в их молекуле радикала у аминогруппы при шестом атоме углерода пуринового кольца. Строение этого радикала также подчиняется следующему правилу: у соединений с алифатическим радикалом активность увеличивается по мере удлинения радикала от 1 до 6 атомов углерода и резко падает при дальнейшем его удлинении.
Введение в пуриновое кольцо дополнительных радикалов, как правило, снижает цитокининовую активность соединения. Однако известны случаи, когда введение метильной группы в 8 и 9 положение пуринового кольца повышало активность.[1]
Цитокинины участвуют во многих физиологических процессах растений, регулируют деления клеток, морфогенез побега и корня, созревание хлоропластов, линейный рост клетки, образование добавочных почек и старение.[9] Соотношение ауксинов к цитокининам является ключевым фактором деления клеток и дифференцировки тканей растения.
В то время как эффект цитокининов на сосудистые растения является плейотропным, цитокинины вызывают изменения роста протонемы у мхов. Образование почек можно считать вариантом дифференцировки клеток и этот процесс является очень специфическим эффектом цитокининов.[10]
Главные функции цитокининов — они стимулируют деление клеток и дифференцировку, усиливая синтез ДНК и белка, активируют растяжение клеток листьев у двудольных растений, образование клубней, снимают апикальное доминирование, вызывая заложение и рост пазушных почек. Цитокинины стимулируют растяжение у изолированных семядолей, отрезков стеблей или колеоптилей.
Цитокинины обладают высокой аттрагирующей способностью, т.е. притягивают ассимиляты (аминокислоты, углеводы) и регуляторные вещества к клеткам и тканям, например, к зоне деления клеток, содержащим большое количество этого гормона, что было доказано с помощью следующего опыта. На левую нижнюю часть листа табака нанесли раствор 14С-глюкозы, на правую верхнюю часть — раствор кинетина. Скоро радиоактивная метка была обнаружена в правой верхней части листа, следовательно, сюда поступила глюкоза.
Эти гормоны задерживают старение листьев, что легче всего можно увидеть в опытах с изолированными листьями. Когда отрезанный лист ставят в воду, старение наступает быстро: разрушается хлорофилл, лист желтеет, в нем усиливается распад белка, РНК. Однако старение листа задерживается, если на черешке образуются придаточные корни, синтезирующие цитокинины. Задержка старения связана еще и с тем, что обработка листа, например, кинетином вызывает образование в хлоропластах новых тилакоидов стромы и гран, разрушившихся при старении, усиливает синтез хлорофилла. Формирование хлоропластов у цветковых растений при добавлении экзогенного цитокинина происходит даже в темноте.[8]
5.3.1 Дифенилмочевина и ее производные
Впервые цитокининовая активность была обнаружена у дифенилмочевины. С тех пор цитокининовая активность была обнаружена у большого числа ее производных. [1]
5.3.1.1 Синтез дифенилмочевины
В колбу загружают анилин, триметилсилиловый эфира диэтилкарбаминовую кислоту и нагревают в перегонной колбе при температуре 150-170°C. Затем отгоняют фракцию при температуре 55-113°C. В колбе выпадает осадок, имеющий т. пл. 236-238°C, что соответствует дифенилмочевине. [11]
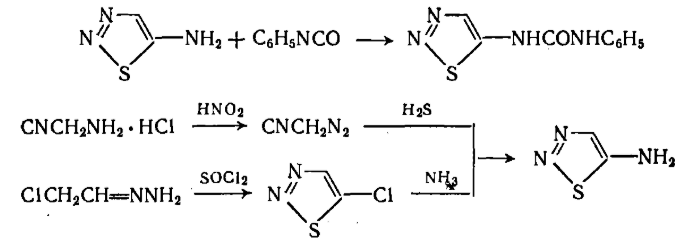
5.3.1.2 Синтез тидиазурона [n-фенил-n'-(1,2,3-тиадиазол-5-ил)мочевины]
Тидиазурон практически с количественным выходом получают по реакции фенилизоцианата с 5-амино-1,2,3-тиадиазолом. Реакция протекает легко в присутствии третичных аминов в качестве катализатора. Необходимый 5-амино-1,2,3-тиадиазол можно синтезировать из нитрила аминоуксусной кислоты или из гидразона монохлорацетальдегида с образованием 5-хлор-1,2,3-тиадиазола и последующим его аминированием. [12]
5.4 Другие стимуляторы роста растений
5.4.1 Фурановые соединения
Некоторые фурановые соединения также являются стимуляторами роста растений.[13]
5.4.1.1 Синтез гидрофуранона:
Реакцию проводят в анодной ячейке, фурфурол смешивают с 30 %-ным Н2О2 и раствором перхлората лития при силе тока 0,01 – 0,03 А.
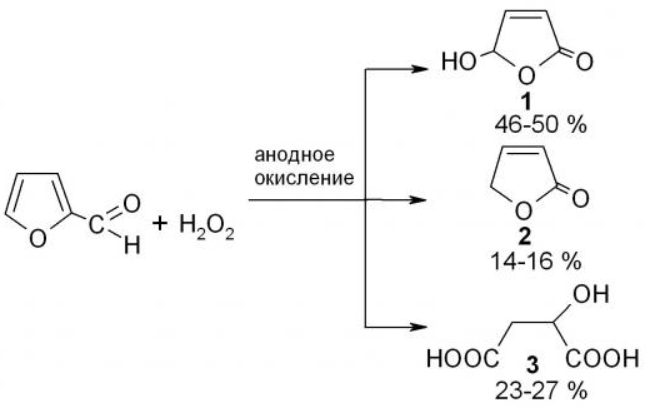
По окончании реакционную смесь нейтрализуют NaHCO3 до рН около 7, удаляют 70-80% воды, удаляют 2(5Н)-фуранон 2 экстракцией CCl4, остаток подкисляют раствором HCl до рН около 2, упаривают досуха, из сухого остатка извлекают 5-гидрокси-2(5Н)-фуранон 1 методом постоянной жидкостной экстракции бензолом в аппарате Сокслета.[14]
5.4.2 Натриевые соли нафтеновых кислот
Водный раствор натриевых солей нафтеновых кислот, содержащий, по-видимому, примеси натриевых солей фенолов, под маркой «НРВ» в настоящее время используется как эффективный стимулятор роста растений. [15]
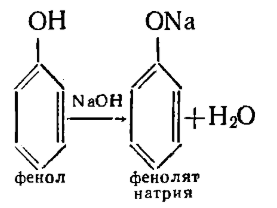
Рис. 7. Схема синтеза фенолята натрия
6 Экспериментальная часть
Было смоделировано следующее соединение в качестве стимулятора: этиловый эфир 4-пиридинкарбоновой кислоты. По предварительной оценке биологической активности соединение обладает следующими свойствами: ингибитор монодегидроаскорбат редуктазы, нитратредуктазы, метилентетрагидрофолатредуктазы, сахарофосфатазы, сульфитоксидазы, регулирует липидный обмен. Все эффекты представлены в таблице 1.
|
Pa |
Pi |
Воздействие |
|
0,897 |
0,004 |
Monodehydroascorbate reductase (NADH) inhibitor |
|
0,885 |
0,003 |
Nitrate reductase (cytochrome) inhibitor |
|
0,874 |
0,009 |
Methylenetetrahydrofolate reductase (NADPH) inhibitor |
|
0,854 |
0,009 |
Sugar-phosphatase inhibitor |
|
0,835 |
0,003 |
Sulfite oxidase inhibitor |
|
0,821 |
0,003 |
Laccase inhibitor |
|
0,817 |
0,005 |
Lipid metabolism regulator |
|
0,813 |
0,008 |
Membrane permeability inhibitor |
|
0,798 |
0,007 |
Ribulose-phosphate 3-epimerase inhibitor |
|
0,775 |
0,006 |
Peroxidase inhibitor |
|
0,750 |
0,007 |
Mitochondrial processing peptidase inhibitor |
|
0,717 |
0,015 |
NADPH-cytochrome-c2 reductase inhibitor |
Таблица 1 — Активности этилового эфира 4-пиридинкарбоновой кислоты в PassOnline
Был предложен и проведен синтез данного соединения:
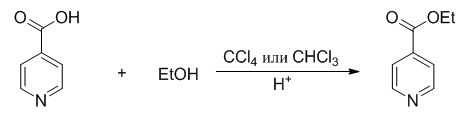
Методика:
В круглодонную колбу (V = 250 мл), снабженную делительной насадкой и обратным холодильником, помещают 30.78 г (0.250 моль) 4-пиридинкарбоновой кислоты, 0.3 мл конц. серной кислоты, 12.67 г (0.275 моль, 10 мл) этанола в 50 мл четыреххлористого углерода или хлороформа. Реакционную массу кипятят на водяной бане до полной отгонки воды. После чего, смесь охлаждают, переносят в делительную воронку и промываю последовательно 100 мл воды, 25 мл насыщенного водного раствора бикарбоната натрия и снова водой до нейтральной реакции. Избыток растворителей упаривают, а остаток перегоняют в вакууме. Получают 23.43 г (62%) продукта в виде маслянистой жидкости, т. кип = 160-162°С при 15 мм. рт. ст. (лит. данные [16]: т. кип = 220°С при 765 мм. рт. ст.).
6.1 Биологические испытания
Было взято два растения (маргаритка): контрольное растение и растение, на которое воздействовали стимулятором (тестовое).

Рис. 8 — Контрольное растение

Рис. 9 — Растение, на которое воздействовали стимулятором
Контрольное растение выросло до 1,5 см, а тестовое — до 2,2 см. Также у тестового растения листочков больше и на верхушке они больше ветвятся.
7 Заключение
-
Было смоделировано следующее соединение: этиловый эфир 4-пиридинкарбоновой кислоты.
-
Были определены его активности в PassOnline.
-
Этиловый эфир 4-пиридинкарбоновой кислоты был синтезирован из 4-пиридинкарбоновой кислоты.
-
Опыт показал, что этиловый эфир 4-пиридинкарбоновой кислоты положительно влияет на рост и ветвление растений.
8 Список использованных источников
-
Гамбург, К. З. Регуляторы роста растений / К. З. Гамбург, О. Н. Кулаева, Г. С. Муромцев, Л. Д. Прусакова, Д. И. Чкаников; под. ред. Г. С. Муромцева. — М.: Колос, 1979. — 246 с.
-
Якушкина, Н. И. Физиология растений: учебное пособие / Н.И. Якушкина, Е.Ю. Бахтенко. — М.: Гуманитар. Изд. центр ВЛАДОС, 2004. — 464 с.
-
Жиряков В. Г., Органическая химия / В. Г. Жиряков - М., 1964. - 488 с.
-
Иоффе И. С., Органическая химия / И. С. Иоффе - Ленинград, 1956.
-
Алферов Б.А., Брахфогель Е.А., Буслаева Л.И. Способ получения 4-хлорфеноксиуксусной или 2,4- дихлорфеноксиуксусной кислот: пат. 2082711 РФ. 1997.
-
Дзбановский Н.А., Терентьев А.П., Уринович Е.М. Способ получения (индолил-3)-гамма-масляной кислоты: пат. 119189 СССР. 1959. Бюл. №8. 4с.
-
Гончаров А. И., Корнилов М. Ю., Справочник по химии / А. И. Гончаров, М. Ю. Корнилов - Киев, 1978. - 308 с.
-
Кузнецов В. В., Дмитриева Г. А., Физиология растений / В. В. Кузнецов, Г. А. Дмитриева - М.: Издательство Юрайт, 2016. — 437 с. — Серия: Бакалавр. Академический курс.
-
Kieber JJ (2002 Cytokinins. In CR Somerville, EM Meyerowitz, eds, [www.aspb.org/publications/arabidopsis/ The Arabidopsis Book]. American Society of Plant Biologists, Rockville, MD, doi: 10.1199/tab.0009
-
Eva L. Decker, Wolfgang Frank, Eric Sarnighausen, Ralf Reski (2006): Moss systems biology en route: Phytohormones in Physcomitrella development. Plant Biology 8, 397—406
-
Шелудяков В. Д., Кирилин А. Д., Кокурочникова Н. Б. Способ получения дифенилмочевины: пат. 583126 СССР. 1978. Бюл. №45. 2с.
-
Мельников Н. Н., Пестициды. Химия, технология и применение / Н. Н. Мельников - М.: Химия, 1987. - 712 с.
-
Пономарев А. А., Синтезы и реакции фурановых веществ / А. А. Пономарев - Саратов, 1960.
-
Яковлев М.М. Реакция фурфурола с пероксидом водорода при воздействии постоянного электрического тока и синтезы гидрофуранонов на ее основе: автореф. дис. канд. хим. наук. Краснодар, 2012.
-
Бурдынь Т. А., Закс Ю. Б., Химия нефти, газа и пластовых вод / Т. А. Бурдынь, Ю. Б. Закс - М., 1978. - 277 с.
-
Потехина А.А. Свойства органических соединений. Справочник. – Л.: Химия. – 1984. – С. 292-293.