Материал: Курсовая медхим
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ
ВЫСШЕГО ОБРАЗОВАНИЯ
«___________________________»
____________________ Минздрава России
УТВЕРЖДАЮ
Заведующих кафедры химии ЛФ
ФГБОУ ВО РНИМУ им.Н.И.Пирогова
Минздрава России ______________________________
« _____» ____________ 20 г.
ОТЧЁТ О НАУЧНО-ИССЛЕДОВАТЕЛЬСКОЙ РАБОТЕ
«СТИМУЛЯТОРЫ РОСТА РАСТЕНИЙ: МОДЕЛИРОВАНИЕ И СИНТЕЗ»
(заключительный)
Исполнитель:
_______________
Руководители:
__________________
|
|
|
|
|
Руководители темы |
_________________/ / подпись, дата |
|
Москва – 2020
1 Реферат
Объем заключительного отчета составил 25 страниц. Было использовано 9 иллюстраций и 1 таблица. Информация была взята из 16 источников.
Ключевые слова: рост растений, стимуляторы роста, стимуляторы роста растений, фитогормоны, ауксины, гиббереллины, цитокинины.
Объект исследования: растение, на котором была протестирована активность синтезированного стимулятора роста.
Цель работы: смоделировать и синтезировать соединение, являющееся стимулятором роста растений.
Методы исследования: анализ информации, прогнозирование, эксперимент.
Результаты работы: был получен смоделированный ранее стимулятор роста растений (этиловый эфир 4-пиридинкарбоновой кислоты), для которого в PassOnline были теоретически определены основные активности. Также было доказано, что полученное соединение является стимулятором роста.
Область применения: соединение может применяться в ботанике и растениеводстве (плодоводство, овощеводство и пр.).
Рекомендации по внедрению результатов: рекомендуется использовать данное соединение для увеличения урожайности и ускорения роста плодовых, овощных и зерновых культур.
Экономическая эффективность работы: внедрение нового стимулятора роста увеличит урожайность и ускорит созревание плодов, что поможет увеличить прибыль от продажи плодовых, овощных и зерновых культур.
2 Содержание
1 РЕФЕРАТ 2
3 ОБОЗНАЧЕНИЯ И СОКРАЩЕНИЯ 4
4
4 ВВЕДЕНИЕ 5
5 ОБЗОР ЛИТЕРАТУРЫ 6
5.1 Ауксины 7
5.1.1 2,4-Д, 4Х и другие феноксикислоты 10
5.1.1.1 Синтез 4Х 10
5.1.2 ИМК [гамма-(индолил-3)-масляная кислота] 10
5.1.2.1 Синтез ИМК 11
5.1.3 НУК (α-нафтилуксусная кислота) 12
5.1.4 НОУК (β-нафтоксиуксусная кислота) 12
5.2 Гиббереллины 13
5.3 Цитокинины 15
5.3.1 Дифенилмочевина и ее производные 16
5.3.1.1 Синтез дифенилмочевины 17
5.3.1.2 Синтез тидиазурона [N-фенил-N'-(1,2,3-тиадиазол-5-ил)мочевины] 17
5.4 Другие стимуляторы роста растений 18
5.4.1 Фурановые соединения 18
5.4.1.1 Синтез гидрофуранона: 18
5.4.2 Натриевые соли нафтеновых кислот 18
6 ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ 20
6.1 Биологические испытания 22
7 ЗАКЛЮЧЕНИЕ 24
8 СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ 25
3 Обозначения и сокращения
ИУК — индолилуксусная кислота.
ИМК — индолилмасляная кислота.
НУК — α-нафтилуксусная кислота.
2,4-Д — 2,4-дихлорфеноксиуксусная кислота.
2,4,5-Т — 2,4,5-трихлорфеноксиуксусная кислота.
3,5-Д — 3,5-дихлорфеноксиуксусная кислота.
2,4,6-Т — 2,4,6-трихлорфеноксиуксусная кислота.
Индолил-3-ПВК — индолил-3-пировиноградная кислота.
4Х — 4-хлорфеноксиуксусная кислота.
НОУК — β-нафтоксиуксусная кислота.
A3 — гибберелловая кислота.
АПК — агропромышленный комплекс.
4 Введение
Сейчас стимуляторы роста очень активно используются в растениеводстве для увеличения урожайности и ускорения произрастания растений. Экзогенные стимуляторы значительно ускоряют получение необходимых для человека культур, что позволяет не только увеличивать урожай, но и сокращать расходы. Поэтому АПК находится в постоянном поиске новых стимуляторов роста, которые будут обладать лучшими характеристиками в сравнении с предыдущими.
Было решено смоделировать и синтезировать новое соединение, которое потенциально будет более дешевым в производстве и/или будет обладать улучшенными свойствами по сравнению с другими стимуляторами.
Цель работы: смоделировать и синтезировать соединение, являющееся стимулятором роста растений.
Задачи работы:
-
Анализ литературы по стимуляторам роста и фитогормонам в целом.
-
Моделирование нескольких соединений, которые потенциально могут стимулировать рост у растений.
-
Проверка этих соединений в PassOnline, отбор лучшего из них, обладающего наиболее подходящими активностями.
-
Синтез отобранного соединения.
-
Проведение опыта на растении (маргаритка), чтобы определить, действительно ли соединение является стимулятором роста.
Актуальность работы: создание новых стимуляторов роста особенно актуально для АПК. Если синтезированный нами этиловый эфир 4-пиридинкарбоновой кислоты будет более дешевым и/или более эффективным, чем другие стимуляторы, то это будет способствовать развитию растениеводства и АПК в целом.
5 Обзор литературы
На рост растений могут оказывать влияние как эндогенные, так и экзогенные вещества. Ниже будут рассмотрены и те, и другие: их строение, функции, механизм (если он известен), а также синтез.
Фитогормоны — это вещества, которые принадлежат к эндогенным регуляторам роста растений, они образуются в растении и участвуют в регуляции обмена веществ на всех этапах его жизни. [1]
Фитогормоны делят на 5 больших групп: ауксины, гиббереллины,
цитокинины, этилен, абсцизовая кислота. [2]
Под действием фитогормонов и экзогенных соединений, стимулирующих рост растений, происходит быстрое удлинение стебля растений, усиление роста, стимуляция цветения и увеличение числа завязей. К активным стимуляторам роста относятся гибберелловые кислоты (гиббереллины) — см. рис. 1, ауксины и гетероауксины. [3]
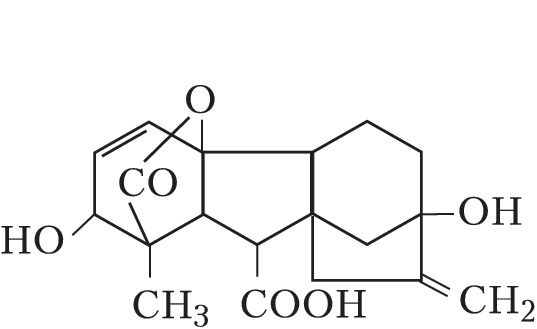
Рис. 1 — Гибберелловая кислота
5.1 Ауксины
Ауксин — первый обнаруженный и наиболее изученный фитогормон. Попытку химической идентификации ауксина впервые предпринял голландский исследователь Кегль, который обнаружил в моче, фекалиях и дрожжах 3-индолилуксусную кислоту. [1]
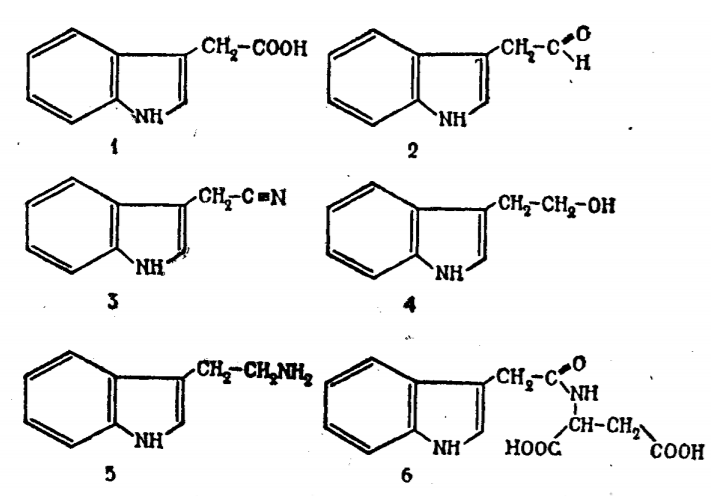
Рис. 2 — Индолилуксусная кислота и ее производные
1 — индолил-3-уксусная кислота; 2 — индолил-3-ацетальдегид; 3 — индолил-3-ацетонитрил; 4 — индолил-3-этанол; 5 — триптамин; 6 — индолил-3-ацетил-N-аспарагиновая кислота.
Наибольшее значение приобрел гетероауксин, представляющий по строению p-индолилуксусную кислоту (рис. 3, а). В настоящее время его готовят в промышленном масштабе и используют в сельском хозяйстве.
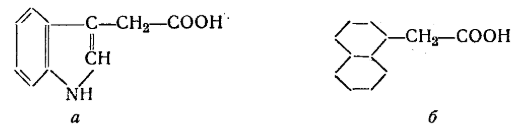
Рис. 3 — Гетероауксин и родственные ему соединения
Получены различные аналоги гетероауксина и родственные ему соединения. Например, альфа-нафтилуксусная кислота (рис. 3, б), которая отличается от него по своему действию — задерживает цветение растений, что позволяет уберечь их от гибели при заморозках. [4]
Ауксиновая активность обнаружена у большого числа соединений, среди которых можно отметить производные фенилуксусной, феноксиуксусной, бензойной кислот, 1-нафтилуксусную кислоту и другие.
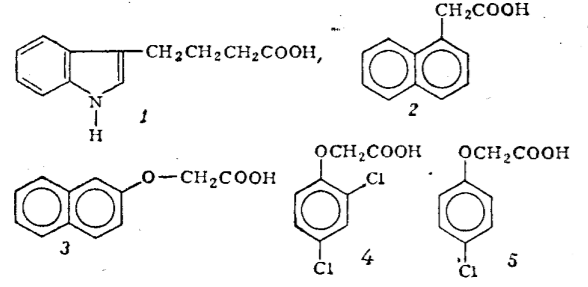
Рис. 4 — Некоторые синтетические аналоги ауксина.
1 — γ-(индолил-3)-масляная кислота; 2 — альфа-нафтилуксусная кислота; 3 — бета-нафтоксиуксусная кислота; 4 — 2,4-дихлорфеноксиуксусная кислота; 5 — 4-хлорфеноксиуксусная кислота.
Помимо участия в тропизмах, для ауксина были установлены и другие эффекты, такие как стимуляция камбиальной активности, роста партенокарпических плодов, образование корней и каллуса, задержка распускания боковых почек и опадания листьев и т. д.
Среди различных гомологов ИУК соединения с четным числом углеродных атомов в боковой цепи обладали более высокой активностью, чем соединения с нечетным числом этих атомов, а индолилкарбоновая кислота вообще не активна. Один из гомологов — индолилмасляная кислота (ИМК) — нашел широкое практическое применение, обладая более высокой активностью в качестве стимулятора образования корней, чем ИУК. Считается, что такой характер зависимости активности от длины боковой цепи определяется тем, что при четном числе углеродных атомов в боковой цепи в результате бета-окисления происходит превращение гомологов в соответствующие уксусные кислоты, а при нечетном числе такое превращение осуществляется с трудом или же приводит к образованию неактивных карбоновых кислот.
Замена одного атома водорода
в боковой цепи ИУК, НУК или 2,4-Д на CH3
приводит к образованию соответствующих
α-пропионовых кислот. При этом возможны
два оптических изомера этих кислот.
Было установлено, что ауксиновая
активность зависит от оптической
изомерии. Например, (+)-изомер
индолил-α-пропионовой кислоты обладал
примерно в 30 раз более высокой активностью,
чем (—)-изомер. При замене обоих атомов
водорода в
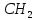 -группе
боковой цепи образуются изомасляные
гомологи ИУК, НУК, 2,4-Д и других синтетических
аналогов ауксина. Эти соединения либо
не обладают ауксиновой активностью,
либо действуют как антиауксины.
-группе
боковой цепи образуются изомасляные
гомологи ИУК, НУК, 2,4-Д и других синтетических
аналогов ауксина. Эти соединения либо
не обладают ауксиновой активностью,
либо действуют как антиауксины.
Введение галогена вместо водорода в ароматическом кольце ИУК, приводящее к образованию 4-хлор-ИУК или 6-хлор-ИУК, также значительно повышает ауксиновую активность. При этих замещениях важное значение имеет взаимное расположение заместителей и ацетильной группы. Например, 2,4-Д и 2,4,5-Т очень активны как ауксины и гербициды, тогда как 2-хлорфеноксиуксусная кислота, 3,5-Д и 2,4,6-Т либо неактивны, либо действуют как антиауксины. [1]
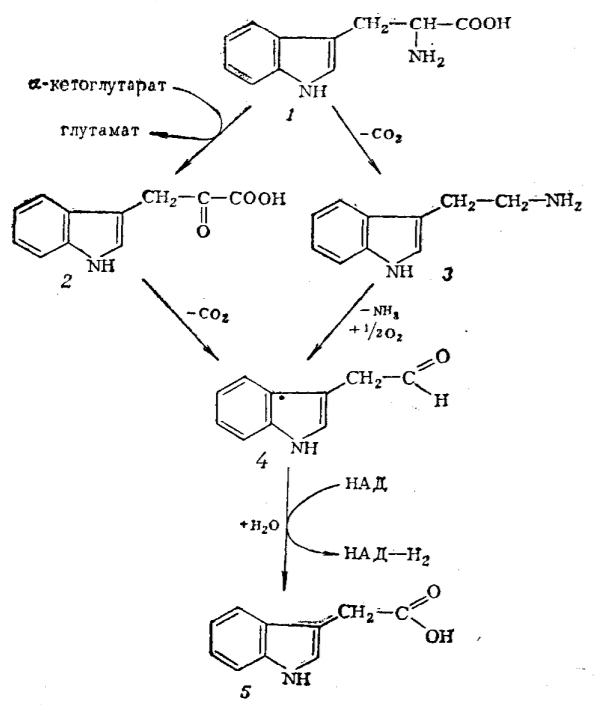
Рис. 5 — Схема путей биосинтеза ИУК
1 — триптофан; 2 — индолил-3-ПВК; 3 — триптамин; 4 — индолил-3-ацетальдегид; 5 — индолил-3-уксусная кислота, НАД и НАД*H2 — окисленный и восстановленный никотинадениннуклеотид.
Есть несколько путей биосинтеза ИУК из триптофана. В основном пути L-Trp под действием трансаминазы превращается в индол-2-пируват, который после декарбоксилирования и окисления превращается в ИУК. Часть ИУК в растениях может иметь бактериальное происхождение. Такое наблюдается в случае заражения бактериями корончатого галла (Agrobacterium tumefaciens). В ходе заражения происходит трансформация растительных клеток плазмидой, несущей гены, отвечающие за неконтролируемый растениями синтез ИУК.
5.1.1 2,4-Д, 4Х и другие феноксикислоты
В качестве регулятора роста используют обычно соли 2,4-Д, хорошо растворимые в воде. Он является физическим аналогом эндогенного ауксина, отличаясь от последнего более высокой персистентностью. Однако эксперименты показали, что применение 2,4-Д в дозах, необходимых для проявления росторегулирующей способности, является фитотоксичным.
В некоторых ситуациях все-таки удается реализовать росторегулирующую активность без фитотоксичности (например, для предотвращения предуборочного опадения цитрусовых).
4-хлорфеноксиуксусная кислота (4Х) обладает гораздо меньшей по сравнению с 2,4-Д фитотоксичностью, что позволяет использовать ее для улучшения плодообразования у томатов. [1]
5.1.1.1 Синтез 4х
В реактор объемом 0,5 л загружают ФУК следующего состава: ФУК 87,0; NaCl 4,8; влага 8,0; фенол 0,2; ледяную уксусную кислоту и уксусный ангидрид. Реакционную массу подогревают до 50°C и начинают подачу хлора. Охлаждают реакционную массу при перемешивании до 11°C и отфильтровывают выпавшую 4-хлорфеноксиуксусную кислоту. Тщательно отжимают уксусную кислоту и промывают 4-хлорфеноксиуксусную кислоту водой, высушивают. [5]
5.1.2 Имк [гамма-(индолил-3)-масляная кислота]
Не содержащаяся в высших растениях ИМК во многих случаях влияет на физиологические процессы так же, как ИУК, но отличается от последней относительно высокой персистентностью.
Представляет собой белое кристаллическое вещество с температурой плавления 124°C, хорошо растворимое в этиловом спирте и многих других органических растворителях. [1]
5.1.2.1 Синтез имк
А. Получение кетокислоты. Реакция протекает по схеме:
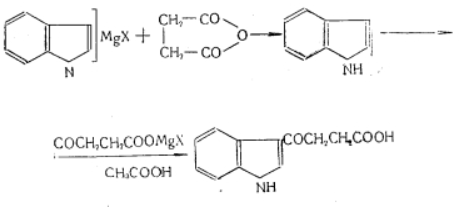
В сухую трехгорлую круглодонную колбу емкостью 500 мл, снабженную мешалкой с затвором, обратным шариковым холодильником и капельной воронкой, помещают магниевую стружку и анизол и затем медленно приливают в течение 1,5-2 час. иодистый этил. В полученный этил магний-иодид при охлаждении в ледяной воде вводят по каплям раствор индола.
K приготовленному раствору индолил магний-иодида, охлажденному до комнатной температуры, быстро приливают горячий раствор янтарного ангидрида.
Затем к смеси приливают разбавленную уксусную кислоту. Выделившуюся кетокислоту отфильтровывают, тщательно отжимают и промывают несколько раз водой. Фильтрат переносят в делительную воронку, где довольно быстро отделяется анизольный слой, из которого анизол может быть легко и с хорошим выходом регенерирован.
Перед восстановлением продукт подвергают щелочному переосаждению и обработке активированным углем.
Б. Восстановление кетокислоты в гамма-(индолил-3)-масляную кислоту.
Реакция протекает по схеме:
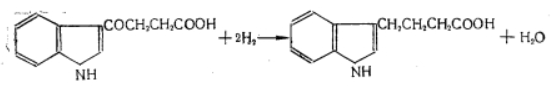
К цинковой пыли (амальгамированной) приливают раствор кетокислоты. Смесь нагревают до кипения при хорошем перемешивании и медленно прибавляют по каплям соляную кислоту. Бутанольный раствор ИМК помещают в прибор для перегонки с паром, смешивают с раствором едкого натра и через смесь пропускают водяной пар до полной отгонки бутанола. Оставшийся щелочной раствор, обычно содержащий небольшое количество бурого хлопьевидного осадка, нагревают до кипения с углем и фильтруют. Фильтрат охлаждают и подкисляют разбавленной соляной кислотой. Затем медленно при перемешивании прибавляют соляную кислоту. Осадок после отжимания на воронке промывают несколько раз холодной водой до удаления соляной кислоты в промывных водах и затем высушивают сначала на воздухе, а потом в эксикаторе.
Для очистки технический продукт перекристаллизовывают из бензола и получают чистую гамма-(индолил-3)-масляную кислоту. [6]
5.1.3 Нук (α-нафтилуксусная кислота)
Физиологический аналог фуксина. Используется в качестве эффективного регулятора роста растений. Производится в виде калиевой соли, амида или метилового эфира. Наибольшее значение имеет калиевая соль α-нафтилуксусной кислоты (КАНУ).
Белое кристаллическое вещество с температурой плавления 131-132°C. Растворимость в 100 мл воды при 25°C 41-42 мг.