Материал: Курс занятий. Нуклеиновые кислоты
Клеточная дифференцировка
Дифференцировка — это процесс, в результате которого клетка становится специализированной, т.е. приобретает химические, морфологические и функциональные особенности. В самом узком смысле это изменения, происходящие в клетке на протяжении одного, нередко терминального, клеточного цикла, когда начинается синтез главных, специфических для данного клеточного типа, функциональных белков. Примером может служить Дифференцировка клеток эпидермиса кожи человека, при которой в клетках, перемещающихся из базального в шиповатый и затем последовательно в другие, более поверхностные слои, происходит накопление кератогиалина, превращающегося в клетках блестящего слоя в элеидин, а затем в роговом слое — в кератин. При этом изменяются форма клеток, строение клеточных мембран и набор органоидов. На самом деле дифференцируется не одна клетка, а группа сходных клеток. Примеров можно привести множество, так как в организме человека насчитывают порядка 220 различных типов клеток. Фибробласты синтезируют коллаген, миобласты — миозин, клетки эпителия пищеварительного тракта — пепсин и трипсин
Изменение белкового состава клеток при дифференцировке (На примере белкового состава полипептидных цепей гемоглобина)
Дифференцировка клеток определенного типа сводится к экспрессии в них комплекса генов, специфичных для данной клеточной линии. Экспрессия этих генов в свою очередь контролируется регуляторными районами гена - промоторами и энхансерами. С промотора начинается транскрипция гена, для чего помимо РНК-полимеразы II требуются и активирующие факторы. Энхансеры - регуляторные районы ДНК, расположенные на некотором расстоянии от контролируемых ими генов, но в том же локусе хромосомы. Активация энхансеров и регуляторных участков промотора ведет к резкому увеличению активности гена, т.е. к усилению скорости его транскрипции. Активация же промоторов и энхансеров происходит при их специфическом взаимодействии с тканеспецифическими ядерными транскрипционными факторами ( ТФ ), набор и специфичность которых определяют направление и уровень дифференцировки данной клеточной линии. Для того, чтобы промоторы и энхансеры тканеспецифических генов могли взаимодействовать с ТФ, они должны быть "открытыми", т.е. не блокированными белками хроматина, который "закрывает" энхансеры и гены, неактивные в клетках данного типа.
Таким образом, дифференцировка клеточной линии осуществляется путем взаимодействия набора тканеспецифических ТФ с энхансерами ипромоторами тканеспецифических генов. Это взаимодействие приводит к экспрессии дифференцировочных генов, определяющих специфичность данной клеточной линии.
Гемоглобины человека. В ходе эволюции из единичных генов-предшественников возникли семейства генов α- и β-глобинов, на хромосомах 16 и 11 соответственно. В процессе онтогенеза у людей образуются разные виды гемоглобинов, обеспечивающие наилучшую адаптацию к меняющимся условиям существования.
НbЕ - эмбриональный, синтезируется у зародыша в первые месяцы развития,
HbF - фетальный, обеспечивает дальнейшее внутриутробное развитие плода, а
НbА и НbA2 осуществляют транспорт кислорода в организме взрослого человека. Эти белки представляют собой тетрамеры, состоящие из полипептидных цепей двух видов: α и β в НbА (2α2β), α и ε в НbЕ (2α2ε), а у остальных гемоглобинов β-цепи заменены на γ-полипептиды в HbF (2α2γ) или на δ-цепи в HbА2 (2α2δ). Полиморфизм гемоглобинов в популяции людей очень велик. Наряду с генами, кодирующими изобелки и занимающими разные локусы на хромосоме, обнаружено большое число вариантов гемоглобина А, являющихся продуктами аллельных генов. К настоящему времени описано свыше 300 вариантов НbА, на основании этого признака всех людей можно разделить на 600 генотипических групп по наиболее часто встречающимся аллелям.
Молекулярные механизмы генетической изменчивости
И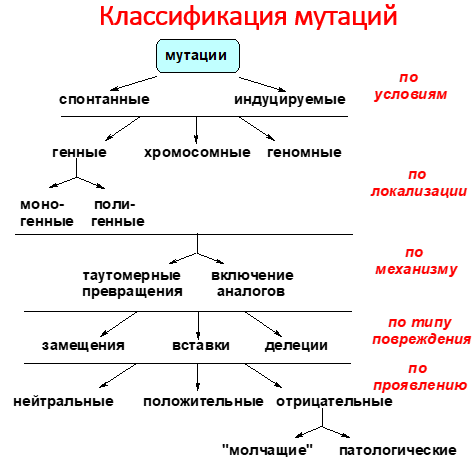
 зменения
в геноме могут быть разнообразны и
затрагивать различные по протяжённости
участки ДНК от хромосом и генов до
отдельных нуклеотидов. Наиболее
драматичны геномные и хромосомные
мутации, часто наблюдаемые на уровне
соматических клеток. Если они имеют
место в половых клетках, то для организма
это имеет чаще всего летальные последствия.
Частота мутаций в половых клетках
высока. Существуют данные, указывающие
на то, что в 20% случаев при беременности
у эмбрионов наблюдают нарушения структуры
хромосом. В 90% случаев это приводит к
ненормальному развитию плода и
элиминированию зародышей в результате
спонтанных абортов. Выкидыши, происходящие
в течение первых нескольких недель
беременности, связаны с серьёзными
нарушениями хромосом. В 50% случаев
отмечается трисомия по аутосомам, т.е.
вместо пары хромосом наблюдаются три.
Пример такой патологии - болезнь Дауна,
при которой хромосома 21 присутствует
в 3 экземплярах. Некоторые генные мутации
закрепляются в популяции, становятся
наследственными и определяют эволюционные
процессы. С мутациями такого типа связано
появление различных наследственных
патологий, сопровождающихся прекращением
синтеза белка, кодируемого повреждённым
геном, либо синтезом изменённого белка.
зменения
в геноме могут быть разнообразны и
затрагивать различные по протяжённости
участки ДНК от хромосом и генов до
отдельных нуклеотидов. Наиболее
драматичны геномные и хромосомные
мутации, часто наблюдаемые на уровне
соматических клеток. Если они имеют
место в половых клетках, то для организма
это имеет чаще всего летальные последствия.
Частота мутаций в половых клетках
высока. Существуют данные, указывающие
на то, что в 20% случаев при беременности
у эмбрионов наблюдают нарушения структуры
хромосом. В 90% случаев это приводит к
ненормальному развитию плода и
элиминированию зародышей в результате
спонтанных абортов. Выкидыши, происходящие
в течение первых нескольких недель
беременности, связаны с серьёзными
нарушениями хромосом. В 50% случаев
отмечается трисомия по аутосомам, т.е.
вместо пары хромосом наблюдаются три.
Пример такой патологии - болезнь Дауна,
при которой хромосома 21 присутствует
в 3 экземплярах. Некоторые генные мутации
закрепляются в популяции, становятся
наследственными и определяют эволюционные
процессы. С мутациями такого типа связано
появление различных наследственных
патологий, сопровождающихся прекращением
синтеза белка, кодируемого повреждённым
геном, либо синтезом изменённого белка.
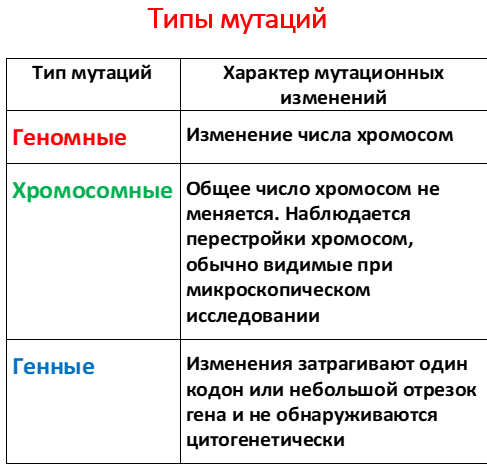
МОЛЕКУЛЯРНЫЕ МУТАЦИИ
Частота мутаций. Считается, что средняя частота возникновения мутаций в структурных локусах (областях локализации гена в хромосоме или в молекуле ДНК) человека колеблется в пределах от 10-5 до 10-6 на одну гамету за каждое поколение. Однако эта величина может значительно варьировать для разных генов (от 10-4 для генов с высокой скоростью мутаций до 10-11 для наиболее устойчивых участков генома). Столь существенные колебания в частоте возникновения мутаций обусловлены характером мутационного повреждения, механизмом возникновения мутации, протяжённостью кодирующей области мутантного гена, функциями белка, закодированного в этом гене. Спрашивается, каким же образом человечество справляется с такой мутационной нагрузкой? Отвечая на этот вопрос, следует помнить, что кодирующие части генов, изменения в которых наиболее опасны, занимают не более 10% генома. Ситуация облегчается ещё и тем, что далеко не каждая мутация в кодирующей области имеет фенотипическое проявление. Многие попадают в 3'-положение кодонов и, таким образом, являются "молчащими", так как благодаря вырожденности генетического кода они не приводят к аминокислотным заменам, другие оказываются в доменах, несущественных для функционирования белков. Потомству передаются мутации, происходящие в гаметах, а их процент совсем невелик.
Виды мутаций |
Изменения в структуре ДНК |
Изменения в структуре белка |
ЗАМЕНА |
|
|
Без изменения смысла кодона |
Замена одного нуклеотида в кодоне |
Белок не изменён |
С изменением смысла кодона (миссенс-мутация) |
|
Происходит замена одной аминокислоты на другую |
С образованием терминирующего кодона (нонсенс-мутация) |
|
Синтез пептидной цепи прерывается, и образуется укороченный продукт |
ВСТАВКА |
|
|
Без сдвига «рамки считывания» |
Вставка фрагмента ДНК из 3 нуклеотидов или с числом нуклеотидов, кратным 3 |
Происходит удлинение полипептидной цепи на одну или несколько АК |
Со сдвигом «рамки считывания» |
Вставка одного или нескольких нуклеотидов, не кратных 3 |
Пептид со «случайной» последовательностью АК, изменяется смысл всех кодонов, следующих за местом мутации |
ДЕЛЕЦИЯ |
|
|
Без сдвига «рамки считывания» |
Выпадение фрагмента ДНК из 3 нуклеотидов или с числом нуклеотидов, кратным 3 |
Происходит укорочение белка на одну или несколько аминокислот |
Со сдвигом «рамки считывания» |
Выпадение одного или нескольких нуклеотидов, не кратных 3 |
Синтезируется пептид со «случайной» последовательностью аминокислот, так как изменяется смысл всех кодонов, следующих за местом мутации |
МЕХАНИЗМЫ УВЕЛИЧЕНИЯ ЧИСЛА
И РАЗНООБРАЗИЯ ГЕНОВ В ГЕНОМЕ
Р екомбинация как источник генетической изменчивости
Генетическая рекомбинация - это перераспределение генетического материала (ДНК), приводящее к возникновению новых комбинаций генов. Рекомбинация может происходить путем обмена клеточными ядрами, целыми молекулами ДНК или частями молекул.
Для всех рекомбинационных процессов характерен этап, на котором молекулы ДНК вступают в контакт в участке, где произойдет обмен полинуклеотидными цепями. Этот этап получил название "синапсис"
Генетическая гетерогенность
Генетическая гетерогенность — явление, когда один и тот же патологический фенотип может быть обусловлен различными мутациями в одном и том же гене (аллельная гетерогенность) либо мутациями в различных генах (локусная гетерогенность).
Полиморфизм белков – изменение первичной структуры белка в пределах одного вида без изменения функций. В его основе лежит генетическая гетерогенность молекул ДНК
гены миоглобина и протомеров гемоглобинов;
группа протеолитических ферментов: трипсин, химотрипсин, эластаза, тромбин и другие белки и ферменты.
Другой важный пример полиморфизма белков, связанный с проблемой переливания крови, - существование в популяции людей 3 аллельных вариантов гена фермента гликозилтрансферазы (А, В и 0). Этот фермент принимает участие в синтезе олигосахарида, локализованного на наружной поверхности плазматической мембраны и определяющего антигенные свойства эритроцитов. Варианты фермента А и В имеют разную субстратную специфичность: вариант А катализирует присоединение к олигосахариду N-ацетилгалактозамина, а вариант В - галактозы. Вариант О кодирует белок, лишённый ферментативной активности. В результате структура олигосахаридов, расположенных на поверхности эритроцитов, будет разной. Антитела к антигенам А и В обычно имеются в сыворотке крови людей, на поверхности эритроцитов которых отсутствует соответствующий антиген, т.е. индивидуумы с антигенами А на поверхности эритроцитов продуцируют в сыворотку крови антитела к В-антигенам (анти-В), а люди с В-антигенами ~ антитела к антигенам А (анти-А). В сыворотке крови анти-А и анти-В обычно присутствуют в высоких титрах и при появлении соответствующих антигенов способны активировать ферменты системы комплемента. При переливании крови руководствуются правилом, согласно которому кровь донора и реципиента не должна содержать антигены и антитела, реагирующие между собой: например, реципиенту, имеющему в сыворотке крови анти-А, нельзя переливать кровь от донора, содержащего на эритроцитах антигены А. При нарушении этого правила происходит реакция антиген-антитело. Это вызывает агглютинацию (склеивание) эритроцитов и их разрушение ферментами комплемента и фагоцитами
Н аследственные болезни
Наследственные болезни - следствие мутаций, произошедших в гаметах или зиготе. Такие мутации могут быть первичными, если возникли в гаметах или в процессе формирования зиготы, или вторичными, если мутантный ген возник раньше и был передан последующему поколению по наследству.
Первичные мутации, как правило, не сопровождаются возникновением болезни, так как происходят обычно в одной из хромосом, и индивидуум, получивший такую мутацию, становится гетерозиготным носителем повреждения в гене. Мутантный ген в гетерозиготном состоянии часто не проявляется как болезнь и существенно не снижает жизнеспособность организма, но способствует его распространению в популяции.
При вторичных мутациях, если каждый из родителей является носителем мутантного гена, будучи гетерозиготой, возможно рождение детей гомозигот по дефектному аллелю. В таком случае развивается наследственная болезнь, часто сопровождаемая очень тяжёлым течением. Около 2,4% всех новорождённых на земном шаре страдают теми или иными наследственными нарушениями. Около 40% ранней младенческой смертности и инвалидности с детства обусловлены наследственной патологией.
К настоящему времени на хромосомах человека выявлено около 800 генов, мутации в которых приводят к развитию различных наследственных болезней. Количество моногенных заболеваний (т.е. вызванных мутациями в определённом гене) ещё больше и равно примерно 950 в результате существования так называемых "аллельных серий", т.е. групп болезней, клинически сильно отличающихся друг от друга, но обусловленных мутациями в одном и том же гене
Более половины генов, в которых найдены мутации, вызывающие наследственные, заболевания охарактеризованы методами молекулярного анализа. Наибольшую по размеру группу составляют ферменты (31% от общего числа). За этой группой следуют белки, модулирующие функции белков и участвующие в правильном сворачивании полипептидных цепей (14%). На каждой хромосоме в среднем идентифицировано около 30 структурных генов, мутации в которых вызывают наследственные болезни.