Материал: Курс занятий. Нуклеиновые кислоты
Строение нуклеиновых кислот
К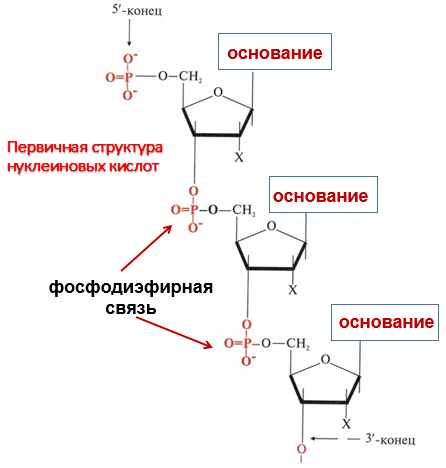 аждый
нуклеотид содержит 3 химически различных
компонента: гетероциклическое азотистое
основание, моносахарид (пентозу) и
остаток фосфорной кислоты. В зависимости
от числа имеющихся в молекуле остатков
фосфорной кислоты различают
нуклеозидмонофосфаты (НМФ), нуклеозиддифосфаты
(НДФ), нуклеозидтрифосфаты (НТФ) .
аждый
нуклеотид содержит 3 химически различных
компонента: гетероциклическое азотистое
основание, моносахарид (пентозу) и
остаток фосфорной кислоты. В зависимости
от числа имеющихся в молекуле остатков
фосфорной кислоты различают
нуклеозидмонофосфаты (НМФ), нуклеозиддифосфаты
(НДФ), нуклеозидтрифосфаты (НТФ) .
В состав нуклеиновых кислот входят азотистые основания двух типов: пуриновые - аденин (А), гуанин(G) и пиримидиновые - цитозин (С), тимин (Т) и урацил (U).
Первичная структура ДНК - порядок чередования дезоксирибонуклеозидмонофосфатов (дНМФ) в полинуклеотидной цепи.
Каждая фосфатная группа в полинуклеотидной цепи, за исключением фосфорного остатка на 5'-конце молекулы, участвует в образовании двух эфирных связей с участием 3'- и 5'-углеродных атомов двух соседних дезоксирибоз, поэтому связь между мономерами обозначают 3', 5'-фосфодиэфирной.
Концевые нуклеотиды ДНК различают по структуре: на 5'-конце находится фосфатная группа, а на 3'-конце цепи - свободная ОН-группа.
Н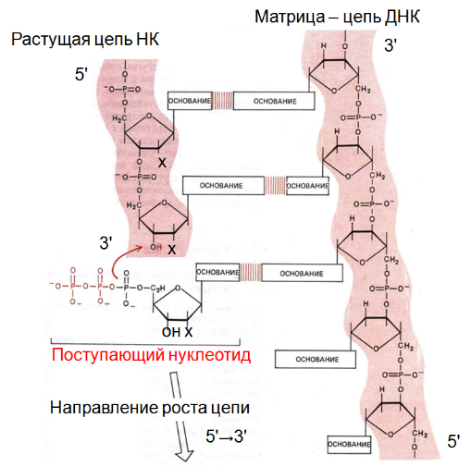 .
к. обладают видовой специфичностью, т.
е. у каждого вида характеризуются
определённым нуклеотидным составом.
.
к. обладают видовой специфичностью, т.
е. у каждого вида характеризуются
определённым нуклеотидным составом.
Биосинтез (репликация) днк
матричный (матрица – обе нити ДНК)
комплиментарный
фрагментарный (нити ДНК синтезируются в виде фрагментов, которые затем соединяются между собой)
полуконсервативный (в каждой из образовавшихся молекул ДНК одна нить исходная – материнская, а одна – вновь синтезированная – дочерняя)
Живые организмы в течение S-фазы клеточного цикла, которая предшествует делению клетки, удваивают содержание ДНК Процесс удвоения хромосом называют репликацией (редупликацией).
Хромосома содержит одну непрерывную двух-цепочечную молекулу ДНК. При репликации каждая цепь родительской двухцепочечной ДНК служит матрицей для синтеза новой комплементарной цепи. Вновь образованная двойная спираль имеет одну исходную (родительскую) и одну вновь синтезированную (дочернюю)цепь. Такой механизм удвоения ДНК получил название «полуконсервативная репликация». Первичная структура дочерней цепи определяется первичной структурой родительской цепи, потому что в основе её образования лежит принцип комплементарности оснований (G = C и A = T).
Д НК–РЕПЛИКАТИВНЫЙ
КОМПЛЕКС
НК–РЕПЛИКАТИВНЫЙ
КОМПЛЕКС
Репликация ДНК осуществляется ДНК-зависимыми ДНК-полимеразами. Субстратами и источниками энергии для синтеза продукта служат 4 макроэргических соединения - дезоксирибонуклеозидтрифосфаты: дАТФ, дГТФ, дЦТФ и дТТФ, для активации которых необходимы ионы магния. Нейтрализуя отрицательный заряд нуклеотидов, они повышают их реакционную способность. Ферменты проявляют каталитическую активность только в присутствии предварительно раскрученной матричной двухцепочечной ДНК. Синтез цепей ДНК происходит в направлении 5'-3' растущей цепи, т.е. очередной нуклеотид присоединяется к свободному З'-ОН-концу предшествующего нуклеотидного остатка. Синтезируемая цепь всегда антипараллельна матричной цепи. В ходе репликации образуются 2 дочерние цепи, представляющие собой копии матричных цепей.
В синтезе эукариотических ДНК принимают участие 5 ДНК-полимераз (α, β, γ, δ, ε). ДНК-полимеразы различают по числу субъединиц, молекулярной массе, ассоциации с разными вспомогательными белками, ускоряющими процесс биосинтеза ДНК, и функциональному назначению. ДНК-полимеразы α (альфа), β (бета), δ (дельта), ε (эпсилон) участвуют в синтезе ДНК в ядре клеток, ДНК-полимераза γ (гамма) - в репликации митохондриальной ДНК. ДНК-полимеразы β, δ, ε не могут инициировать образование дочерних цепей, так как не имеют сродства к одиночной нити ДНК.
Инициирует репликацию ДНК-полимераза α, которая комплементарна определённому сайту одноце-почечной ДНК. Присоединяясь к нему, ДНК-полимераза α синтезирует небольшой фрагмент РНК - праймер, состоящий из 8-10 рибо-нуклеотидов. ДНК-полимераза α состоит из четырёх субъединиц. Каждая из субъединиц фермента выполняет определённую функцию: «узнавание» сайта репликации, синтез прайме-ра (8-10 рибонуклеотидов), синтез фрагмента цепи ДНК, около 50 дезоксирибонуклеотидов. Таким образом, ДНК-полимераза α синтезирует олигонуклеотид, содержащий примерно 60 нуклеотидньгх остатков; первые 8-10 представлены рибонуклеотидами (праймер), а остальные - дезоксирибонуклеотидами
Этапы репликации
1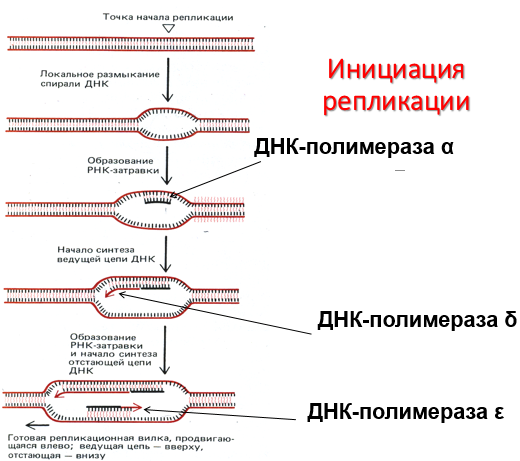 .
Инициация:
.
Инициация:
Топоизомераза находит точку начала репликации, гидролизует одну фосфодиэфирную связь и даёт возможность компоненатам репликативной системы разомкнуть нити ДНК и образовать репликативную «вилку», а затем вновь соединяет связь между мононуклеотиджами
Хеликаза разрывает водородные связи между нитями ДНК
ДНК-связывающие белки (SSB-белки) стабилизируют репликативную вилку, не давая восстанавливаться водородным связям между комплиментарными нуклеотидами
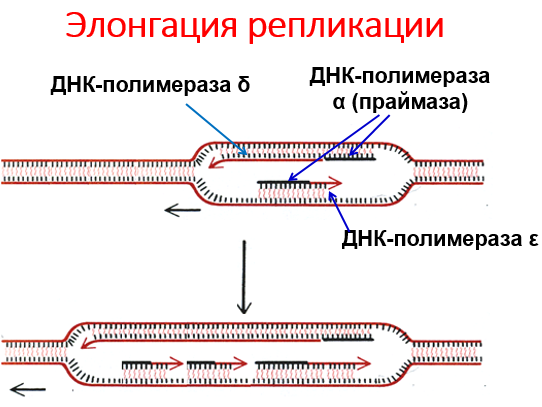
ДНК-полимераза α (праймаза) строит праймер («затравку») из 8-10 рибонуклеотидов и 40-50 дезоксирибонуклеотидов, а ДНК-полимераза δ достраивает нить из дезоксирибонуклеотидов на лидирующей нити, а ДНК-полимераза ε – на отстающей нити ДНК
2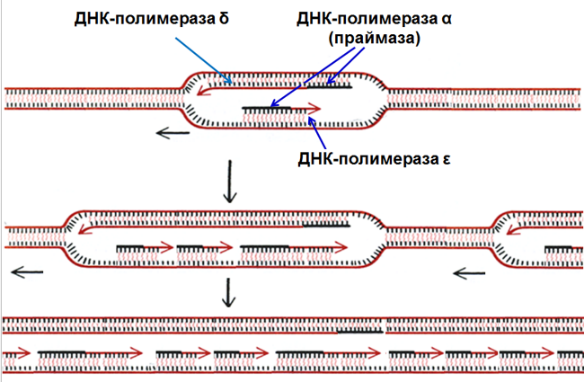 .
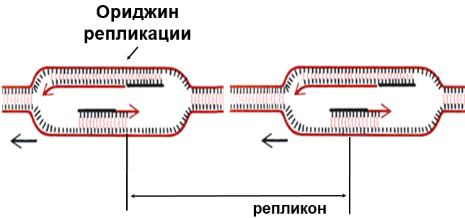
Элонгация
.
Элонгация
ДНК-полимераза δ продолжает удлинять нить из дезоксирибонуклеотидов на лидирующей нити, а ДНК-полимераза ε – фрагменты (фрагменты Оказаки) на отстающей нити ДНК по мере движения репликативной вилки
3. Терминация
ДНК-полимераза β (фермент репарации) удаляет праймеры и достраивает фрагменты ДНК
ДНК-лигаза соединяет фрагменты между собой
Синтез днк и фазы клеточного деления.
РОЛЬ ЦИКЛИНОВ И ЦИКЛИНЗАВИСИМЫХ ПРОТЕИНКИНАЗ В ПРОДВИЖЕНИИ КЛЕТКИ ПО КЛЕТОЧНОМУ ЦИКЛУ.
Процесс митоза принято подразделять на четыре основные фазы: профазу, метафазу, анафазу и телофазу. Так как он непрерывен, смена фаз осуществляется плавно — одна незаметно переходит в другую.
Циклин-зависимые киназы — группа белков, регулируемых циклином и циклиноподобными молекулами. Большинство Циклин–зависимых киназ участвуют в смене фаз клеточного цикла; также они регулируют транскрипцию и процессингмРНК.
Циклин-зависимые киназы являются серин\треониновыми киназами, и фосфорилируют соответствующиеостатки белков. Известно несколько CDK, каждая из которых активируется одним или более циклинами ииными подобными молекулами после достижения их критической концентрации, притом по большей частиCDK гомологичны, отличаясь в первую очередь конфигурацией сайта связывания циклинов. В ответ науменьшение внутриклеточной концентрации конкретного циклина происходит обратимая инактивациясоответствующей CDK. Если CDK активируются группой циклинов, каждый из них как бы передаваяпротеинкиназы друг другу, поддерживает CDK в активированном состоянии длительное время. Такие волны активации CDK возникают на протяжении G1- и S- фаз клеточного цикла.
Повреждение и репарация днк
ДНК-РЕПАРИРУЮЩИЙ КОМПЛЕКС
Процесс, позволяющий живым организмам восстанавливать повреждения, возникающие в ДНК, называют репарацией. Все репарационные механизмы основаны на том, что ДНК - двухцепочечная молекула, т.е. в клетке есть 2 копии генетической информации. Если нуклеотидная последовательность одной из двух цепей оказывается повреждённой (изменённой), информацию можно восстановить, так как вторая (комплементарная) цепь сохранена.
Процесс репарации происходит в несколько этапов. На первом этапе выявляется нарушение комплементарности цепей ДНК. В ходе второго этапа некомплементарный нуклеотид или только основание устраняется, на третьем и четвёртом этапах идёт восстановление целостности цепи по принципу комплементарности. Однако в зависимости от типа повреждения количество этапов и ферментов, участвующих в его устранении, может быть разным.
Биосинтез белка
К оллинеарность
- свойство, обусловливающее соответствие
между последовательностью кодонов
нуклеиновых кислот и аминокислот
полипептидных цепей. В белке воспроизводится
та же последовательность аминокислот,
в какой соответствующие кодоны
располагаются в гене. Это означает, что
положение каждой аминокислоты в
полипептидной цепи зависит от особого
участка гена. Генетический код считается
коллинеарным, если кодоны нуклеиновых
кислот и соответствующие им аминокислоты
в белке расположены в одинаковом линейном
порядке.
оллинеарность
- свойство, обусловливающее соответствие
между последовательностью кодонов
нуклеиновых кислот и аминокислот
полипептидных цепей. В белке воспроизводится
та же последовательность аминокислот,
в какой соответствующие кодоны
располагаются в гене. Это означает, что
положение каждой аминокислоты в
полипептидной цепи зависит от особого
участка гена. Генетический код считается
коллинеарным, если кодоны нуклеиновых
кислот и соответствующие им аминокислоты
в белке расположены в одинаковом линейном
порядке.
Инициация начинается с присоединения к мРНК в области «кэпа» малой субъединицы рибосомы 40S, факторов инициации (IF), инициирующей Мет-тРНКМет и ГТФ. Когда в результате движения этого комплекса по мРНК антикодон Мет-тРНКМет свяжется с инициирующим кодоном АUG, комплекс останавливается. Происходит присоединение 60S-субъединицы рибосомы, сопровождающееся гидролизом ГТФ и отделением факторов инициации. Формируется 80S-рибосома с двумя активными центрами: Р (пептидильным) центром, в котором находится Мет-тРНКМет, и А(аминоацильным) центром, в область которого поступает первый смысловой кодон мРНК.
Этап элонгации включает три последовательные стадии:
- Связывание аа-тРНКаа в А-центре.
- Образование пептидной Пептидил-тРНК связи.
- Транслокация - перемещение рибосомы по мРНК.
Терминация трансляции происходит после включения в А-центр одного из стоп кодонов: UAG, UGA, UAA
Транскрипцией называется синтез РНК на ДНК-матрице. В результате образуются первичные траскрипты мРНК, тРНК, рРНК, комплементарные матричной цепи ДНК, имеющей направление от 3'-, к 5'-концу. Субстратами и источниками энергии для синтеза РНК являются рибонуклеозидтрифосфаты ( НТФ: АТФ, ГТФ, ЦТФ, УТФ).
Катализируют синтез РНК ферменты РНК-полимеразы. В ядре клеток эукариотов обнаружены три фермента:
• РНК-полимераза I, синтезирующая пре-рРНК;
• РНК-полимераза II, ответственная за синтез пре-мРНК;
• РНК-полимераза III, синтезирующая пре-тРНК.
Синтез начинается с того момента, когда РНК-полимераза II присоединяется к матрице в специальном участке - протомотре. Промотор содержит ТАТА-последоательность, которую узнают белком ТАТА-фактором. Матрицей для синтеза служит одна из цепей ДНК.
Элонгация - наращивание молекулы РНК происходит путем присоединения очередного рибонуклеотида, комплементарного тому дезоксирибонуклеотиду ДНК, который находится в активном центре РНК-полимеразы
Терминация. участок ДНК содержит определенный участок - сайт терминации, где заканчивается ген, представляющий из себя последовательность нуклеотидов.И фермент отделяется ДНК-цепь. Модификации пре-мРНК начинаются на стадии элонгации. Когда длина первичного транскрипта достигает примерно 30 нуклеотидов, происходит «кэпирование» 5'-конца.
Первичный транскрипт или пре-мРНК комплементарен гену, содержит как экзоны - последовательности, кодирующие определенные участки молекулы белка, так и интроны - некодирующие последовательности. В процессе образования молекул «зрелой» мРНК интроны вырезаются из первичного транскрипта, концы экзонов соединяются друг с другом - эту реакцию называют сплайсингом РНК
Процесс вырезания интронов протекает при участии малых ядерных рибонуклеопротеинов (мяРНП), которые образуют комплексы - сплайсосомы. После завершения сплайсинга «зрелая» мРНК становится примерно в четыре раза короче первичного транскрипта. Сплайсинг происходит в ядре, в цитоплазму переносится уже «зрелая» мРНК
Биологический код
Биологический код - это способ записи информации об аминокислотной последовательности белков с помощью последовательности нуклеотидов в ДНК или РНК
Триплетность (1 аминокислота кодируется 3 нуклеотидами)
Специфичность (каждому кодону соответствует только 1 аминокислота)
Вырожденность (1 аминокислота может кодироваться более чем 1 триплетом)
Линейная запись (прочтение кода «без знаков препинания»)
Универсальность (одинаков для всех живых существ)
Наряду со значимыми есть и «бессмысленные» кодоны (терминирующие – УАА, УАГ, УГА)
Колинеарность(соответствие линейной последовательности кодонов гена и последовательности АК кодируемого белка)
Транспортная рнк как адаптор аминокислот
Второй тип РНК называют транспортной (адапторной сокращенно— т-РНК). Она выполняет функцию переносчика активированных аминокислотк месту синтеза белка. Каждая молекула такой РНК является адаптером только какой-нибудь одной аминокислоты, т. е. находит место аминокислоты на и-РНК- Поэтому в клетке имеется не менее 20 разновидностей РНК, специализированных для 20 аминокислот.
П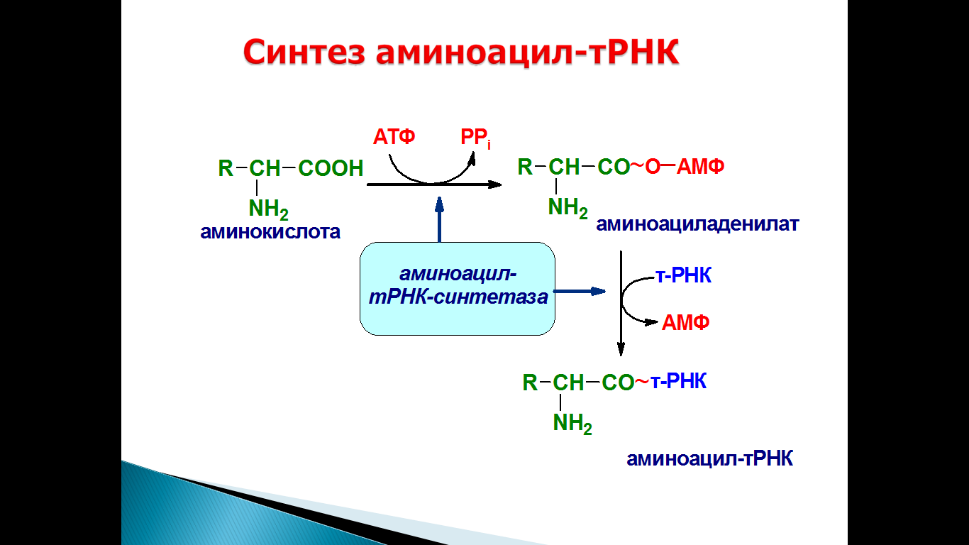 осле
присоединения к соответствующей тРНК
аминокислота уже не участвует в
определении специфичности аминоацил-тРНК,
ибо сама по себе аминоацильная группа
не узнается ни рибосомой, ни мРНК.
Специфичность аминоацил-тРНК обеспечивается
исключительно структурой тРНК. Это было
окончательно доказано четкими опытами,
в которых с помощью ферментов была
получена цистеинил-тPHKCys, которую затем
выделили и химическим путем превратили
в аланил-тPHKCys. После этого такую гибридную
аминоацил-тРНК, которая несет аланин,
но содержит антикодон для цистеина,
инкубировали в бесклеточной
белоксинтезирующей системе. При анализе
новосинтезированного полипептида было
обнаружено, что в положениях, которые
должен занимать цистеин, присутствует
аланин
осле
присоединения к соответствующей тРНК
аминокислота уже не участвует в
определении специфичности аминоацил-тРНК,
ибо сама по себе аминоацильная группа
не узнается ни рибосомой, ни мРНК.
Специфичность аминоацил-тРНК обеспечивается
исключительно структурой тРНК. Это было
окончательно доказано четкими опытами,
в которых с помощью ферментов была
получена цистеинил-тPHKCys, которую затем
выделили и химическим путем превратили
в аланил-тPHKCys. После этого такую гибридную
аминоацил-тРНК, которая несет аланин,
но содержит антикодон для цистеина,
инкубировали в бесклеточной
белоксинтезирующей системе. При анализе
новосинтезированного полипептида было
обнаружено, что в положениях, которые
должен занимать цистеин, присутствует
аланин
Субстратная специфичность арс-аз изоакцепторные т-рнк.
Реакция аминоацилирования осуществляется ферментами аминоацил-тРНК-синтетазами, способными узнавать три различных субстрата: АТФ, аминокислоту и тРНК. В активном центре молекулы фермента осуществляются активация аминокислоты и присоединение ее к концевому остатку рибозы тРНК. Для каждой аминокислоты в клетке имеется аминоацил-тРНК-синтетаза (АРСаза), способная отличать свою аминокислоту от остальных, часто очень похожих по структуре/
Аминоацил-тРНК-синтетазы осуществляют присоединение аминокислоты к молекуле транспортной РНК, что является ключевым моментом в реализации генетической информации.
Изоакцепторные тРНК. - Группа тРНК, связывающих одну и ту же аминокислоту, но имеющих разные антикодоны; разные Изоакцепторные тРНК узнаются одной и той же аминоацил-тРНК-синтетазой; Изоакцепторные тРНК отсутствуют у метионина и триптофана, а наибольшее их число (по 6) распознают кодоны аденина, лейцина и серина;Изоакцепторные тРНК могут иметь одинаковые антикодоны, но различную первичную структуру.
Строение рибосомы
Различают рибосомы эукариот и рибосомы прокариот. Число рибосом прокариот - 10(в 4 степени), диаметр 8 нм. Число рибосом эукариот 10 ( в 5 степени), диаметр 23 нм..Химически рибосомы представляют собой нуклеопротеины, состоящие из РНК и белков, причем 80S (Сведбергов) рибосомы эукариот содержат примерно равное соотношение РНК и белка, а у 70S рибосом прокариот соотношение составляет 65% и 35% соответсвенно. Рибосома представляет собой сложную молекулярную "машину" синтеза белка. Так же рибосома представлена двумя субчастицами - большой и малой. Большая субчастица рибосомы состоит из одной высокомолекулярной рРНК, двух низкомолекулярных рРНК и 41 белка. В состав малой субчастицы рибосомы входит другая высокомолекулярная РНК и 31 белок.
Полирибосома — несколько рибосом, одновременно транслирующих одну молекулу иРНК. Поскольку длина средней молекулы мРНК значительно превышает количество нуклеотидов, занимаемых на РНК рибосомой, одну молекулу РНК, в зависимости от скорости инициации одновременно транслируют несколько рибосом. Образование и количество рибосом в полирибосоме зависит от скорости инициации, элонгации и терминации на данной конкретной РНК. Чем длиннее пептидная цепь кодируемого белка, тем длиннее молекула РНК и тем больше рибосом в полирибосоме.