Материал: Конспект
Параметри стану|достатку|
Фізичні величини, що визначають стан|достаток| речовини, називаються параметрами стану|достатку|. Вони підрозділяються на термічні і калоричні|.
Термічні параметри:
Тиск – сила, що діє по нормалі до одиниці площі. Ра = Рб + Рм; Ра – абсолютний тиск; Рб – барометричний тиск; Рм – манометричний (надлишковий тиск) Рв = Рб - Ра Рв – вакуум (розрідження) Одиниці вимірювання тиску
Т,К = toC + 273 3. Об’єм V, м3 Питомий об’єм - v, м3/кг
|
Калоричні параметри: 1.Внутрішня
енергія –
Питома
внутрішня енергія -
Зміна внутрішньої енергії
2. Ентальпія – I або Н, Дж
Питома ентальпія i або (h), Дж/кг
Зміна ентальпії Δі Δ 3. Ентропія – S, Дж/К Питома ентропія
Для
ідеального газу:
Для
реального газу
S – функція параметрів стану s=f(Р,V,t).
|
Рівняння стану|достатку| ідеального газа
Ідеальним газом називається газ між молекулами якого відсутні сили тяжіння і відштовхування, а молекули і атоми цього газу взаємодіють між собою як матеріальні точки|точки|.
Найбільш просте рівняння стану|достатку| – це рівняння Менделєєва – Клапейрона.
Для , кг| газу; для 1кг| газу:
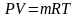 ;
;
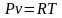
Газова
стала
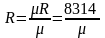 ;
;
;
;
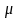 - молекулярна вага газу
- молекулярна вага газу
I закон термодинаміки
Теплота – форма передачі енергії за допомогою елементарних частинок|частинок|, що хаотично переміщаються. Повна|цілковита| теплота – Q, Дж; питома теплота – q=Q/m, Дж/кг.
Робота – форма передачі енергії, що характеризується переміщенням тіл в просторі|простір-час|. Повна|цілковита| робота – L, питома робота l=L/m Дж/кг .
Робота і теплота визначаються за формулами:
|
|
Формулювання I закону термодинаміки:
Повна енергія ізольованої термодинамічної системи залишається постійною при будь-яких процесах, що відбуваються в системі, або
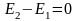 .
.Теплота, що підводиться до тіла або системи в термодинамічному процесі, витрачається на зміну внутрішньої енергії і здійснення роботи для газу масою m: Q=ΔU+L; для 1кг: q=Δu+l; у диференціальній формі: dq=du+dl=du+pdv або dq=di-vdp.
Неможливо побудувати таку теплову машину, в якій роботи вироблялося б більше, ніж кількість теплоти, що підводиться (вічний двигун першого роду неможливий).
3.1. Теплоємність
Теплоємністю називається кількість теплоти, що підводиться (відводиться|відводить|) до одиниці кількості речовини, для зміни температури на один градус С
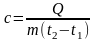 ;
;
де
Q –
кількість теплоти, Дж;
- кількість речовини;
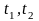 - початкова і кінцева|скінченна|
температури. Залежно від одиниці
кількості речовини розрізняють такі
питомі теплоємності:
- початкова і кінцева|скінченна|
температури. Залежно від одиниці
кількості речовини розрізняють такі
питомі теплоємності:
1. Масова теплоємність – с, Дж/(кг∙К);|із|
2.
Об'ємна теплоємність -
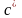 ,
Дж/(кг∙К);
,
Дж/(кг∙К);
3.
Молярна теплоємність -
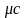 ,
Дж/(кмоль∙К).
,
Дж/(кмоль∙К).
Теплота може:
1. Не залежати від температури, тоді
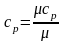 ;
;
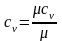
2.
Залежати від температури лінійно
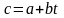 або не лінійно
або не лінійно
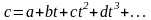
де
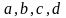 - коефіцієнти,
- коефіцієнти,
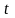 - температура
- температура
Якщо
теплоємність визначається в межах
якоїсь однієї температури, то така
теплоємність називається істинною
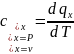 ;
якщо її визначають в інтервалі температур,
то теплоємність називають середньою
;
якщо її визначають в інтервалі температур,
то теплоємність називають середньою
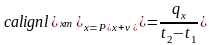 .
.
Якщо
теплота підводиться в процесі з постійним
тиском,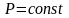 ,
то такі теплоємності називають
ізобарними:
,
то такі теплоємності називають
ізобарними: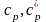 ,
,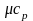 ;
якщо ж теплота підводиться в процесі з
постійним об'ємом
;
якщо ж теплота підводиться в процесі з
постійним об'ємом
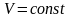 ,
то такі теплоємності називають ізохорними:
,
то такі теплоємності називають ізохорними:
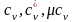 .
.
При лінійній залежності значення теплоємності визначають експериментально|експериментальний| (дослідом|дослідом|) і заносять в таблиці. Тоді середня теплоємність
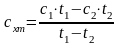
х=Р
х=v
4. II закон термодинаміки
Формулювання:
1. Теплота не може довільно переходити від тіл менш нагрітих до тіл більш нагрітих.
2. Неможливо створити періодично діючу теплову машину, всі дії якої зводилися б до піднімання|підняття| вантажу|тягаря| і охолодження|охолодження| теплового джерела.(Вічний двигун II роду неможливий).
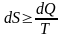 - аналітичне вираз|вираз|
закону.
- аналітичне вираз|вираз|
закону.
Знак
«=»|
відноситься до протікання в системі
оборотних процесів, при цьому ентропія
системи не змінюється. Знак «>»|
відноситься до протікання в системі
необоротних|незворотних|
процесів, при цьому ентропія системи
досягає будь-якого максимального
значення. Якщо
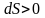 -
теплота підводиться, якщо
-
теплота підводиться, якщо
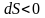 - відводиться|відводить|.
- відводиться|відводить|.
5. Термодинамічні процеси
1.
Ізобарним
називається процес, що протікає з|із|
постійним тиском|тисненням|
.
Співвідношення між параметрами
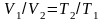 - закон Гей – Люсака.
- закон Гей – Люсака.
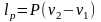 ;
;
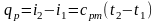
2.
Ізохорним
називається процес, що протікає з|із|
постійним об'ємом|обсягом|,
,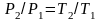 ,
- закон Шарля;
,
- закон Шарля;
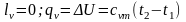
3.
Ізотермічним
називається процес, що протікає з|із|
постійною температурою,
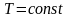 ,
,
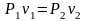 ,
закон Бойля – Маріотта.
,
закон Бойля – Маріотта.
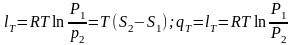
4.
Адіабатним
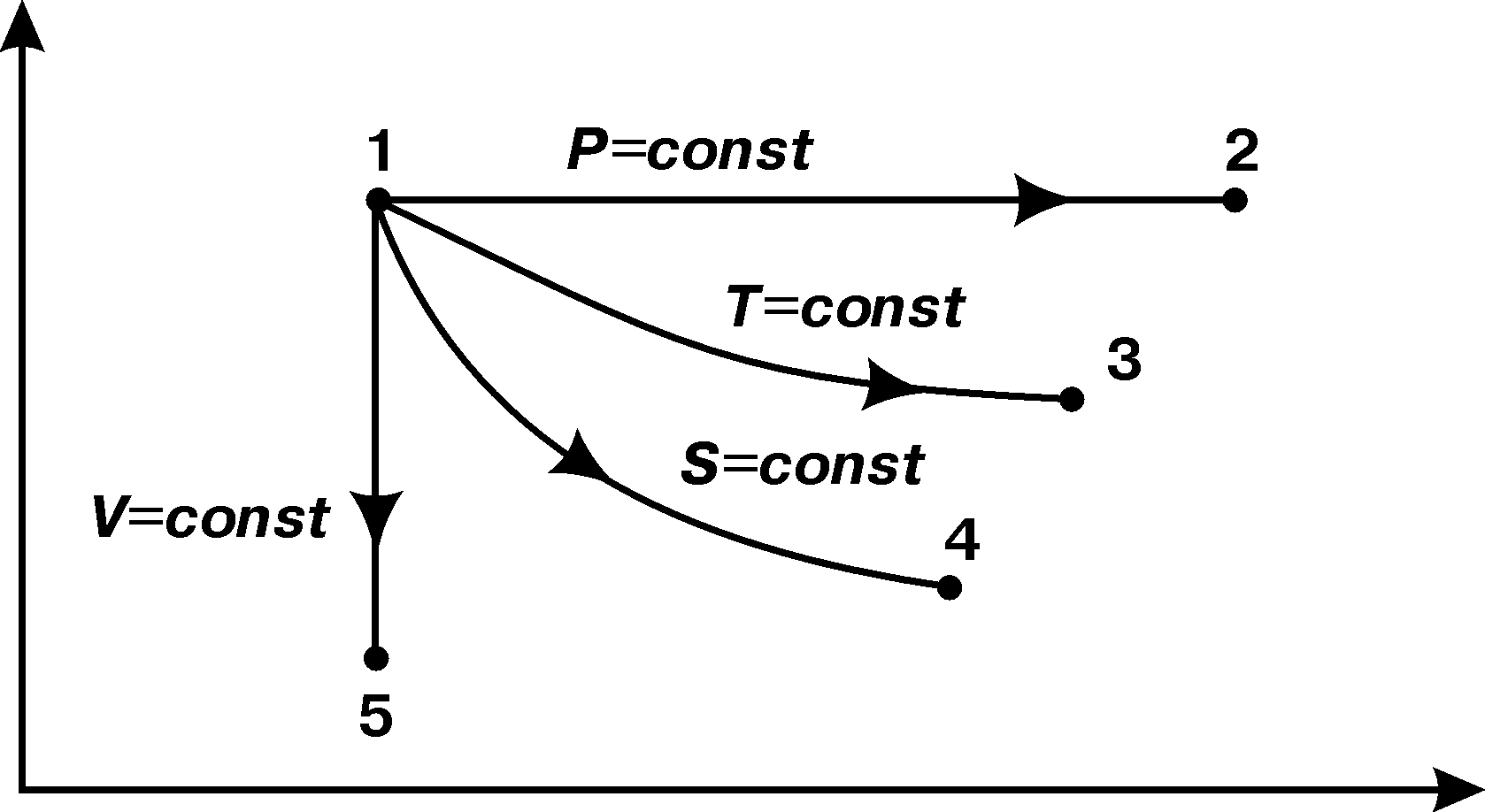
називається процес, що протікає без
теплообміну з|із|
навколишнім середовищем при постійній
ентропії
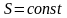 ,
,
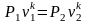 ,
,
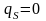 ;
;
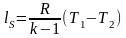
де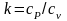 - показник адіабати;
- показник адіабати;
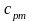 - середня теплоємність при постійному
тиску|тисненні|,
- середня теплоємність при постійному
тиску|тисненні|,
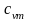 - середня теплоємність при постійному
об'ємі|обсязі|.
- середня теплоємність при постійному
об'ємі|обсязі|.
5.
Політропним
називається процес, що протікає з|із|
постійною теплоємністю і підпорядковується
рівнянню
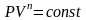 ;
;
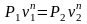 ;
п -
показник політропи
;
п -
показник політропи
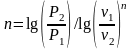
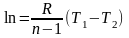 ;
;
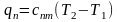 ;
;
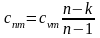
Процеси в P-| V координатах
|
Лінії на P – V діаграмі: 1-2 – ізобара, ; 1-3 – ізотерма, ; 1-4 – адіабата
,
1-5 – ізохора,
|
Реальні гази
Реальним газом називається газ, між молекулами якого існують сили тяжіння і відштовхування, а молекули і атоми газу мають масу і об'єм|обсягом|. Рівняння стану|достатку| реального газу Ван - дер-Ваальса
|
а, b – постійні коефіцієнти, які залежать від природи газу; v – власний об'єм молекул;
|
|
|
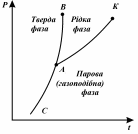
|Перехід речовини з|із| одного агрегатного стану|достатку| в інший називається фазовим переходом. Перехід з твердої фази в рідку – плавлення. Перехід з рідкої фази в пароподібну: випаровування – пароутворення з поверхні рідини, кипіння – бурхливе пароутворення в об'ємі з паровими міхурами. Перехід з пароподібного стану в рідкий – конденсація. Перехід з твердої фази у пароподібну – сублімація. Криві фазових переходів зображаються в P-t діаграмі.
|
Рівноважні криві: АВ – плавлення; АК – пароутворення; АС – сублімація. Точка, у якій речовина існує в трьох агрегатних станах, називається потрійною точкою (т.А). Лінія пароутворення закінчується критичною точкою К. Її параметри. У цій точці:
Ніяким зусиллям стиснення неможливо сконденсувати пару. |
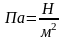
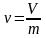
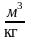 ;
;
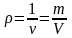
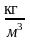
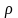 - густина речовини;
- густина речовини;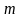 - маса речовини.
- маса речовини.
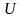 ,
Дж
,
Дж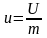
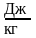
 Δ
Δ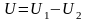
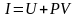
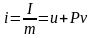
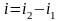
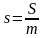
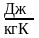 ;
;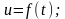
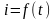
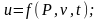
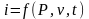
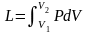 ,
,
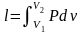 ;
;
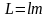
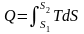 ,
,
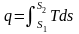 ,
,
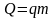
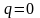 ,
;
,
;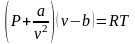
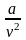 - внутрішній тиск.
- внутрішній тиск.