Материал: Конкуренция среди семи субъединиц Escherichia coli
При насыщении порядок кор-фермент-связанных субъединиц σ составлял σ70 > σN > σF > σH/σFecI > σE > σS. В условиях насыщения σ доля холофермента Eσ70 составляла ∼39% от общего количества холоферментов. Отсюда мы заключаем, что в условиях конкурентного связывания в присутствии всех семи субъединиц σ сродство σ70 является самым сильным, а сродство σS-самым слабым. Судя по разнице сродства (>16 раз) в связывании кор-фермента между σ70 и σS и значению Kd = 0,26 нм для σ70 (см. выше), мы оцениваем, что кажущееся значение KD для σS с кор-ферментом составляет ≈ 4,3 нм (табл.1).
-
σ subunit
Kd (nM)a
Core binding affinity
Intracellular concentrationb
Holoenzyme ratioc (%)
(fmol/mg protein)
(molecules/cell)
σ70 (σD)
0.26
1.0
160
700
78
σ54 (σN)
0.30
1.55
25
110
8
σ38 (σS)
4.26
16.4
<1
<1
0
σ32
(σH)
1.24
4.75
2.1
<10
0
σ28
(σF)
0.74
2.85
85
370
14
σ24
(σE)
2.43
9.35
1.4
<10
0
σ18
(σFecI)
1.73
6.65
<1
<1
0
Переключение одной кор-фермент-связанной σ на другую σ-субъединицу
 Исходя
из сродства связывания каждой субъединицы
σ, как указано выше, мы можем предсказать
эффективность замены одной σ-субъединицы,
связанной с кор-ферментом, другой
σ-субъединицей. Здесь мы протестировали
две крайние комбинации: (i) σ70
и σH,
которые имеют в 10 раз более низкое
сродство связывания с кор-ферментом,
чем σ70;
и (ii) σ70
и σN,
которые имеют сродство связывания с
кор-ферментом вплоть до σ70.
Эквимолярную смесь кор-фермента (20
пмоль) и одной субъединицы σ (20 пмоль)
инкубировали до равновесия и затем
добавляли эквимолярное количество (20
пмоль) второй субъединицы σ. В различные
моменты времени после добавления второй
σ-субъединицы измеряли концентрацию
σ-связанной с ферментом субъединицы.
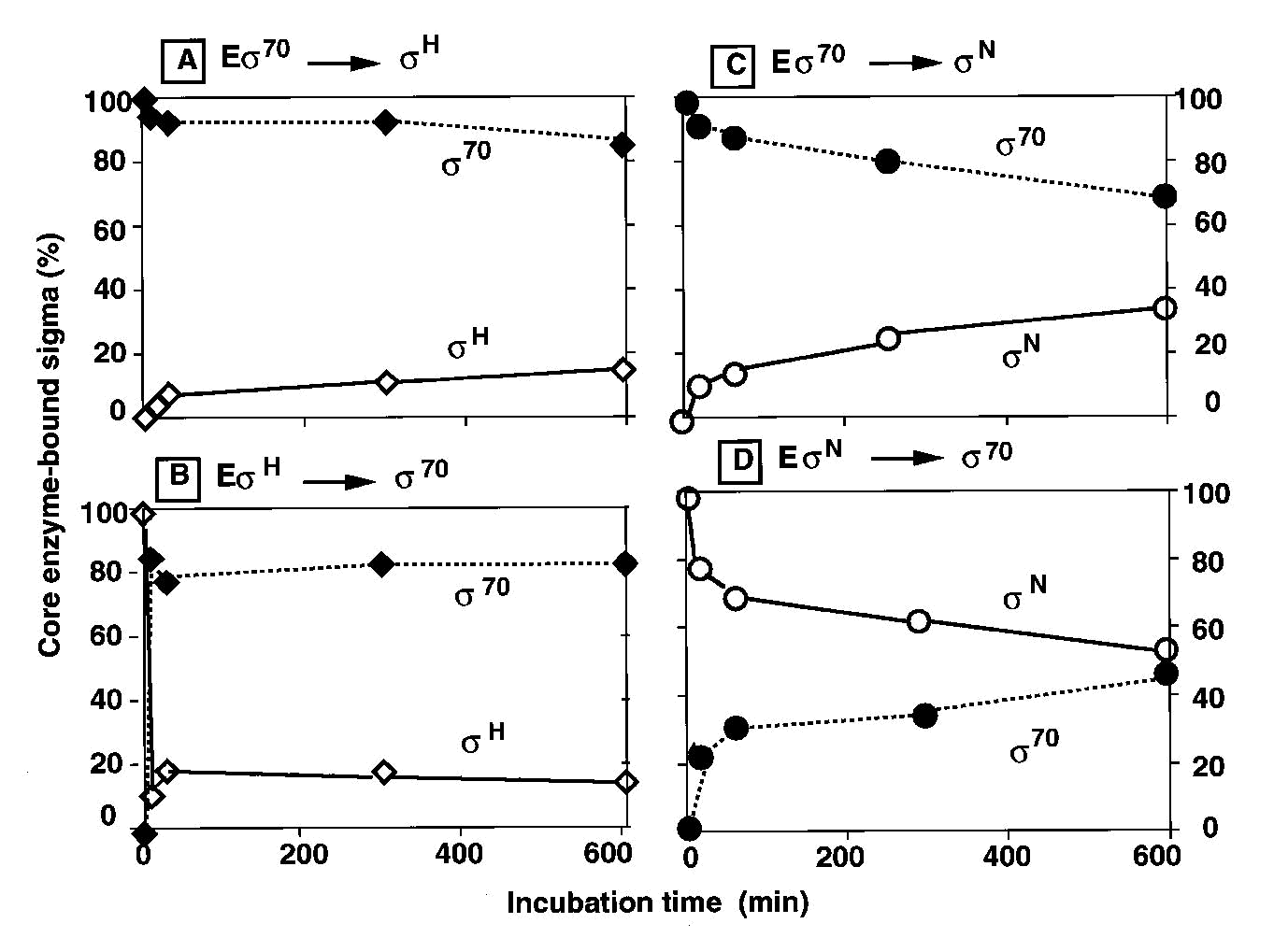
Результаты конкурентных экспериментов
с σ70
/ σH
показали, что: замещение связанного с
ферментом σ70
при добавлении σH
было мало даже после 600-минутной инкубации
(рис. 4А); связанный с кор-ферментом σH
был быстро заменен на σ70
в течение 10 минут (рис. 4В). С другой
стороны, в конкурентном эксперименте
между σ70
и σN
≈30%
σ70, свяязанного с кор-ферментом, было
заменено добавленным σN
(рис. 4C), в то время как по меньшей мере
половина σN,
связанного с кор-ферментом, оставалась
связанной даже после длительной инкубации
в течение 600 минут после добавления σ70
(рис. 4D). Все эти результаты находятся в
хорошем согласии с различиями в сродстве
связывания кор-фермента между σ70
и σH
и между σ70
и σN
(рис. 3; см. также таблицу 1). Более того,
небольшая разница в скорости замены σ
между двумя комбинациями, Eσ70
/ EσN
(30% на рис. 4C) и EσN
/ Eσ70
(50% на рис. 4D), отражает небольшую разницу
в сродстве связывания с кор-ферментом
между σ70
и σN
(см. рис. 3).
Исходя
из сродства связывания каждой субъединицы
σ, как указано выше, мы можем предсказать
эффективность замены одной σ-субъединицы,
связанной с кор-ферментом, другой
σ-субъединицей. Здесь мы протестировали
две крайние комбинации: (i) σ70
и σH,
которые имеют в 10 раз более низкое
сродство связывания с кор-ферментом,
чем σ70;
и (ii) σ70
и σN,
которые имеют сродство связывания с
кор-ферментом вплоть до σ70.
Эквимолярную смесь кор-фермента (20
пмоль) и одной субъединицы σ (20 пмоль)
инкубировали до равновесия и затем
добавляли эквимолярное количество (20
пмоль) второй субъединицы σ. В различные
моменты времени после добавления второй
σ-субъединицы измеряли концентрацию
σ-связанной с ферментом субъединицы.
Результаты конкурентных экспериментов
с σ70
/ σH
показали, что: замещение связанного с
ферментом σ70
при добавлении σH
было мало даже после 600-минутной инкубации
(рис. 4А); связанный с кор-ферментом σH
был быстро заменен на σ70
в течение 10 минут (рис. 4В). С другой
стороны, в конкурентном эксперименте
между σ70
и σN
≈30%
σ70, свяязанного с кор-ферментом, было
заменено добавленным σN
(рис. 4C), в то время как по меньшей мере
половина σN,
связанного с кор-ферментом, оставалась
связанной даже после длительной инкубации
в течение 600 минут после добавления σ70
(рис. 4D). Все эти результаты находятся в
хорошем согласии с различиями в сродстве
связывания кор-фермента между σ70
и σH
и между σ70
и σN
(рис. 3; см. также таблицу 1). Более того,
небольшая разница в скорости замены σ
между двумя комбинациями, Eσ70
/ EσN
(30% на рис. 4C) и EσN
/ Eσ70
(50% на рис. 4D), отражает небольшую разницу
в сродстве связывания с кор-ферментом
между σ70
и σN
(см. рис. 3).
Обсуждения
Различие в сродстве связывания с кор-ферментом среди семи субъединиц E.coli
Сравнение сродства связывания с кор-ферментом среди семи субъединиц σ из E.coli указывает на то, что субъединица σ70 имеет наибольшее сродство с кор-ферментом для транскрипции генов роста и «домашнего хозяйства». Разница между сродством σ70 (0,26 нМ) и σS (с самой слабой связывающей активностью (4,28 нМ)) была в 16 раз меньше (см. Таблицу 1). Эта оценка проводилась при таких условиях, что содержание функциональных молекул σ в отношении связывания с кор-ферментом было одинаковым для семи препаратов субъединиц σ. Однако, некоторые молекулы σ неактивны при связывании с кор-ферментом при проведении полного цикла транскрипции. Например, в случае субъединицы σ70 содержание транскрипционно компетентных молекул составляло ~ 50%, что измерялось уровнем синтеза матричной РНК lacUV5 в однократном анализе транскрипции. Это значение полностью функциональной субъединицы σ70 представляет собой минимум, потому что: (i) определенная доля комплексов инициации с Eσ70 становится неудавшейся до выхода промотора (уровень неудачной инициации зависит от природы промотора) (см., например, 35); (ii) некоторые транскрипционно неактивные Eσ70, как определено с помощью анализа транскрипции, направленной на промотор lacUV5, могут быть активными с промоторами, отличными от lacUV5. Точная оценка функциональных молекул более сложна для других σ-субъединиц, потому что доступные промоторы, распознаваемые этими σ-субъединицами, ограничены и мы не знаем соотношения продуктивной и абортивной инициации транскрипции in vitro, катализируемой каждым холоферментом. Однако мы позаботились о том, чтобы получить остальные шесть субъединиц σ в такой же активной форме, как и субъединица σ70, используя те же процедуры для экспрессии и очистки белка, что и для субъединицы σ70. В результате все используемые препараты были полностью активны в связывании с кор-ферментом.
Чистота семи субъединиц σ находилась в диапазоне от 90 до 98%, что определялось окрашиванием SYPRO Orange (SYPRO Orange - флуоресцентный краситель мероцианинового типа, который используется для окрашивания белка в процессе определения характеристик белка), которое столь же чувствительно, как окрашивание серебром. Загрязнение σ-препаратов анти-σ факторами Rsd (36), FlgM (37) и Rse (38,39) может привести к снижению концентрации функциональных молекул σ или интерференции взаимодействия с σ-ферментом. Однако иммуноблот-анализ (аналитический метод, используемый для определения в образце специфичных белков) препаратов σ, использованных в этом исследовании, не дал никакого сигнала против антител, анти-Rsd и анти-FlgM (данные не представлены).
Определенное значение Kd (0,26 нМ) для σ70 немного ниже, чем предыдущее (0,5–1,0 нМ) с использованием методов ВЭЖХ гель-фильтрации и флуоресценции (40). Разница может быть связана с различием в содержании функциональной субъединицы σ70 и/или кор-фермента или в условиях анализа. Joo и соавторы (41) определили значение Kd 1 нМ для σH в эксперименте насыщения σ при транскрипции in vitro, а значение 100 нМ при центрифугировании в градиенте глицерина. Константы связывания, полученные посредством гель-фильтрации и центрифугирования в градиенте глицерина, должны быть ниже, чем полученные в анализах транскрипции, из-за эффекта разбавления при отделении связанной с кор-ферментом σ от несвязанной свободной σ. Таким образом, необходимы дальнейшие технические усовершенствования для точного определения сродства связывания каждой субъединицы σ для кор-фермента, но настоящее исследование обеспечивает относительный порядок сродства связывания кор-фермента среди семи σ-субъединиц E.coli. Настоящее исследование ясно показывает, что сродство σN-субъединицы к кор-ферменту так же высоко, как и у других σ-субъединиц. Таким образом, АТФ-зависимая реакция в образовании открытого комплекса EσN-промотор может быть на стадии после связывания холофермента EσN с промотором.
Структурная основа разницы в сродстве связывания с кор-ферментом между субъединицами σ
Семейство белков σ70 имеет общую структурную организацию, за исключением σ54, которая состоит из четырех консервативных доменов (4,5). Роль каждого домена в распознавании промотора была тщательно изучена с использованием генетического, химического и физического подходов (обзор см. 4). Однако, наши знания о роли σ-структурных доменов (последовательностях) в межбелковых взаимодействиях с кор-ферментом ограничены. Мы идентифицировали поверхности взаимодействия субъединиц σ70, σN и σS на субъединицах кор-фермента после взаимодействия контактно-зависимых мест расщепления с тетраацетатом железа (S) -1- (п-бромацетамидобензил)этилендиамин (Fe-BABE) (42), связанным в различных позициях с σ-субъединицами (43–45). Результаты показали, что несколько мест вдоль этих σ-полипептидов вовлечены в контакт с β- и β’-субъединицами кор-фермента, большинство из которых расположены в консервативных местах (последовательностях) среди трех σ-субъединиц. Исследования на мутацию также показали, что субъединица σ70 содержит множественные поверхности взаимодействия с кор-ферментом (46) и, кроме того, одни и те же области и даже эквивалентные аминокислотные остатки, как в σ70, так и σH, участвуют в связывании кор-фермента. Если основные поверхности для межбелковых контактов с кор-ферментом одни и те же в семействе белков, то различия в сродстве связывания кор-фермента, наблюдаемые в этом исследовании, могут объясняться различиями в количестве поверхностей контакта или остатков контактной аминокислоты или в сродстве второстепенных поверхностей, характерных для каждой субъединицы. Эксперименты по контакт-зависимому расщеплению белка с FeBABE действительно указали на присутствие небольшого количества уникальных мест контактов субъединиц с кор-ферментом, характерных для каждой субъединицы (43–45).
Внутриклеточные уровни различных холоферментных форм рнк-полимеразы e.Coli
Внутриклеточная концентрация в E.coli W3110 (A) является самой высокой для субъединицы σ70 среди семи σ-субъединиц E.coli как в экспоненциальной, так и в стационарной фазах, а также в различных стрессовых условиях (20–22). Исходя из констант диссоциации связывания кор-фермента с внутриклеточными концентрациями, мы можем теперь оценить внутриклеточную концентрацию каждого холофермента (см. Таблицу 1). Концентрация РНК-полимеразы в E.coli W3350 составляет приблизительно 2000 молекул на клетку в экспоненциальной фазе, из которых около трети (700 молекул) остается в цитозоле (3,6). Поскольку общее количество объединенных σ-субъединиц (∼1200 молекул на клетку) больше, чем у РНК-полимеразы, не участвующей в цикле транскрипции (∼700 молекул на клетку), то большая часть РНК-полимеразы в цитозоле должна быть в форме холофермента, связанной с одной из σ-субъединиц. Например, в клетке E.coli W3110, находящейся в экспоненциальной фазе, число каждого холофермента составляет 545 молекул для Eσ70, 100 молекул для EσF и 55 молекул для EσN.
Однако считается, что некоторые из субъединиц σ70, σF и σN существуют как комплексы с анти-σ факторами (24,36). Таким образом, фактические концентрации холоферментов Eσ70, EσF и EσE в E.coli должны быть ниже уровней, оцененных выше. Например, значительная часть субъединицы σF остается в виде комплекса с FlgM (анти-σF фактором) в тех же условиях культивирования, что и используемые в этом исследовании (36,37). Активность σE регулируется с помощью RseA (регулятор σE или анти-σE фактор), который связан с внутренней мембраной и подавляет активность σE путем непосредственного взаимодействия с σE (38,39). Недавно мы идентифицировали Rsd (регулятор для σD), предполагаемую анти-σ70-субъединицу, которая вырабатывается в E.coli при переходе от экспоненциальной к стационарной фазе (25,36). Контроль функциональных форм σ-субъединиц с помощью анти-σ-факторов или σ-переключающих факторов может в определенной степени способствовать регулированию относительных уровней различных форм холофермента (6, 27, 47).