Материал: Конкуренция среди семи субъединиц Escherichia coli
Конкуренция среди семи субъединиц Escherichia coli σ: относительное сродство к основной РНК-полимеразе
Краткое содержание
В кишечной палочке Escherichia coli существует семь различных видов σ РНК-полимеразы, каждый из которых связывается с одним видом кор-фермента и тем самым направляет транскрипцию определенного набора генов. Чтобы проверить модели конкуренции σ в глобальной регуляции транскрипции генов все семь субъединиц E.coli σ были очищены и сравнены на предмет их связывающего сродства с одной и той же РНК-полимеразой. При наличии фиксированного количества σ70, основного σ для генов, связанных с ростом, уровень образования холофермента σ70 увеличивался линейно с увеличением уровня кор-фермента, давая кажущийся Кd для кор-фермента 0,26 нМ. Эксперименты по смешанному восстановлению в присутствии фиксированного количества кор-фермента и увеличивающихся количеств эквимолярной смеси всех семи субъединиц σ показали, что σ70 является самой сильной субъединицей с точки зрения связывания с кор-ферментом, за которым следуют σN, σF, σE/ σFecI, σH и σS в порядке убывания. Порядок сродства ферментов, связывающих ядро, между σ70 и σN и между σ70 и σH был подтвержден измерением замены одной связанной с ядром σ другой субъединицей σ. Взятые вместе с внутриклеточными уровнями σ, мы попытались оценить количество каждой формы холофермента в растущих клетках E.coli.
Введение
Бактериальная РНК-полимераза состоит из кор-фермента (состав субъединицы α2ββ') с каталитической активностью полимеризации РНК и одного из множества видов субъединицы σ для распознавания промотора (1–6). В Escherichia coli известны семь различных видов субъединиц σ70, σN (также называемых σ54), σS (σ38), σH (σ32), σF (σ28), σE (σ24) и σFecI, каждая из которых направляет транскрипцию определенного набора генов. Большинство генов, связанных с ростом и «домашним хозяйством», экспрессируемых в экспоненциальной фазе клеточного роста, транскрибируются холоферментом, содержащим σ70 (продукт гена rpoD), тогда как холофермент EσS необходим для транскрипции некоторых генов, специфичных для стационарной фазы (7, 8). Гены ответа на стресс транскрибируются холоферментами РНК-полимеразы, содержащими альтернативные минорные σ-субъединицы. Холофермент EσN транскрибирует гены, которые регулируются доступностью азота (9) и некоторых генов ответа на стресс (10); холофермент EσH транскрибирует гены белков теплового шока (4,10); EσF необходим для экспрессии генов жгутиков и хемотаксиса (11); холофермент EσE отвечает за транскрипцию генов для экстрацитоплазматических функций, а также за реакцию теплового шока (12–14); продукт гена fecI, который первоначально был идентифицирован как регуляторный ген для транспортной системы цитрата железа (15), теперь известен как новый член подсемейства факторов экстрацитоплазматической функции (ECF) на основе последовательности белка (далее упоминаемой как σFecI) и участвует в транскрипционной регуляции генов для экстрацитоплазматических функций (16–18). Мы очистили все семь видов субъединицы E.coli и проанализировали их специфичность распознавания для различных промоторов E.coli (18–20). Используя специфические антитела, полученные против очищенных σ-белков, мы также измерили внутриклеточные концентрации всех семи σ-субъединиц как для экспоненциальной, так и для стационарной фазы культур E.coli W3110 (A) (20–22).
Считается, что глобальная структура транскрипции генов определяется путем конкуренции между доступными субъединицами σ (23-25), и, если это так, то замена одной σ-субъединицы, связанной с кор-ферментом, на другую должна быть главным определяющим фактором в изменении глобальной структуры транскрипции (рассматривается в 26,27). Фактически, изменение глобальной транскрипционной картины при переходе фазы роста из экспоненциальной в стационарную (21,22) или при внезапном воздействии теплового удара (28,29) сопровождается изменением внутриклеточных уровней субъединиц σ. Однако в настоящее время остается неясным, могут ли изменения только в концентрациях σ объяснить изменение транскрипционной картины. Чтобы получить представление о механизме переключения σ, мы провели качественное сравнение связывающих свойств всех семи субъединиц E.coli σ для одного и того же кор-фермента. На основе этого первого систематического сравнения связывающего сродства каждой субъединицы σ для кор-фермента вместе с определением внутриклеточных концентраций каждой субъединицы σ (20-22) была сделана попытка оценить общее количество каждого холофермента в E.coli. На основании этих наблюдений оценивается модель конкуренции σ.
МАТЕРИАЛЫ И МЕТОДЫ
Сверхэкспрессия и очистка субъединиц σ
Сверхэкспрессию σ70, σN, σS, σF, σH, σE и σFecI проводили с использованием плазмид экспрессии pGEMD (30), pKES259 (31), pETF (18), pETSF (19), pET21H (S.Kusano и A.Ishihama, неопубликованные результаты), pRPOE (32) и pETFecI (20), соответственно. Штамм Escherichia coli BL21 (DE3) трансформировали соответствующей плазмидой экспрессии σ и выращивали в среде Luria-Bertani (LB), содержащей ампициллин (0,2 мг/мл). После индукции изопропил-β-D-тиогалактопиранозидом (IPTG) клетки собирали, промывали 10 мМ трис-HCl, pH 8,0, 1 мМ EDTA и 150 мМ NaCl и хранили при -80 ° C до использования. Клетки ресуспендировали в буфере для лизиса (50 мМ Трис-HCl, рН 8,0, 1 мМ ЭДТА и 0,1 мМ NaCl) и обрабатывали фенилметилсульфонилфторидом (PMSF), лизоцимом и дезоксихолатом натрия. Лизат гомогенизировали путем мягкой обработки ультразвуком, а нерастворимые вещества извлекали центрифугированием. Все семь σ-белков были извлечены из телец включения с помощью элюирующего буфера (50 мМ Трис-HCl, рН 8,0, 0,1 мМ ЭДТА, 0,1 мМ DTT и 5% глицерина), содержащего 0,5% Тритон Х-100 или 0,5 М KCl. Очистку солюбилизированных σ-субъединиц проводили без использования денатурирующих белков, по существу, как описано ранее (30).
Концентрацию белка определяли с помощью набора для анализа белка Брэдфорда (Bio-Rad), используя бычий сывороточный альбумин в качестве стандарта. Относительное содержание каждой субъединицы σ в очищенных пробах оценивали путем измерения интенсивности окрашивания Кумасси бриллиантовым синим (CBB) σ полос после отделения загрязняющих белков при помощи SDS-PAGE. Очищенные σ-субъединицы хранили замороженными при -80°С в буфере для хранения [50 мМ Трис-HCl (рН 7,6 при 4°С), 10 мМ ацетата магния, 0,1 мМ ЭДТА, 1 мМ DTT, 0,2 М KCl и 50% (v/v) глицерин] до использования.
РНК-полимеразный кор-фермент
РНК-полимеразу очищали из E.coli W3350, а кор-фермент очищали, пропуская очищенную РНК-полимеразу три раза через фосфоцеллюлозную колонку. Повторение колоночной хроматографии на фосфоцеллюлозе, по крайней мере, три раза было необходимо для полного удаления минорных субъединиц σ из кор-фермента (33,34). Уровень оставшихся субъединиц σ был дважды проверен путем тестирования транскрипционной активности in vitro, направленной специфическими промоторами, и путем иммуноокрашивания антителами, индуцированными против каждой субъединицы σ. Очищенный кор-фермент, хранили замороженным при -80°С в буфере для хранения [50 мМ Трис-HCl (рН 7,6 при 4°С), 10 мМ ацетата магния, 0,1 мМ ЭДТА, 1 мМ DTT, 0,2 М KCl и 50% (v/v глицерин] до использования.
Восстановление холоферментов
Кор-фермент и отдельный вид или комбинации различных σ-субъединиц смешивали в 50 мкл восстановительного буфера [10 мМ Трис-HCl (рН 7,6 при 4°С), 0,1 мМ DTT, ЭДТА, 0,1 мМ, 200 мМ NaCl и 5% глицерина] и инкубировали в течение 10 мин при 30°С. Аликвоты по 40 мкл подвергали гель-фильтрации через колонку Superdex 200 PC3.2 / 300 (объем слоя 0,9 мл) с системой SMART (Pharmacia, Швеция). Элюирование буфером для разведения проводили при скорости потока 40 мкл/мин при 20°С. Как холофермент, так и кор-фермент извлекались в объеме пустот (время элюирования 22–23 мин). Аликвоты каждой фракции элюирования анализировали с помощью SDS-PAGE. Гели окрашивали с помощью набора для окрашивания SYPRO Orange (Molecular Probes, США). Концентрацию белка определяли сканированием гелей с помощью FluorImager (Vistra, США). Концентрации белков РНК-полимеразы, определенные с помощью набора для окрашивания SYPRO Orange, совпадали с концентрациями, окрашенными CBB, хотя чувствительность обнаружения намного выше для окрашивания SYPRO. Уровень образования холофермента определяли путем измерения соотношения между α (репрезентативной субъединицей кор-фермента) и σ-субъединицами в пике РНК-полимеразы (холофермент плюс кор-фермент).
Результаты
Константа диссоциации образования холофермента Eσ70
Холофермент РНК-полимеразы может быть получена in vitro при смешивании очищенного кор-фермента и σ субъединицы. Для сравнения связывающих способностей различных σ субъединиц и кор-фермента, мы очистили свободные от σ субъединиц кор-ферменты пропуская очищенную РНК-полимеразу через фосфорно-целлюлозную колонку три раза. Все семь σ субъединиц были очищены от клеток E. coli, не используя денатурацию белка как в случае очистки σ70. Образование холофермента было измерено при помощи смешивания субъединиц и кор-фермента в разных пропорциях. Количество кор-ферментов, связанных с субъединицами было определено при помощи измерения молярного соотношения между сигма- и альфа-субъединицами в пике РНК-полимераз гель-фильтрационной хроматографической колонки.
Сначала
мы определили константу равновесной
диссоциации образования холофермента
Eσ70
(E представляет собой кор-фермент).
Постоянное количество (0,02 пмоль/50 мкл
или 0,4 нм) субъединицы σ70
и увеличивающееся количество кор-фермента
смешивали при 0°С и после 10-минутной
инкубации при 30°С для установления
равновесия восстановленный холофермент
Eσ70
быстро отделяли в течение 22-23 мин от
несвязанного σ70
гель-фильтрацией через колонку Superdex
200 с использованием интеллектуальной
системы (Pharmacia, Швеция). На рис. 1А показан
уровень связанного с ядром σ70,
определяемый путем измерения м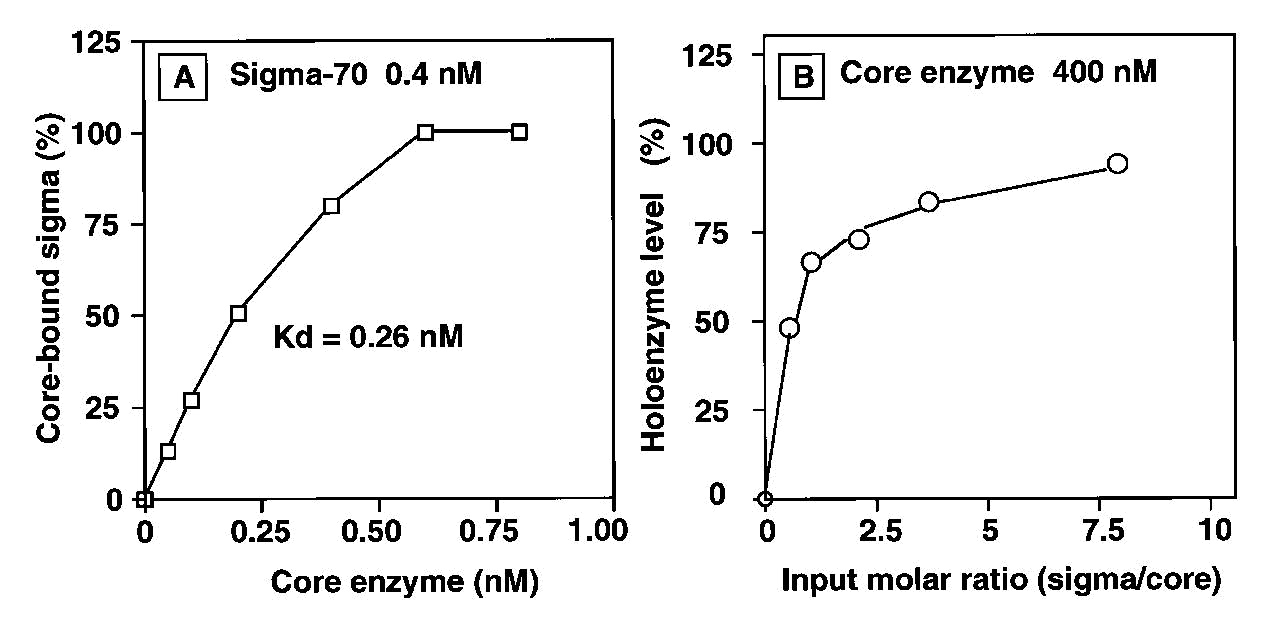 олярного
отношения между субъединицами σ70
и α в пике РНК-полимеразы. В присутствии
избыточного количества кор-фермента
практически все очищенные субъединицы
σ70
образовывали холофермент Eσ70
(см. ниже), что указывает на то, что
используемый препарат σ70
был полностью активен в связывании с
основным ферментом. Поскольку диссоциация
предварительно сформированного Eσ70
практически незначительна в этом
интервале времени, кажущаяся константа
диссоциации (Kd)
σ70
кор-фермента была оценена как ∼0,26
нм (рис. 1А). Для подтверждения высокой
активности σ70
в связывании
кор-фермента мы проводили восстановление
холофермента с увеличением количества
субъединицы σ70
в присутствии избытка (20 пмоль в 50 мкл
или 400 Нм) кор-фермента. Входящая σ70
количественно связывалась с кор-ферментом
до 10 пмоль, и почти 75% входного основного
фермента было преобразовано в холофермент
(Eσ70)
путем добавления 20 пмоль σ70
(входное
молярное отношение 1) (Рис. 1Б). При
добавлении 10-кратного молярного избытка
субъединицы σ70
весь входной кор-фермент был преобразован
в форму холофермента. Количество σ70,
необходимое для насыщения основного
фермента, было несколько больше, чем
ожидалось от значения Kd,
вероятно, потому, что некоторые из
молекул σ70
и/или кор-фермента образовывали агрегаты
при таких высоких концентрациях белка.
олярного
отношения между субъединицами σ70
и α в пике РНК-полимеразы. В присутствии
избыточного количества кор-фермента
практически все очищенные субъединицы
σ70
образовывали холофермент Eσ70
(см. ниже), что указывает на то, что
используемый препарат σ70
был полностью активен в связывании с
основным ферментом. Поскольку диссоциация
предварительно сформированного Eσ70
практически незначительна в этом
интервале времени, кажущаяся константа
диссоциации (Kd)
σ70
кор-фермента была оценена как ∼0,26
нм (рис. 1А). Для подтверждения высокой
активности σ70
в связывании
кор-фермента мы проводили восстановление
холофермента с увеличением количества
субъединицы σ70
в присутствии избытка (20 пмоль в 50 мкл
или 400 Нм) кор-фермента. Входящая σ70
количественно связывалась с кор-ферментом
до 10 пмоль, и почти 75% входного основного
фермента было преобразовано в холофермент
(Eσ70)
путем добавления 20 пмоль σ70
(входное
молярное отношение 1) (Рис. 1Б). При
добавлении 10-кратного молярного избытка
субъединицы σ70
весь входной кор-фермент был преобразован
в форму холофермента. Количество σ70,
необходимое для насыщения основного
фермента, было несколько больше, чем
ожидалось от значения Kd,
вероятно, потому, что некоторые из
молекул σ70
и/или кор-фермента образовывали агрегаты
при таких высоких концентрациях белка.
Открытие, что почти вся входная субъединица σ70 была преобразована в холофермент путем добавления избыточного количества кор-фермента (см. 1А) указывает на то, что практически все молекулы σ в используемом препарате σ70 активны, по крайней мере, в связывании с кор-ферментом. Холофермент, образованный из молекул σ70, был, однако, не полностью активен в транскрипции, как это было измерено с помощью одного раунда транскрипционного анализа in vitro, направленного промотором lacUV5, что означает, что часть неактивной субъединицы σ70 по отношению к общей транскрипции все еще активна в связывании с кор-ферментом. Таким образом, константа диссоциации (Kd) образования Eσ70 должна быть <0,26 нМ.
Соперничество между семью субъединицами за кор-фермент
Для
сравнения сродства связывания
кор-ферментов между семью σ субъединицами
E. coli мы очистили все остальные шесть
субъединиц σ от сверхэкспрессированных
клеток E. coli до кажущейся однородности
(рис. 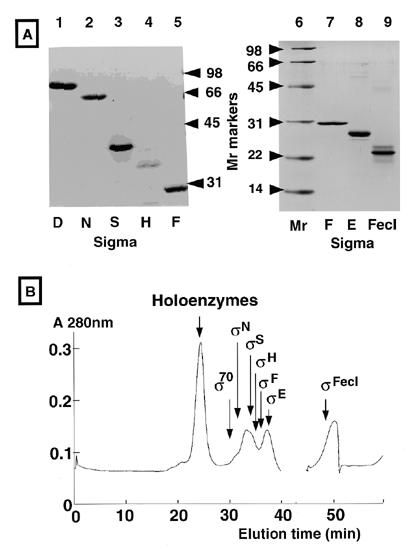 2А).
Чтобы восстановить все семь субъединиц
σ в активных формах, была предпринята
попытка очистить σ субъединицы той же
самой процедурой от сверхэкспрессированных
клеточных экстрактов, т. е. извлечение
σ белков из фракции гранул
сверхэкспрессированных клеточных
экстрактов с использованием буфера
солюбилизации, содержащего неионный
детергент, без использования ионных
детергентов. Концентрацию каждой
субъединицы σ определяли после коррекции
на чистоту (90-98%), согласно оценке SDS-PAGE
с последующим окрашиванием CBB. Так как
все эти очищенные субъединицы σ полностью
превращались в соответствующие
холоферменты путем добавления избыточных
количеств кор-фермента (данные не
показаны), используемые препараты σ
были полностью активны, по крайней мере,
в связывании с кор-ферментом.
2А).
Чтобы восстановить все семь субъединиц
σ в активных формах, была предпринята
попытка очистить σ субъединицы той же
самой процедурой от сверхэкспрессированных
клеточных экстрактов, т. е. извлечение
σ белков из фракции гранул
сверхэкспрессированных клеточных
экстрактов с использованием буфера
солюбилизации, содержащего неионный
детергент, без использования ионных
детергентов. Концентрацию каждой
субъединицы σ определяли после коррекции
на чистоту (90-98%), согласно оценке SDS-PAGE
с последующим окрашиванием CBB. Так как
все эти очищенные субъединицы σ полностью
превращались в соответствующие
холоферменты путем добавления избыточных
количеств кор-фермента (данные не
показаны), используемые препараты σ
были полностью активны, по крайней мере,
в связывании с кор-ферментом.
Используя очищенные субъединицы σ, мы сначала проанализировали кривую насыщения каждой субъединицы σ, чтобы преобразовать фиксированное количество (20 пмоль) кор-фермента в соответствующий холофермент. При входном молярном соотношении 1 более 80% входного кор-фермента было преобразовано в холофермент для пяти субъединиц σ: σ70, σN, σF, σE и σFecI, а 60-65% входного кор-фермента было преобразовано в холофермент для σS и σH (данные не показаны). Для насыщения σ входного кор-фермента требовалось более высокой концентрации как для σS, так и для σH. Входной кор-фермент насыщали добавлением 2-кратного молярного избытка σ даже для σS и σH, со слабым сродством связывания. Аналогичный порядок активности σ был получен при определении уровня функционального холофермента путем измерения кривой насыщения σ с использованием транскрипционных тестов in vitro, направленных специфическими промоторами для каждой субъединицы σ (данные не показаны). Однако при наличии единичных σ-добавок было трудно определить небольшое различие в сродстве связывания кор-фермента между семью σ-субъединицами.
Д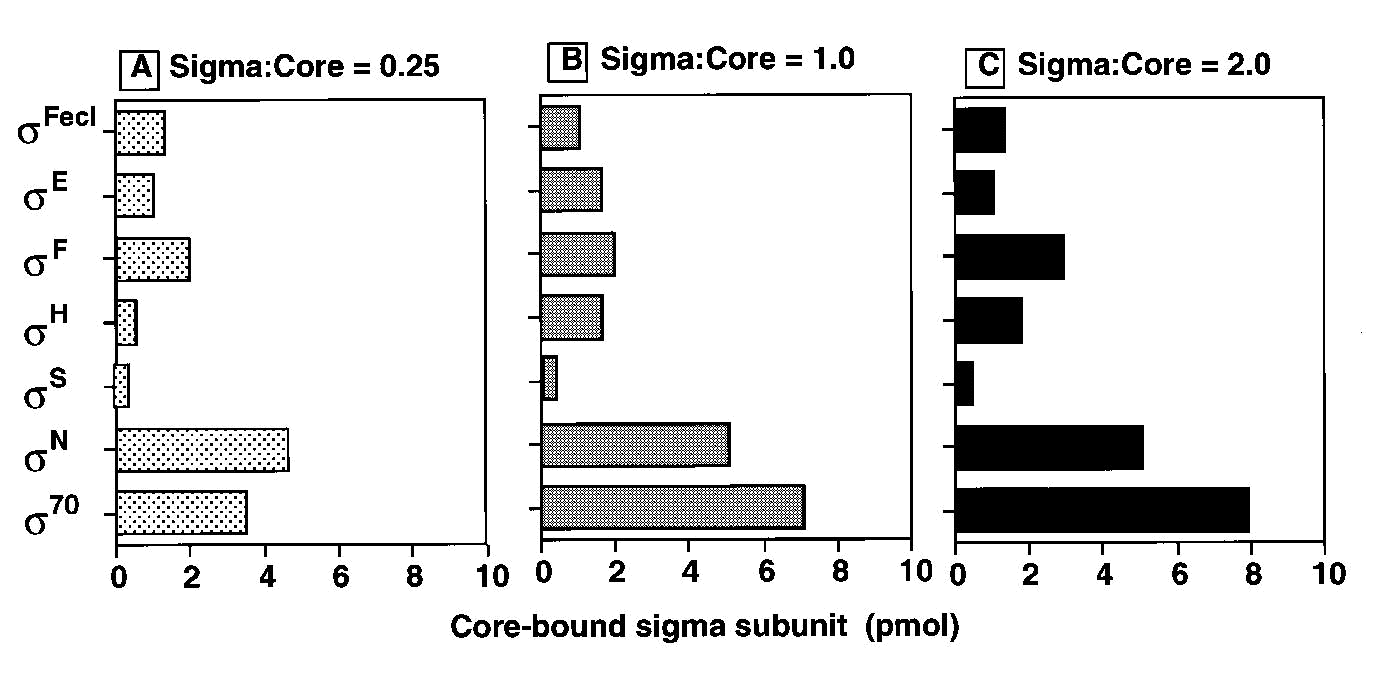 ля
того чтобы измерить относительное
сродство связывания кор-фермента между
семью субъединицами σ, мы провели
смешанный эксперимент восстановления
в присутствии всех семи субъединиц σ в
одной и той же реакционной смеси. К 20
пмоль кор-фермента добавляли увеличивающиеся
количества эквимолярной смеси всех
семи субъединиц σ, а субъединицы σ
фракционировали на связанные с
кор-ферментом и несвязанные фракции
методом гель-фильтрационной колоночной
хроматографии (рис. 2B). После измерения
молярных соотношений между α-субъединицей
и каждой σ-субъединицей в пике холофермента
определяли основные связанные с ферментом
σ-субъединицы. Почти 68% кор-фермента
было преобразовано в холоферменты при
входном молярном отношении 0,25 для каждой
субъединицы σ (или 1,75 для комбинированных
субъединиц σ) (рис. 3А) и >90% входного
кор-фермента связывалось с одной из
семи субъединиц σ при входном молярном
отношении 1,0 для каждой субъединицы σ
(или 7,0 для комбинированных субъединиц
σ) (рис. 3Б). Входной фермент ядра насыщался
одной из субъединиц σ при входном
молярном отношении 2,0 для каждой
субъединицы σ (или 14 для комбинированных
субъединиц σ) (рис. 3С). Однако
кор-фермент-связанная фракция существенно
отличалась среди семи субъединиц σ. При
низкой концентрации σ (или уровне
насыщения 60-70%) σN
проявлял сродство столь же высокое, как
и субъединица σ70,
а комбинированный уровень EσN
и Eσ70
достигал 60% от общего количества
холоферментов. Уровень холоферментов
был почти одинаковым среди EσF,
EσFecI
и
EσE,
каждый из которых составлял 14, 10 и 8%
соответственно, в то время как количество
EσH
составлял <1% от общего количества
холоферментов. Уровень образования EσS
был самым низким при использованных
условиях восстановления. Фракции,
связанные с кор-ферментом, увеличивались
параллельно для всех семи субъединиц
σ одновременно с увеличением входных
субъединиц σ до фиксированного количества
основного фермента (рис. 3B и C).
ля
того чтобы измерить относительное
сродство связывания кор-фермента между
семью субъединицами σ, мы провели
смешанный эксперимент восстановления
в присутствии всех семи субъединиц σ в
одной и той же реакционной смеси. К 20
пмоль кор-фермента добавляли увеличивающиеся
количества эквимолярной смеси всех
семи субъединиц σ, а субъединицы σ
фракционировали на связанные с
кор-ферментом и несвязанные фракции
методом гель-фильтрационной колоночной
хроматографии (рис. 2B). После измерения
молярных соотношений между α-субъединицей
и каждой σ-субъединицей в пике холофермента
определяли основные связанные с ферментом
σ-субъединицы. Почти 68% кор-фермента
было преобразовано в холоферменты при
входном молярном отношении 0,25 для каждой
субъединицы σ (или 1,75 для комбинированных
субъединиц σ) (рис. 3А) и >90% входного
кор-фермента связывалось с одной из
семи субъединиц σ при входном молярном
отношении 1,0 для каждой субъединицы σ
(или 7,0 для комбинированных субъединиц
σ) (рис. 3Б). Входной фермент ядра насыщался
одной из субъединиц σ при входном
молярном отношении 2,0 для каждой
субъединицы σ (или 14 для комбинированных
субъединиц σ) (рис. 3С). Однако
кор-фермент-связанная фракция существенно
отличалась среди семи субъединиц σ. При
низкой концентрации σ (или уровне
насыщения 60-70%) σN
проявлял сродство столь же высокое, как
и субъединица σ70,
а комбинированный уровень EσN
и Eσ70
достигал 60% от общего количества
холоферментов. Уровень холоферментов
был почти одинаковым среди EσF,
EσFecI
и
EσE,
каждый из которых составлял 14, 10 и 8%
соответственно, в то время как количество
EσH
составлял <1% от общего количества
холоферментов. Уровень образования EσS
был самым низким при использованных
условиях восстановления. Фракции,
связанные с кор-ферментом, увеличивались
параллельно для всех семи субъединиц
σ одновременно с увеличением входных
субъединиц σ до фиксированного количества
основного фермента (рис. 3B и C).