Материал: Комплексные соединения
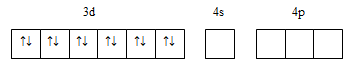
При образовании комплекса с ионами Cl-, сравнительно слабо взаимодействующими с ионами Ni2+ (ибо ион Cl- имеет большой радиус), электронные пары поступают на
орбитали следующего электронного уровня:
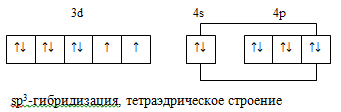
С молекулами NH3 ион Ni2+ взаимодействует сильнее, чем с ионами Cl-, поэтому он присоединяет 6 молекул NH3, образуя ион [Ni(NH3)6]2+, имеющий
следующее строение:
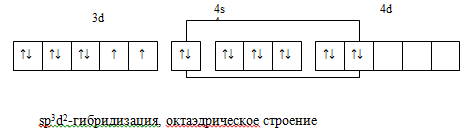
Как и в предыдущем примере, в этом комплексе имеются неспаренные электроны, следовательно, оба комплекса обладают магнитными свойствами, т.е. они парамагнитны.
Еще более сильно ион Ni2+ взаимодействует с ионами CN-.
В этом случае происходит спаривание двух d-электронов иона Ni2+, и образовавшиеся свободная
ячейка заполняется электронной парой иона CN-:
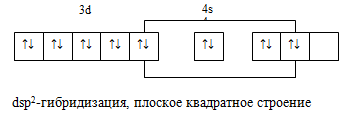
Поскольку в этом комплексе нет неспаренных электронов, то он не обладает магнитными свойствами. т.е. он диамагнитен.
Из рассмотренных примеров видно, что гибридизация с участием d-орбиталей может быть двух видов: с использованием внешних d-орбиталей (4d в случае [Ni(NH3)6]2+) и с использованием внутренних d-орбиталей (3d для [Ni(СN)4]2-).
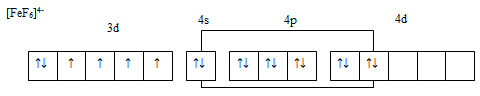
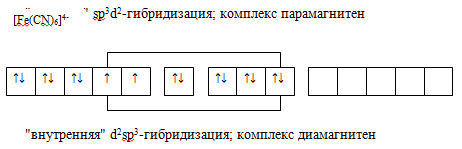
В случае "внешней" гибридизации связь лигандов с комплексообразователями слабее, чем при наличии "внутренней" гибридизации. Поэтому один из лигандов сравнительно легко может отделиться от комплекса, предоставив свое место другой частице. например, комплекс [Fe(NH3)6]2+, в котором имеет место "внешняя" гибридизация, гораздо более реакционноспособная, чем [Fe(СN)6]2-, где гибридизация "внутренняя".
Примеры "внешней" и "внутренней" гибридизации:
В заключение следует отметить огромное значение комплексных соединений, чем тех, которые называются простыми.
Минералы, окружающей нас природы, а также сложнейшие химические вещества животного организма и растений в большинстве своем представляют собой комплексные соединения. Например, как отмечалось выше, гемоглобин (красящее вещество крови, переносчик кислорода) является комплексным соединением железа, а хлорофилл (зеленый пигмент растений, катализирующий процесс ассимиляции СО2) - это комплексное соединение магния.
Комплексные соединения широко применяются в современной химии и химической технологии. Ими пользуются для получения химически чистых металлов: платины, золота, родия, индия, урана, церия, циркония и др. Их применяют в аналитической химии для быстрого обнаружения того или иного элемента и количественного отделения его от других.
Комплексные соединения имеют большое значение не только для практической
химии и технологии, но и теоретической точки зрения. Изучение их строения и
свойств заставило пересмотреть некоторые уже устоявшиеся понятия в химии и
привело к открытию новых закономерностей.
Библиографический список
1. Карапетьянц М. Х. , Дракин С.И. Общая и неорганическая химия. - М.: Химия, 1993. - 590 с.
. Ахметов Н.С. Общая и неорганическая химия. Учебник для вузов. - М.: Высш. шк., 2001. -679 с.
. Угай Я.А. Общая и неорганическая химия. - М.: Высш. шк., 1997. 527 с.
. Дроздов Д.А, Зломанов В.П., Мазо Г.Н., Спиридонов Ф.М. Неорганическая химия. В 3-х томах. Т.2. Химия непереходных элементов. / Под ред. Ю.Д. Третьякова -М.: Изд. "Академия", 2004, 368с.
. Тамм И.Е., Третьяков Ю.Д. Неорганическая химия: В 3-х томах, Т.1. Физико-химические основы неорганической химии. Учебник для студентов ВУЗв / Под ред. Ю.Д. Третьякова -М.: Изд. "Академия", 2004, 240с.
. Коржуков Н.Г. Общая и неорганическая химия. Учеб. Пособие. /Под ред В.И. Деляна-М.: Изд. МИСИС: ИНФРА-М, 2004, 512с.
. Ершов Ю.А., Попков В.А., Берлянд А.С., Книжник А.З. Общая химия. Биофизичческая химия. Химия биогенных элементов. Учебник для ВУЗов. /Под ред. Ю.А. Ершова. 3-е изд., -М.: Интеграл-Прес, 2007. 728 с.
. Глинка Н.Л. Общая химия. Учебное пособие для ВУЗов. Изд. 30-е исправленное./ Под ред. А.И. Ермакова. -М.: Интеграл-Пресс, 2007, 728 с.
. Черных, М.М. Овчаренко. Тяжелые металлы и радионуклиды в биогеоцинозах. -М.: Агроконсалт, , 2004.
. Н.В. Гусакова Химия окружающей среды. -Ростов-на-Дону, Феникс, 2004.
. Балецкая Л.Г. Неорганическая химия. -Ростов-на-Дону, Феникс, 2005.
. М. Хенце, П. Армоэс, Й. Ля-кур-янсен, Э. Арван. Очистка сточных вод. -М.: Мир, 2006.
. Коровин Н.В. Общая химия. - М.: Высш. шк., 1998. -558 с.
. Петрова В.В. и др. Обзор свойств химических элементов и их соединений. Учебное пособие по курсу "Химия в микроэлектронике". - М.: Изд-во МИЭТ, 1993. -108 с.
. Харин А.Н., Катаева Н.А., Харина Л.Т. Курс химии. - М.: Высш. шк., 1983. -511 с.