Материал: Комплексные соединения
Комплексные соединения
Комплексные соединения
Основные положения координационной теории
Из предыдущего курса мы помним, что силы притяжения существуют не только между атомами, но и между молекулами. Взаимодействие молекул приводит к образованию других, более сложных молекул. Например, газообразные вещества при соответствующих условиях переходят в жидкое и твердое агрегатное состояния. Любое вещество в какой-то мере растворимо в другом, что свидетельствует об их взаимодействии. Во всех случаях наблюдается взаимная координация взаимодействующих частиц, которую можно определить как комплексообразование.
Первые комплексные соединения были синтезированы в середине прошлого века. В 1893 году швейцарский химик Вернер опубликовал координационную теорию. Большой вклад в развитие химии комплексных соединений внесли русские ученые: Л. А. Чугаев и другие.
Для того чтобы наглядно представить себе механизм образования комплексных соединений, рассмотрим следующий пример.
Если к раствору иодида калия прилить раствор хлорида ртути (II), то в результате реакции обмена выпадает осадок иодида ртути (II) красного цвета:
2
+ 2KI = ↓HgI2 + 2KCl.
Казалось бы, на этом реакция должна закончиться. Однако, если прилить
избыток иодида калия, то осадок иодида ртути растворится и снова образуется бесцветный
раствор, если этот раствор осторожно упарить, то можно получить желтоватые
кристаллы состава К2HgI4. Очевидно HgI2 может
реагировать с KI по следующему уравнению:
HgI2 + 2KI = К2[HgI4].
Рассмотренное соединение К2[HgI4] диссоциирует следующим образом:
К2HgI4 = 2К+ + [HgI4]2-.
Таким образом, в состав соединения К2[HgI4] входят ионы [HgI4]2-, которые, в отличие от образующих их простых ионов Hg2+ и I-, были названы комплексными (сложными) ионами.
Итак, комплексными соединениями называют молекулярные соединения, в состав которых входят сложные (комплексные) ионы, способные к существованию, как в кристалле, так и в растворе.
По теории Вернера в структуре комплексных соединений различают
координационную (внутреннюю) сферу, состоящую из центральной частицы
(комплексообразователя) и координируемых вокруг него окружающих его лигандов
(ионы, молекулы). Ионы, находящиеся за пределами координационной сферы,
образуют внешнюю сферу комплекса. В формулах комплексных соединений внутренняя
координационная сфера заключается в квадратные скобки:

Центральный атом координирует лиганды, геометрически правильно располагая их в пространстве. Поэтому комплексные соединения часто называют координационными.
Число лигандов в комплексе называется координационным числом (К.Ч.) комплексообразователя. Для рассмотренного комплексного соединения К.Ч.=4 оно показывает число мест во внутренней сфере комплексного соединения или число мест вокруг комплексообразователя, на которых могут разместиться лиганды. К.Ч. бывает от 2 до 12. Часто встречаются комплексные соединения с К.Ч. = 4 или 6, затем 8 или 2.
Заряд комплексного иона численно равен суммарному заряду внешней сферы и противоположен ей по знаку. Во внешней сфере комплексного соединения К3[Fe(CN)6] находятся три положительно заряженных иона калия. Следовательно, сам комплексный ион имеет три отрицательных заряда. Заряд комплексного иона равен сумме зарядов комплексообразователя и сумме зарядов лигандов. Отсюда в K3[Fe(CN)6] степень окисления железа равна +3.
Комплексообразователями могут быть:
а) положительные ионы неметаллов: Si+4, P+5, B+3, H2[SiF6], K[PF6] ; и др.
б) ионы металлов, преимущественно d-элементов: Cu+2, Ag+, Au+3, Cr+3, Pt+4;
в) нейтральные атомы: Fe, Ni;
Лигандами могут быть:
а) нейтральные молекулы: CO, NH3, H2O, NO, N2H4 (гидразин), C6H5N (пиридин), NH2 - CH2 - CH2 - NH2 (этилендиамин);
б) отрицательные ионы: F-, CI-, Br-, OH- (гидроксо), CN- (циано), CNS- (родано), NO2- (нитро), O2- (оксо), S2- (серо), CIO4- (перхлорато).
Лиганды, занимающие во внутренней координационной сфере одно место, называются монодентатными, а два или несколько мест - соответственно би- и полидентатными.
Примерами бидентптных лигандов могут служить оксалат-ион С2О42- и молекула этилендиамина NH2-CH2-CH2-NH2.
Номенклатура комплексных соединений
Многие комплексные соединения до сих пор сохранили свои исторические названия, связанные с их цветом или именем ученого, их синтезировавшего. В настоящее время принципы наименования комплексных соединений утверждены комиссией по номенклатуре IUPAC. Ниже приведены основные правила, заимствованные из материалов этой комиссии, с учетом особенностей номенклатуры соединений, принятой в русском языке.
Порядок перечисления ионов. Первым называют анион, затем катион:
[Ag(NH3)2]Cl - хлорид диамминсеребра (I),2[CuCl3] - трихлорокупрат (I) калия.
При этом в названии комплексного аниона употребляется корень латинского наименования комплексообразователя, а в названии комплексного катиона - его русское наименование в родительном падеже:
K3[Fe(CN)6] - гексацианоферрат (III) калия,
[Fе(NН3)6]СI3 - хлорид гексаамминжелеза (III).
Порядок перечисления лигандов. Лиганды в комплексе перечисляются в следующем порядке: а) анионные; б) нейтральные; в) катионные без разделения друг от друга дефисом. Анионы перечисляются в порядке О2-, ОН-, простые анионы, полиатомные анионы и, наконец, органические анионы в алфавитном порядке: [PtEn(NH3)2(NO2)Cl]SO4 сульфатхлоронитродиамминэтилендиамин платины (IV)
Окончания координационных групп. Нейтральные группы называются так же, как молекулы. Исключениями являются аква (H2O) и аммин (NH3). К отрицательно заряженным ионам прибавляют соединительную гласную "о": [Co(NH3)6][Fe(CN)6]- -гексацианоферрат(IV)гексаамминкобальта(III)Приставки, указывающие число лигандов: ди-, три-, тетра-, пента-, гекса- и т.д., используются перед простыми лигандами (дихлоро-, триоксалато-, тетраоксо-, гексагидроксо-): K4[SnF8] - октофторостаннат (IV) калия.
Приставки "бис", "трис" используют перед лигандами со сложным названием, где в самом названии лиганда уже имеются приставки (моно-, ди- и т.д.). Названия таких лигандов заключают в скобки: [Fе(Еn)3]СI3 - хлорид трис(этилендиамин)железа (III).
Окончания названий комплексов. Характерным окончанием для анионных комплексов является "ат" или "овая", если называется кислота. Для катионных и нейтральных комплексов типичных окончаний нет: K3[Co(CN)6] - гексацианокобальтат (III) калия, H2[Pt(CN)6] - гексацианоплатиновая (IV) кислота, или гексацианоплатинат (IV) водорода.
Состояние окисления. Степень окисления комплексообразователя обозначается цифрами в скобках после его названия. [Сu (NН3)2]ОН - гидроксид диамминмеди (I).
При названии электронейтральных комплексных соединений степень окисления комплексообразователя не указывается. Например,
[Co(NH3)3(NO2)3] - тринитритотриамминкобальт,
[Pt(NH3)2Cl4] - тетрахлородиамминплатина.
Классификация комплексных соединений
Применяющиеся системы классификации комплексных соединений основываются на различных принципах.
По принадлежности к определенному классу соединений различают:
комплексные кислоты - H2[SiF6], H[AuCI4];
комплексные основания - [Ag(NH3)2]OH, [Со(Еn)3](ОН)3;
комплексные соли - K2[HgI4], [Сг(Н2O)6]СI3.
По природе лигандов. Если лигандом является вода, комплексы называются аквакомплексами: [Со(Н2О)6]SO4, [Сu(Н2O)4](NO3)2. Комплексы, образованные аммиаком, - амминокомплексы: [Ag(NH3)2]Cl, [Cu(NH3)4]SO4, [Со(NН3)6]СI2. . Соединения с ОН- - группами в виде лигандов называют гидроксокомплексами, например, К3[АI(ОН)6].Оксалатные, карбонатные, цианидные, галогенидные и другие комплексы, содержащие в качестве лигандов анионы различных кислот, называют ацидокомплексами. Например, K4[Fe(CN)6] и K2[HgI4] - цианидный и иодидный ацидокомплексы
По знаку заряда комплекса различают:
катионные комплексы: [Со(NН3)6]СI3, [Zn(NH3)4]CI2;
анионные комплексы: Li[AlH4], К2[Ве(СО3)2];
нейтральные комплексы: [Pt(NH3)2Cl2], [Co(NH3)3Cl3].
Нейтральные комплексы не имеют внешней сферы. Более сложными являются бикомплексы, состоящие из комплексных катионов и анионов, например, [Co(NH3)6][Fe(CN)6].
Циклические или хелатные (клешневидные) компелексные соединения содержат
би- или полидентатный лиганд, который образует с центральным атомом замкнутый
цикл, как бы захватывая его подобно клешням рака, благодаря чему эти соединения
отличаются большой прочностью.
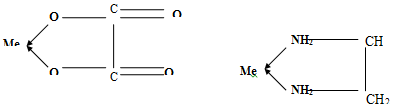
В этих комплексах символом Ме обозначен атом комплексообразователя, а стрелкой - координационная связь. Примером может служить оксалатный комплекс железа (III) [Fe(C2O4)2]2+.
Особой и очень важной группой хелатов являются так называемые
внутрикомплексные соединения, в которых один и тот же лиганд связан с
комплексообразователем как обычной, так и донорно-акцепторной связью. Примером
может служить открытый Л.А. чугаевым в 1905 г. диметилглиоксимат никеля:
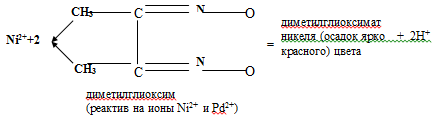
Из формулы диметилглиоксимата никеля
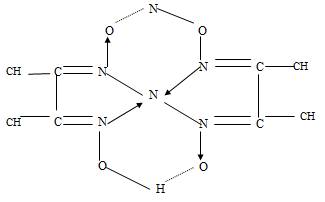
следует, что вокруг никеля координированы только атомы азота и существуют пятичленные циклы. Кроме того, благодаря наличию водородных связей образуются еще две циклические группировки, увеличивающие устойчивость молекул.
Важнейшими представителями внутрикомплексных соединений являются природные вещества гемоглобин и хлорофилл. Комплексообразователем гемоглобина является ион железа Fe2+. К гемоглобину могут присоединяться молекулы кислорода О2 и оксида углерода СО; в первом случае образуется оксигемоглобин, во втором - карбоксигемоглобин.
В легких гемоглобин присоединяет кислород воздуха и в виде оксигемоглобина переносит его до самых мелких кровеносных капилляров. Так как парциальное давление кислорода в этих капиллярах гораздо меньше, чем в легких, оксигемоглобин распадается на гемоглобин и кислород. Последний потом используется для осуществления различных ферментативных процессов окисления органических веществ.
Устойчивость карбоксигемоглобина гораздо выше устойчивости оксигемоглобина, чем и объясняется ядовитость оксида углерода СО. При вдыхании воздуха, содержащего СО, в легких образуется не оксигемоглобин, а более устойчивый карбоксигемоглобин. Тем самым прекращается снабжение клеток кислородом, необходимым для протекания процессов жизнедеятельности.
Строение хлорофилла с точки зрения химии комплексных соединений подобно строению гемоглобина, однако комплексообразователем в хлорофилле является ион Mg2+. Хлорофилл играет важнейшую роль в процессах фотосинтеза, протекающих во всех зеленых растениях.
Устойчивость комплексных соединений
Константа нестойкости. Двойные соли
При растворении в воде комплексные соединения обычно распадаются так, что
внутренняя сфера ведет себя как единое целое:
[Ag(NH3)2]Cl![]() [Ag(NH3)2]+ +Cl-
[Ag(NH3)2]+ +Cl-
Наряду с этим процессом, хоть и в незначительной степени, происходит
диссоциация внутренней сферы комплекса (т.е. процесс обратим):
[Ag(NH3)2]+ ![]() Ag+ + NH3
Ag+ + NH3
[Ag(CN)2]- ![]() Ag+ + 2CN-.
Ag+ + 2CN-.
Применив к этим равновесиям выражение для константы ионизации, получим соотношение, называемое константой нестойкости комплекса:
![]() ;
;
![]()
комплексный соединение координационный лиганд
Константа
нестойкости комплексного иона Кн характеризует прочность (или
устойчивость) внутренней сферы комплексного соединения: чем меньше Кн,
тем более устойчив комплексный ион. В приведенных примерах комплексный ион [Ag(CN)2]-
более устойчив, чем комплексный ион [Ag(NH3)2]+, поэтому второй ион может
быть легко разрушен за счет образования первого иона:
[Ag(NH3)2]+ + 2СN-
= [Ag(CN)2]- + 2NH3.
Двойные
соли также относятся к числу комплексных соединений, ибо принципиального
различия между двойными солями и комплексными соединениями нет. Отличаются они
лишь диссоциацией комплексного иона: у первых она практически полная. у вторых
- незначительная. Например, двойной хлорид калия и меди 2KCl ∙ CuCl2 ∙ 2H2O
можно рассматривать как комплексное соединение К2[CuCl4] ∙ 2H2O
диссоциация которого происходит следующим образом:
К2[CuCl4] ∙ 2H2O = 2К+ + [CuCl4]2- + 2H2O;
[CuCl4]2- ↔ Cu2+ + 4Cl-.
В
данном случае комплексный ион устойчив только в концентрированных растворах, при
комнатной температуре константа нестойкости этого иона велика.
1.5 Химическая связь в комплексных соединениях
Согласно теории валентных связей, при образовании комплексов возникают
донорно-акцепторные связи за счет неподеленных электронных пар лигандов Эти
электронные пары поступают в общее пользование лиганда и центрального иона,
занимая при этом свободные гибридные орбитали комплексообразователя. например:
Cu+ + 2NH3 = [Cu(NH3)2]4;2+
+ 4NH3 = [Zn(NH3)4]2+.
Ионы Cu+ и Zn2+ имеют законченный третий электронный
уровень, а в следующем, четвертом, имеются свободные s- и p-орбитали.
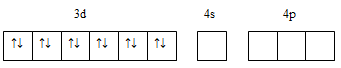
В комплексе [Cu(NH3)2]4 две электронные
пары молекул NH3 занимают две sp-гибридные орбитали, следовательно,
образуется линейная структура комплекса:
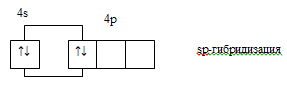
В комплексе [Zn(NH3)4]2+ четыре электронные пары
занимают четыре sp3-гибридные орбитали, следовательно,
комплекс имеет тетраэдрическое строение:
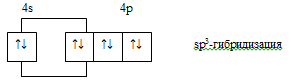
При образовании донорно-акцепторных связей в комплексах могут
использоваться не только s- и
р-орбитали, но и d-орбитали. В этом
случае возникает гибридизация с участием d-орбиталей (табл.1)
Таблица 1

Вид гибридизации и структура комплексов определяются в основном
электронным строением центрального иона, а также зависят от природы лигандов.
Например, ион Ni2+ имеет конфигурацию внешнего электронного уровня d8: