Материал: Изменение состава периферической крови под воздействием физических нагрузок
лимфоциты 30%;
моноциты - от 2 до 10%;
эозинофиллы - 5%;
базофиллы до 1%;
нейтрофиллы от 40 до 70%.
Показателем номер три были взяты тромбоциты или кровяные пластинки (бляшки Биццоцеро). Эти компоненты крови неправильной, округлой формы, имеющие длину 1-4 мкм, и толщину 0,5-0,75 мкм. Содержание их в крови состовляет 180-320х109/л. Образуются в красном костном мозге путем отщепления части протоплазмы от мегакариоцитов. От 1 мегакариоцита образуется 3-4 тысячи тромбоцитов. 2/3 тромбоцитов циркулируют в крови, остальные - депонированы в селезенке. Тромбоциты способны фагоцитировать небиологические инородные тела, вирусы, иммунные комплексы, таким образом, участвуя в неспецифической защитной системе организма. Продолжительность пребывания их в крови 5-11 дней, после чего они разрушаются в печени, легких и селезенке. Одной из основных функций тромбоцитов является их участие в процессе свертывания крови. При разрушении тромбоцитов высвобождаются адреналин, норадреналин, серотонин, а также вещества вызывающие адгезию и агрегацию [9].
Исследуя показатели крови, необходимо также упомянуть о таком показателе как концентрация гемоглобина. Одной из важнейших функций крови является перенос поглощаемого в легких кислорода к органам и тканям и транспорт углекислого газа в обратном направлении. Ключевую роль в этом процессе играют эритроциты, благодаря содержанию в них красного кровяного пигмента - гемоглобина. По химической природе это хромопротеид, состоящий из белка глобина и простетической группы гема, который в свою очередь представлен протопорфирином, в центре которого расположен атом железа.
Функции гемоглобина:
транспорт О2 (в виде оксигемоглобина HHbO2);
транспорт углекислого газа;
участие в поддержании кислотно-щелочного состояния [10].
.3 Изменения исследуемых показателей после физической нагрузки, их
причины и закономерности
Наибольшее количество исследований о влиянии физической нагрузки на периферическую кровь было посвящено изучению лейкоцитов. W. Winternitz (1893), Е. Willebrand (1903) установили появление лейкоцитоза после мышечной деятельности [11, 12]. Для объяснения этого было высказано несколько предположений. Согласно одному из них, увеличение количества лейкоцитов обусловлено сгущением крови, происходящим отчасти вследствие усиленного потоотделения, но в основном за счет перехода жидкой части плазмы в работающие мышцы. Усиление сердечной деятельности и ускорение циркуляции крови также приводит к поступлению в кровь пристеночных лейкоцитов и вымыванию их из внутренних органов в ток крови.
Лейкоцитоз, наступающий после мышечной работы называется миогенным лейкоцитозом. Он наступает вследствие интоксикации организма продуктами обмена веществ, в частности белкового, а увеличение количества лейкоцитов способствует обезвреживанию этих продуктов. Одним из подтверждений этого можно высказать то, что степень увеличения количества лейкоцитов зависит от мощности работы.
Первым исследователем, установившим закономерности изменения количества лейкоцитов под непосредственным влиянием физической нагрузки, был А. П. Егоров (1926). Он впервые дал качественную и количественную характеристику изменениям лейкоцитов и выделил 3 фазы миогенного лейкоцитоза. 1-я фаза (лимфоцитарная) возникает после относительно небольшой работы. Она характеризуется незначительным лейкоцитозом (8 - 12х109/л), снижением относительного количества нейтрофилов, абсолютным и относительным увеличением количества лимфоцитов и относительным уменьшением количества эозинофилов. Вторая фаза (нейтрофильная) появляется после сравнительно большой работы. Она характеризуется большим увеличением количества лейкоцитов (от 16 до 18x109/л), по сравнению с первой фазой, резким увеличением количества нейтрофилов со сдвигом влево, уменьшением количества лимфоцитов и эозинофилов. 3-я фаза (интоксикационная) протекает по 2 типам: регенеративному и дегенеративному. При регенеративном типе происходит значительное увеличение количества лейкоцитов (от 20 до 50x109/л), увеличение количества нейтрофилов со сдвигом влево, уменьшение количества лимфоцитов (1 %), полное исчезновение эозинофилов. Дегенеративный тип характеризуется такими же изменениями морфологического состава, как и регенеративный, но с менее выраженным лейкоцитозом (10-15x109/л), более резким сдвигом нейтрофилов влево, абсолютной лимфо- и эозинопенией и появлением дегенеративных форм. Интоксикационная фаза миогенного лейкоцитоза свидетельствует о крайней чрезмерности нагрузки [13].
Сущность возникновения 1-й фазы заключается в перераспределении лейкоцитов в кровеносном русле и их вымывании из селезенки. Причиной же 2-й и 3-й фаз является выход лейкоцитов из костного мозга, что доказывается появлением юных форм лейкоцитов и появлением дегенеративных форм лейкоцитов. Однако не всегда лимфоцитарная фаза переходит в нейтрофильную. Так, у хорошо физически подготовленных людей даже после значительной нагрузки такого перехода не наблюдается. Это свидетельствует о достаточно высокой приспособленности человека к выполнению нагрузки. Усиление кроветворной функции костного мозга, как следствие физической нагрузки, было подтверждено группой советских учёных под руководством В. А. Иванова (1950). Ими было установлено усиление лейкопоэза у лыжников после пробега [14].
Таким образом, появление в периферической крови лимфоцитарной фазы миогенного лейкоцитоза в ответ на значительную нагрузку является положительным прогностическим признаком высокого функционального состояния человека, и наоборот, появление нейтрофильной или интоксикационной фазы после относительно небольшой нагрузки свидетельствует о его недостаточной подготовленности к выполнению работы. В то же время отсутствие изменений в ответ на физическую нагрузку относительного количества форменных элементов в лейкоцитарной формуле следует считать либо признаком плохой приспособляемости организма к физическим нагрузкам, либо чрезмерностью физического напряжения для данного индивидуума [15, 16].
Однако картину изменений периферической крови нельзя считать полной без учета количества эритроцитов и гемоглобина. Использование этих показателей для оценки воздействия физической нагрузки на систему крови традиционно. Такие исследования проводились многими авторами. При обследовании спортсменов разных видов спорта ими установлено, что под влиянием физической нагрузки происходит увеличение количества эритроцитов и гемоглобина. Некоторые авторы считают, что увеличение этих показателей происходит за счет выхода крови из депо, а также сгущения крови из-за дегидратации. Эта реакция расценивается как показатель хорошей подготовленности человека к физической нагрузке. Наряду с данными о повышении количества эритроцитов и гемоглобина в крови при физической нагрузке, в литературе имеются сведения об их уменьшении. Как считают А. Н. Воробьев и М. С. Киреева (1961), подобная реакция связана со снижением резистентности форменных элементов, но в основном она происходит за счет поступления тканевой жидкости в кровеносное русло из-за увеличения хлоридов в крови вследствие усиленного потоотделения при мышечной деятельности. Одновременно наступает нарастание количества ретикулоцитов вследствие увеличения их выработки костным мозгом в результате раздражения его продуктами распада эритроцитов и усиленного созревания эритробластов в костном мозге [17].
Другим важным показателем системы крови, который заслуживает внимания спортивного врача, являются тромбоциты. Помимо своей роли в свертывающей системе, они могут влиять на агрегацию эритроцитов, способствуя тем самым ухудшению кислородтранспортной функции крови. В работах А. М. Ефименко (1980), А. В. Мурашко и соавт. (1985), С. В. Коновалова (1986) и др. показано, что под влиянием физической нагрузки увеличиваются количество тромбоцитов, агрегация как тромбоцитов, так и эритроцитов. Можно считать, что определение этих показателей будет иметь значение как критерий оценки функционального состояния спортсменов. Проведенные исследования, как у спортсменов, так и у не занимающихся спортом, выявили определенную взаимосвязь между уровнем функционального состояния и агрегацией тромбоцитов и эритроцитов. Так, под влиянием физической нагрузки у лиц с недостаточно высоким уровнем функционального состояния отмечалось значительное увеличение указанных показателей. Следует полагать, что это связано с нарушениями в системе микроциркуляции и вполне закономерно.
Таким образом, под влиянием физической нагрузки в периферической крови человека наблюдаются эритро-, тромбо- и лейкоцитоз, изменение лейкоцитарной формулы, степень выраженности которых зависит от мощности и интенсивности нагрузки [18, 19].
Показатели количества эритроцитов, лейкоцитов и гемоглобина в периферической крови после физической нагрузки увеличивается у всех испытуемых, а через 30 мин отдыха возвращается к исходному уровню в покое. Степень этих изменений не зависит от спортивного мастерства и стажа.
Таким образом, можно полагать, что изменение картины периферической крови
способно отражать те изменения, которые наступают в организме человека в ответ на
физическую нагрузку. При этом об его приспособленности к выполнению нагрузки
можно судить по степени изменения указанных показателей [20].
2. Объект, программа и методика исследований
.1 Объект и программа исследований
Объектом исследований являются показатели периферической крови человека.
Предметом исследований являются влияние физической нагрузки на вариацию
показатели периферической крови. Для достижения поставленной цели на базе УО
«Гомельская федерация Джиу-джитсу» в течение двух месяцев проводилось
обследование группы мужчин в возрасте от 20-ти до 35-ти лет. Всего обследовано
57 человек, которые на протяжении более чем трех лет регулярно занимались
данным видом спорта. В таблице 2 представлен состав обследованной группы по
стажу спортивных тренировок.
Таблица 2 - Состав обследованной группы по стажу
|
К-во обследованных |
Стаж занятий, лет |
|
11 |
<1 |
|
33 |
1-3 |
|
13 |
>3 |
Перед выполнением специальных упражнений на занятие в течение 30 минут проводилась стандартная тренировка, которая включает: 15 минут бег в умеренном темпе (30 м/мин), 15 минут комплекс силовых упражнений (подтягивания 20 раз в минуту, отжимания от пола 50 раз в минуту, приседания 50 раз в минуту). После выполнения разминочных упражнений участники 30 минут выполняли элементы спарринга (броски). Начальный этап тренировки можно охарактеризовать как комплекс упражнений средней аэробной мощности, которому соответствует уровень потребления кислорода 55-65% от индивидуального максимального поглощения. Это упражнения, при выполнении которых почти вся энергия рабочих мышц обеспечивается аэробными процессами. Основным энергетическим субстратом служат жиры рабочих мышц и крови, в меньшей степени значение имеют углеводы (дыхательный коэффициент около 0,8). Предельная продолжительность таких упражнений до нескольких часов. Заключительный этап тренировки (спарринг) сочетает скоростно-силовые упражнения со статическим напряжением мышечной системы (броски и захваты). Статическое напряжение адаптировано к работе преимущественно в анаэробном режиме. Расход энергии при борьбе очень высокий. При выполнении захвата он достигает в среднем 10-12 ккал и более за 1 мин. Частота дыхательных движений во время выполнения элемента увеличивается до 35-40 и более движений в минуту [10].
Проведение обследования включало забор периферической крови до начало выполнения упражнений и сразу после окончания. Методика включала стандартную процедуру взятия капиллярной крови из пальца в мини-контейнер, содержащий консервант и антикоагулянт трилон-В. В течение часа пробы были доставлены в клинико-диагностическую лабораторию ГУ «ГГКБ №3» и обработаны на автоматическом гематологическом анализаторе SISMYX-500,предназначенном для диагностики in vitro. В основе работы анализатора используется метод проточной флуоресцентной цитометрии с использованием полупроводникового лазера. Эритроциты и тромбоциты анализировались с помощью эритроцитарного детектора, использовался метод гидродинамической фокусировки [11].
Таким образом, по результатам обследования были получены показатели общего анализа крови:
) концентрации гемоглобина;
) количество эритроцитов;
) количество лейкоцитов;
) количество тромбоцитов.
Программа исследования включала в себя решение следующих задач:
1) Анализ источников литературы по теме исследования;
) Отработка методики;
) Проведение обследования и сбор экспериментальных данных;
) Анализ и статистическая обработка полученных данных;
) Оформление курсовой работы по ГОСТу.
.2 Методика исследований
Забор крови, с последующим её исследованием производился у мужчин в
возрасте от 20-ти до 35-ти лет, до и после физической нагрузки. В исследовании
приняла участие группа из тридцати трёх человек, каждый из которой, после
взятия пробы до физической нагрузки, проходил стандартную тренировку в течение
часа. В таблице 3 сведены типы и продолжительность упражнений, которым
подвергались все испытуемые.
Таблица 3 - типы физической нагрузки, применяемой в исследовании
|
Тип физической нагрузки |
Продолжительность, мин |
Темп выполнения |
|
Бег |
15 |
Средний |
|
Комплекс упражнений |
15 |
Ускоренный |
|
Спарринг |
30 |
Средний |
Тренировка включала в себя 15 минут бега в нормальном темпе (один тридцатиметровый круг в минуту); выполнение комплекса упражнений (подтягивания, отжимания от пола, приседания) в течение 15 минут в ускоренном темпе (20 подтягиваний в минуту, 50 приседаний в минуту, 30 отжиманий в минуту); 30 минутный спарринг в нормальном темпе (20-25 бросков в минуту). По окончанию тренировки вновь бралась проба такого же объёма, у тех же испытуемых, что и до тренировки.
2.2.1 Техника проведения общего анализа крови
Основные этапы выполнения общего анализа крови:
1 взятие материала;
приготовление мазков крови;
проведение анализов на гематологическом анализаторе;
фиксация мазков крови;
окраска мазков крови;
подсчёт лейкоцитарной формулы.
Взятие материала. Кровь для исследования получили путём прокола четвёртого пальца левой руки обследуемого слева от срединной линии на некотором расстоянии от ногтя. В зависимости от толщины кожи глубина прокола составляет 2-3 мм. Обработанная кожа пальца высыхает несколько секунд. Цель этого «высыхания» - исключить растекание крови по пальцу, а также гемолитического воздействия антисептика на эритроциты. Скарификатор одноразового использования плотно зажимается между указательным и большим пальцами правой руки; производится прокол. Прокол произвели перпендикулярно рисунку кожных покровов пальца, так как в этом случае происходит повреждение нескольких капилляров, ход которых совпадает с ходом линий кожного рисунка. Учитываем, что разрез произведённый параллельно кожным линиям, спадается, что затрудняет забор крови. Первую, выступившую каплю крови удалили ватным тампоном, а последующие были взяты на исследование. Взятую кровь поместили в пронумерованные и обработанные раствором антикоагулянта. Трилоном-Б, пластиковые микрокюветы. На следующем рисунке показаны одноразовые пластиковые микрокюветы, более удобные и безопасные в использовании, чем стеклянные пробирки.
Все манипуляции связанные с забором крови проводились используя
стерильные комплекты инструментов для взятия крови (капилляры Панченкова,
предметные стёкла, скарификаторы и микрокюветы). Для каждого обследуемого
использовалась индивидуальная пара перчаток и стерильных ватных укладок. Все
манипуляции проводились в соответствии с требованиями приказа №165 МЗ РБ от
25.11.2002 г «О методах стерилизации и дезинфекции в медицинских учреждениях»
[21].
Рисунок
1 - Микрокюветы с раствором антикоагулянта
Приготовление
мазков крови. Для изготовления мазка крови использовались тщательно
обезжиренные предметные стёкла. Мазок крови готовился шлифованным стеклом с
идеально ровным краем, ширина которого была приблизительно на 2-3 мм уже
предметного стекла. К куполу свеже выпущенной из прокола капли было сделано
прикосновение предметным стеклом на расстоянии 1,5-2 см от его края, не касаясь
кожи в месте прокола. Размер капли на стекле не менее 2-3 мм в диаметре.
Шлифованным стеклом, приставленным к предметному под углом 45°, быстрым
движением справа налево был сделан мазок. Критерием правильности выполненного мазка
является его полупрозрачность и желтоватый цвет. Техника приготовления мазка
крови представлена на следующем рисунке.
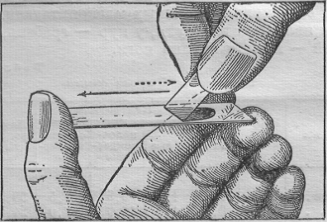
Рисунок
2 - Техника приготовления мазка крови
Проведение анализов на гематологическом анализаторе. Для исследований использовался гематологический анализатор SISMYX-500. Взятую кровь в миниёмкастях тщательно перемешали и поместили в загрузочную часть аппарата. Предварительно была проведена калибровка данного аппарата, которая заключалась в проведении полного анализа микрокюветы с дистиллированной водой. Определение параметров исследуемой крови протекает в автономном режиме, без непосредственного участия человека. По завершению цикла исследования сняли выданные аппаратом результаты [22].