Материал: Использование жидкостной хроматографии для контроля качества лекарственных средств, применяемых в медицине
· Предел обнаружения пика (соответствующий отношению сигнал/шум равному 3) находится ниже допустимого содержания примеси (порога, ниже которого присутствие примеси отрицается) в тесте на родственные соединения.
- Предел количественного определения пика (соответствующий отношению сигнал/шум равному 10) равен или меньше, чем порог обнаружения примесей (порог, при котором отрицается присутствие примеси) в тесте на родственные соединения. Проверка пригодности системы включена для того, чтобы гарантировать требуемое разделение для удовлетворительного проведения теста или количественного определения. Неподвижные фазы описаны только в общем виде, так как существует огромное количество их доступных коммерческих разновидностей, отличающихся по хроматографическому поведению и для того, чтобы достигнуть предписанных требований пригодности системы, в ряде случаев приходится вносить некоторые изменения в хроматографические условия. В методиках обращено-фазовой хроматографии, в особенности, регулирование различных параметров не всегда приводит к удовлетворительному разделению. В этом случае может возникнуть необходимость заменить одну колонку другой, обеспечивающей желаемое хроматографическое поведение, такого же типа (например, октадецилсиликагель), но от другого производителя.
Регулирование критических параметров для
гарантии пригодности системы чётко указывается в частной статье. Следует
избегать множественных изменений условий, которые могут оказать совместное
влияние на эффективность системы.
. Аппаратура для жидкостной хроматографии
В современной жидкостной хроматографии используют приборы различной степени сложности - от наиболее простых систем, до хроматографов высокого класса, снабженных различными дополнительными устройствами.[15]
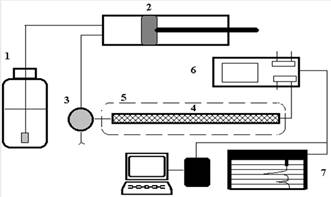
Рис.1 Блок-схема жидкостного хроматографа
- насос предназначен для создания постоянного потока растворителя. Его конструкция определяется, прежде всего, рабочим давлением в системе. Для работы в диапазоне 10-500 МПа используются насосы плунжерного (шприцевого), либо пистонного типов. Недостатком первых является необходимость периодических остановок для заполнения элюентом, а вторых - большая сложность конструкции и, как следствие, высокая цена. Для простых систем с невысокими рабочими давлениями 1-5 МПа с успехом применяют недорогие перистальтические насосы, но так как при этом трудно добиться постоянства давления и скорости потока, их использование ограничено препаративными задачами.
- инжектор,обеспечивающий ввод пробы смеси разделяемых компонентов в колонку с достаточно высокой воспроизводимостью( используют толстостенные стеклянные колонки).
- термостат обеспечивает постоянноство температуры.
- детектор(проточная кювета, в которой происходит непрерывное измерение какого-либо свойства протекающего элюента).
- регистрирующая система (дифференциальный усилитель или самописец).
Желательно также наличие интегратора,
позволяющего рассчитывать относительные площади получаемых пиков. В сложных
хроматографических системах используется блок интерфейса, соединяющий
хроматограф с персональным компьютером, который осуществляет не только сбор и
обработку информации, но и управляет прибором.[15]
. Жидкостную колоночную хроматографию
Жидкостную колоночную хроматографию используют преимущественно для выделения и очистки простых эфиров и перекисей. Классическую жидкостную колоночную хроматографию при низких давлениях и неоднородных сорбентах используют в основном для предварительного разделения. В подавляющем большинстве случаев применяют жидкостную хроматографию высокой эффективности ( ВЭЖХ) с высокими давлениями, обусловливающими высокие скорости разделения, и сорбентами высокой степени однородности.
Термин распределительная жидкостная колоночная хроматография, строго говоря, предполагает наличие двух жидких фаз, неподвижной и подвижной, при том, что неподвижность одной из них обусловлена ее связью с твердой матрицей, заполняющей хромато-графическую колонку. Этот вид хроматографии базируется на явлении растворимости. Движение хроматографических зон по колонке и элюция пиков подвижной фазой происходят в направлении от % менее гидрофильных к более гидрофильным компонентам смеси. При изократической элюции последние лишь понемногу и с трудом диффундируют от неподвижной водной фазы в подвижную. Для ускорения их элюции можно постепенно (градиентно) увеличивать полярность подвижной фазы, например уменьшая в ней содержание органического растворителя в пользу воды.
Основой жидкостной колоночной хроматографии является разделение веществ, находящихся в растворе (подвижная фаза), на колонках, заполненных неподвижной фазой. Подвижная фаза перемещается ( фильтруется) вдоль слоя неподвижной фазы со скоростью, зависящей от силы взаимодействия компонентов с подвижной и неподвижной фазами.[12]
7. Жидкостная бумажная хроматография
Жидкостная бумажная хроматография - хроматография на бумаге - метод разделения и анализа смесей веществ, основанный на их распределении между подвижной и неподвижной жидкими фазами; в качестве носителя неподвижной жидкой фазы используют бумагу. Метод предложен англ. учёными А. Мартином и Р. Синго в 1941. В Б. х. используют специальные сорта бумаги, различающиеся по номерам, с возрастанием к-рых плотность бумаги увеличивается. Бумага удерживает в порах воду, которая и является неподвижной жидкой фазой. Раствор пробы наносят в виде капель на лист бумаги на некотором расстоянии от края. После испарения растворителя край листа помещают в герметичную камеру, содержащую проявитель - подвижную жидкую фазу (напр., спирты, кетоны, фенолы, четырёххлористый углерод, хлороформ и др., их смеси, а также смеси с неорганического растворителями).
При этом происходит передвижение исходного пятна
по току проявителя и разделение смеси на компоненты. Если вещества не окрашены,
то хроматограмму проявляют, напр., опрыскиванием раствором индикатора,
рассматривают в ультрафиолетовых лучах и пр. Отношение расстояния Rf,
пройденного пятном I, к расстоянию, пройденному фронтом проявителя m, при
одинаковых условиях эксперимента является постоянной величиной; Rf для разл.
веществ отличаются по значению и могут быть использованы для идентификации
соединений. Количественные определения различных веществ в пятнах хроматограммы
ведутся обычными аналитическими методами. Различают одномерные, двумерные,
круговые, колоночные и электрофоретические хроматограммы. [11]
8. Жидкостно-адсорбционная хроматография
В основе адсорбционной хроматографии лежит различная адсорбционная способность компонентов разделяемой смеси на поверхности выбранного адсорбента. Адсорбенты представляют собой пористые твердые вещества с сильно развитой поверхностью. Адсорбент должен быть химически инертным к компонентам разделяемой смеси, избирательным , механически прочным и термически устойчивым. Наиболее широко применяемыми адсорбентами являются углекислый кальций, окись магния, окись кальция, окись алюминия, cиликагель, активированный уголь и цеолиты (алюмосиликаты). Одной из наиболее распространенных теорий адсорбции является теория Лэнгмюра. Согласно этой теории на поверхности твердого тела (адсорбента) имеются активные центры, на которых и происходит адсорбция молекул из раствора или газа.
Адсорбция обуславливается или физическими
ван-дер-ваальсовыми силами межмолекулярного взаимодействия (молекулярная
хроматография), или силами химического сродства, действующими, например, в
процессе реакции при обмене ионов разделяемых компонентов на подвижные ионы
применяемого ионообменного адсорбента (ионообменная хроматография). Адсорбция
зависит от температуры, концентрации раствора, давления газа, от природы
вещества и от природы и структуры адсорбента. [11]
. Эксклюзионная жидкостная хроматография
Эксклюзионная жидкостная хроматография - (ситовая хроматография), жидкостная хроматография, основанная на различной способности молекул разного размера проникать в поры неионогенного геля, который служит неподвижной фазой. Различают гель-проникающую хроматографию (элюент - орг. растворитель) и гель-фильтрацию (элюент - вода). Ддя эксклюзионной хроматографии используют макропористые неорганические. или полимерные сорбенты. Для эксклюзионной хроматографии полярных полимеров неорганические. сорбенты (силикагели и макропористые стекла) модифицируют кремнийорг. радикалами, а для эксклюзионной хроматографии гидрофильных полимеров -гидрофильными группами.
Среди полимерных сорбентов наиболее
распространены стирол-дивинилбензольные (для эксклюзионной хроматографии
высокополимеров и олигомеров). Для гель-фильтрации биополимеров, прежде всего
белков, используют гидрофильные полимерные сорбенты (сефадексы - декстраны с
поперечными сшивками, а также полиакриламидные гели) или модифицированные
полисахаридами макропористые силикагели. Эксклюзионную хроматографию эффективно
применяют при разработке новых полимеров, технологических процессов их
получения, контроле производства и стандартизации полимеров. Эксклюзионную
хроматографию используют для анализа ММР полимеров, исследования, выделения и
очистки полимеров, в т. ч. биополимеров.[12]
. Реакционная жидкостная хроматография
Реакционная жидкостная хроматография - метод
анализа и физ.-хим. исследования, в котором наряду с хроматографическим
разделением осуществляют химические превращения исследуемых веществ. Термин
"реакционная хроматография" применяют в основном в газовой
хроматографии. Аналогичные разновидности жидкостной хроматографии обычно
называют терминами, например "реакционное
детектирование"-совокупность методов превращения анализируемых соединения
после их выхода из колонки с целью улучшения характеристик последующего
детектирования, "химическая дериватизация" - методы получения
производных анализируемых соединения с целью улучшения характеристик разделения
и детектирования. Иногда ионообменную и лигандообменную (с использованием
хелатообразующих сорбентов) хроматографию рассматривают как частный случай
реакций жидкостной хроматографии. Химические реакции проводят в
хроматографической системе (в спец. микрореакторе или устройстве для ввода
пробы, хроматографич. колонке, детекторе) или вне ее для улучшения разделения
веществ, понижения предела их обнаружения, повышения селективности и т. д. [13]
. Контроль качества лекарственных средств
Контроль качества лекарственных средств можно
осуществить с помощью жидкостной хроматографии. Общие принципы использования
данных методов изложены в общих и частных фармакопейных статьях.
. Кальция глюконат для инъекций
Calcii gluconas at iniectabile GLUCONATE FOR INJECTION
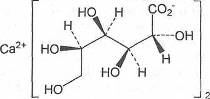
Определение
Кальция глюконат для инъекций содержит не менее 99,0% и не более 101,0% кальция D-глюконата моногидрата. Белый или почти белый кристаллический или гранулированный порошок. Умеренно растворим в воде, легкорастворим в кипящей воде.
Применение жидкостной хроматографии для испытания данного вещества на примеси - оксалаты.
Оксалаты. Не более 0,01 % (100 ррт). Жидкостная хроматография
Испытуемый раствор. 1,00 г испытуемого образна растворяют в воде для хроматографии. Р и доводят до объема 100,0 мл этим же растворителем.
Раствор сравнения. 1,00 г испытуемого .образца растворяют в воде для хроматографии Р. прибавляют 0,5 мл раствора 0,152 г/л натрия оксалата Р в воде для хроматографии Р и доводят водой для хроматографии Р до объема 100,0 мл.
Условия хроматографирования:
- предколонка длиной 30 мм и внутренним диаметром 4 мм, заполненная подходящей смолой анионообменной сильноосновной с размером частиц 30-50 мкм;
- колонки 1 и 2 длиной 0,25 м и внутренним диаметром 4 мм, заполненные подходящей смолой анионообменной сильноосновной с размером частиц 30-50 мкм;
- анион-подавляющая колонка: расположена между предколонкой и аналитическими колонками, снабжена микромембраной, которая отделяет подвижную фазу от регенерирующего раствора, двигающегося противотоком подвижной фазе;
подвижная фаза: 0,212 г натрия карбоната безводного Р и 63 мг натрия гидрокарбоната Р
- растворяют в воде для хроматографии Р и доводят до объема 1000,0 мл этим же растворителем;
- скорость подвижной фазы: 2 мл/мин;
- регенерирующий раствор: раствор 1,23 г/л кислоты серной Р в воде для хроматографии Р;
- скорость регенерирующего раствора:
- мл/мин;
- кондуктометрический детектор;
- объем вводимой пробы: по 50 мкл каждого раствора трижды.
Пригодность хроматографической системы: раствор сравнения:
- относительное стандартное отклонение: не более 2,0% для пика оксалата при пяти повторных вводах пробы.
Содержание оксалатов в одной части на миллион частей (ррт) рассчитывают по формуле:
ST -50
SR
-ST
где: ST - площадь пика оксалата на хроматограмме испытуемого раствора:
SR
- площадь пика оксалата на хроматограмме раствора сравнения.[1,6]
13.
Бетаметазона
валериат
Betamethasoni valeras
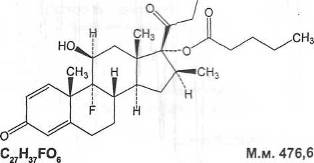
BETAMETHASONE
VALE
диен-17-илпентаноата в пересчете на сухое вещество.
Описание (свойства)
Белый или почти белый кристаллический порошок.
Практически нерастворим в воде, легкорастворим в ацетоне и в метилехлориде, растворим в 96% спирте.
Температура плавления: около 192°С (с разложением).
Применение жидкостной хроматографии для испытания данного вещества на примеси - сопутствующие примеси.
Раствор А. К 1000 мл подвижной фазь прибавляют 1 мл кислоты уксусной ледяно1 Р и тщательно перемешивают.
Испытуемый раствор. 62,5 мг испытуе мого образца растворяют в растворе А и до водят до объема 25,0 мл этим же раствори телем.
Раствор сравнения (а). 2 мг ФСО бетаметазона 17-валериата и 2 мг ФСО бетаметазона 21-валериата растворяют в растворе А и доводят до объема 50,0 мл этим же растворителем.
Раствор сравнения (Ь). 1,0 мл испытуемого раствора доводят раствором А до объема 50,0 мл.
Условия хроматографирования:
- колонка из нержавеющей стали длиной 0,25 м и внутренним диаметром 4,6 мм, заполненная силикагелем октадецилсилильным для хроматографии Р с размером частиц 5 мкм;
- подвижная фаза: смешивают 350 мл воды Р с 600 мл ацетонитрила Р, выдерживают до установления равновесия, доводят объем раствора водой Р до объема 1000 мл и снова перемешивают;
- скорость подвижной фазы: 1 мл/мин;
- спектрофотометрический детектор, длина волны 254 нм;
- объем вводимой пробы: 20 мкл;
- время установления равновесия: не менее 45 мин;
- время хроматографирования: 2,5-крат- ное время удерживания бетаметазона 17-валериата.
Время удерживания пиков (раствор сравнения (а)): бетаметазона 17-валериат - около
- мин; бетаметазона 21-валериат - около
- мин.
Пригодность хроматографической системы: раствор сравнения (а):
разрешение: не менее 5,0 между пиками бетаметазона 17-валериата и бетаметазона 21-валериата; при необходимости изменяют концентрацию ацетонитрила в подвижной фазе.
Предельное содержание примесей:
любая примесь (не более 1,5%): на хроматограмме испытуемого раствора площадь любого пика, кроме основного, не должна превышать 0,75 площади основного пика на хроматограмме раствора сравнения (Ь), и площадь не более чем одного из таких пиков может превышать 0,5 площади основного пика на хроматограмме раствора сравнения (Ь) (1 %);
сумма примесей (не более 3,0%): на хроматограмме испытуемого раствора сумма площадей всех пиков, кроме основного, не должна превышать 1,5-кратную площадь основного пика на хроматограмме раствора сравнения (Ь).
На хроматограмме испытуемого раствора не
учитывают пики с площадью менее 0,025 площади основного пика на хроматограмме
раствора сравнения (Ь) (0,05%).[6]
14.
Бетаметазона
дипропионат
Betamethasoni dipropionas DIPROPIONATE
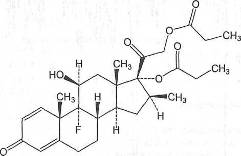
C28H37F07 Mm.
504,6
Определение
Бетаметазона дипропионат содержит не менее 97,0% и не более 103,0% 9-фтор-11р- гидрокси-16(3-метил-3,20-диоксопрегна-1,4- диен-17,21-диилдипропионата в пересчете на сухое вещество.